砷是国际癌症研究机构(International Agency form Research on Cancer,IARC)明确的人类I类致癌物。流行病学调查发现饮水慢性砷暴露与人群学习记忆和认知能力损伤相关[1]。Mong等[2]研究表明小鼠慢性砷暴露后出现学习记忆能力损伤。小胶质细胞是脑内唯一的实质细胞,参与脑内炎症反应[3]。小胶质细胞的活化是脑内神经炎症的标志且在学习记忆损伤中起着重要作用[4]。环氧化酶 – 2(cyclooxygenase-2,COX-2)是小胶质细胞活化的标志 [5],是与认知损伤密切相关的前列腺素的关键前体限速酶[6]。本研究以C57BL/6J雄性小鼠为研究对象建立亚砷酸钠饮水染毒模型,通过检测小鼠海马中COX-2、核因子κB p65(nuclear factor kappa B p65,NF-κB p65)蛋白表达和白细胞介素 – 6(interleukin-6,IL-6)、肿瘤坏死因子α(tumor necrosis factor alpha,TNF-α)的含量,探讨COX-2在亚砷酸钠介导的神经毒性中对小胶质细胞的作用,为深入研究砷中毒介导的神经毒性提供实验依据。结果报告如下。
1 材料与方法 1.1 实验动物与分组清洁级C57BL/6J雄性小鼠20只,购于重庆医科大学动物实验中心,许可证号:SYXK(渝)2018 – 0003。实验前适应性饲养小鼠1周,昼夜12 h循环,自由进水进食。适应饲养1周后,将小鼠随机分为对照组和砷暴露组,每组10只,自由饮水染毒12周。根据课题组前期研究选用50 mg/L作为砷暴露组小鼠染毒剂量 [7]。
1.2 主要仪器与试剂酶标仪(美国Themo公司),超速低温离心机(美国Sigma公司),移液枪(德国Eppendof公司),荧光显微镜(日本Olympus公司),电泳仪(美国BIO-RAD公司),亚砷酸钠(美国Sigma公司),小鼠IL-6、小鼠TNF-α、FITC标记驴抗兔荧光二抗(中国博士德生物工程有限公司),IBA-1、NF-κB p65、COX-2、β-actin兔抗鼠单克隆抗体(美国Cell Signal Technology公司)
1.3 指标与方法 1.3.1 Morris水迷宫行为学测试(1)定位航行实验:连续训练5 d,每天4次;将小鼠头朝池壁分别从4个不同象限下水寻找目标平台,记录小鼠成功找到平台时间,即逃避潜伏期。(2)空间探索实验:去除平台,记录60 s内小鼠在目标象限的停留距离,检测小鼠对目标象限的记忆保持能力。
1.3.2 海马病理结构观察将5 μm小鼠海马冠状面石蜡切片脱蜡,苏木精-伊红(hematoxylin-eosin,HE)染色法染色,70 % 乙醇洗涤2次后,脱水、透明、封片后光镜下观察(400 ×)。
1.3.3 海马超微结构观察将钝性分离的脑海马组织快速切割成1 mm3;浸润于2.5 % 戊二醛4 ℃固定24 h;磷酸盐缓冲液(phosphate-buffered saline,PBS)漂洗3次,每次15 min;1 % 锇酸中固定2 h后丙酮脱水;环氧树脂包埋制成1 μm超薄切片,饱和醋酸铀染色,透射电子显微镜观察超微结构(20 000 ×)。
1.3.4 小鼠海马IBA-1表达检测采用免疫荧光法,将小鼠大脑置于4 % 多聚甲醛溶液中固定,常规脱水,石蜡包埋,连续冠状面切片(5 μm)。切片经过60 ℃常规烤片、脱蜡、水化后,进行微波抗原修复,PBS清洗,加入5 % BSA室温封闭30 min后加入IBA-1(1 ∶ 1 000)一抗,4 ℃孵育过夜。第二天清洗切片,滴加荧光二抗,室温孵育1 h,PBS清洗后DAPI染核,常规清洗加入抗荧光淬灭剂封片,荧光显微镜观察。
1.3.5 IBA-1、COX-2、NF-κBp65蛋白表达检测采用蛋白印迹(Western blot,WB)法,染毒结束后,断颈处死小鼠,称取0.1 g小鼠脑海马组织,加入组织裂解液冰上匀浆裂解提取蛋白,二喹啉甲酸试剂盒(bicinchoninic acid,BCA)测定蛋白浓度,凝胶电泳参照文献[8]。IBA-1、COX-2、NF-κBp65和 β-actin抗体的稀释比例分别为1 ∶ 1 000、1 ∶ 1 000、1 ∶ 1 000和1 ∶ 3 000。使用Image J软件分析目的条带光密度值,计算目的蛋白相对表达量。
1.3.6 海马组织中IL-6、TNF-α含量检测采用ELISA法,称取0.1 g小鼠海马组织加入1 mL生理盐水(0.9 % NaCl)匀浆,根据ELISA试剂盒说明书操作,通过绘制标准曲线计算小鼠海马IL-6和TNF-α含量。
1.4 统计分析数据用
对照组和砷暴露组小鼠体重分别为(26.53 ± 0.93)和(25.88 ± 0.95)g,差异无统计学意义(t = 1.209,P = 0.255)。
2.2 NaAsO2对小鼠学习记忆能力影响(表1)|
表 1 砷暴露对小鼠学习记忆能力影响(
|
与对照组比较,砷暴露组小鼠第5天逃避潜伏期明显延长(P < 0.05);空间探索实验结果显示,与对照组比较,砷暴露组小鼠有效停留距离明显缩短( P < 0.05)。
2.3 NaAsO2对小鼠海马组织病理影响(图1)
|
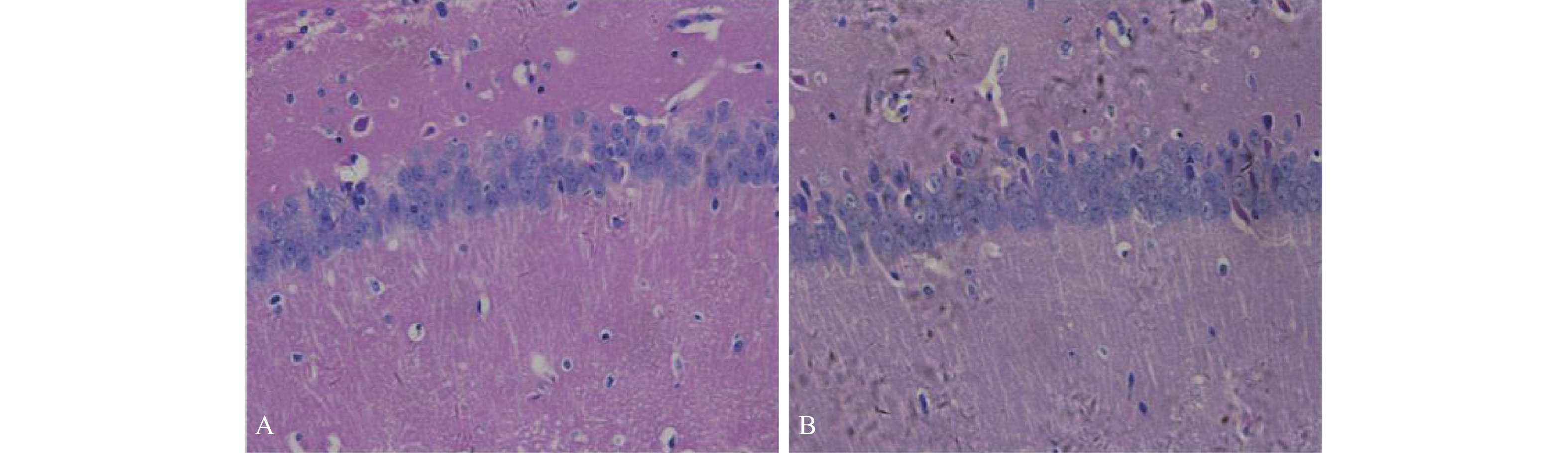
注:A对照组;B砷暴露组。 图 1 砷暴露对小鼠海马组织病理学影响(HE,× 400) |
结果显示,对照组小鼠海马锥体细胞结构正常,排列整齐(图1A),而砷暴露组小鼠部分海马锥体细胞出现核固缩,胞浆深染,空泡增多等损伤表现(图1B)。
2.4 NaAsO2对小鼠海马超微结构影响(图2)

|
注:A:对照组;B:砷暴露组 图 2 砷暴露对小鼠海马组织超微结构影响(× 20 000) |
对照组小鼠海马组织粗面内质网均匀,线粒体可见脊(图2A),砷暴露组小鼠脑海马组织细胞器可见显著水肿,空泡,线粒体见明显脊减少或空泡样改变,粗面内质网扩张(图2B)。
2.5 NaAsO2对小鼠海马IBA-1表达影响(图3)

|
注:A:对照组;B:砷暴露组 图 3 砷暴露对小鼠海马IBA-1表达影响(荧光染色,× 400) |
与对照组比较,砷暴露组小鼠海马区可见明显的小胶质细胞表达(绿色荧光)增多。
2.6 NaAsO2对小鼠海马IBA-1、COX-2和NF-κBp65蛋白表达影响(图4、表2)
|
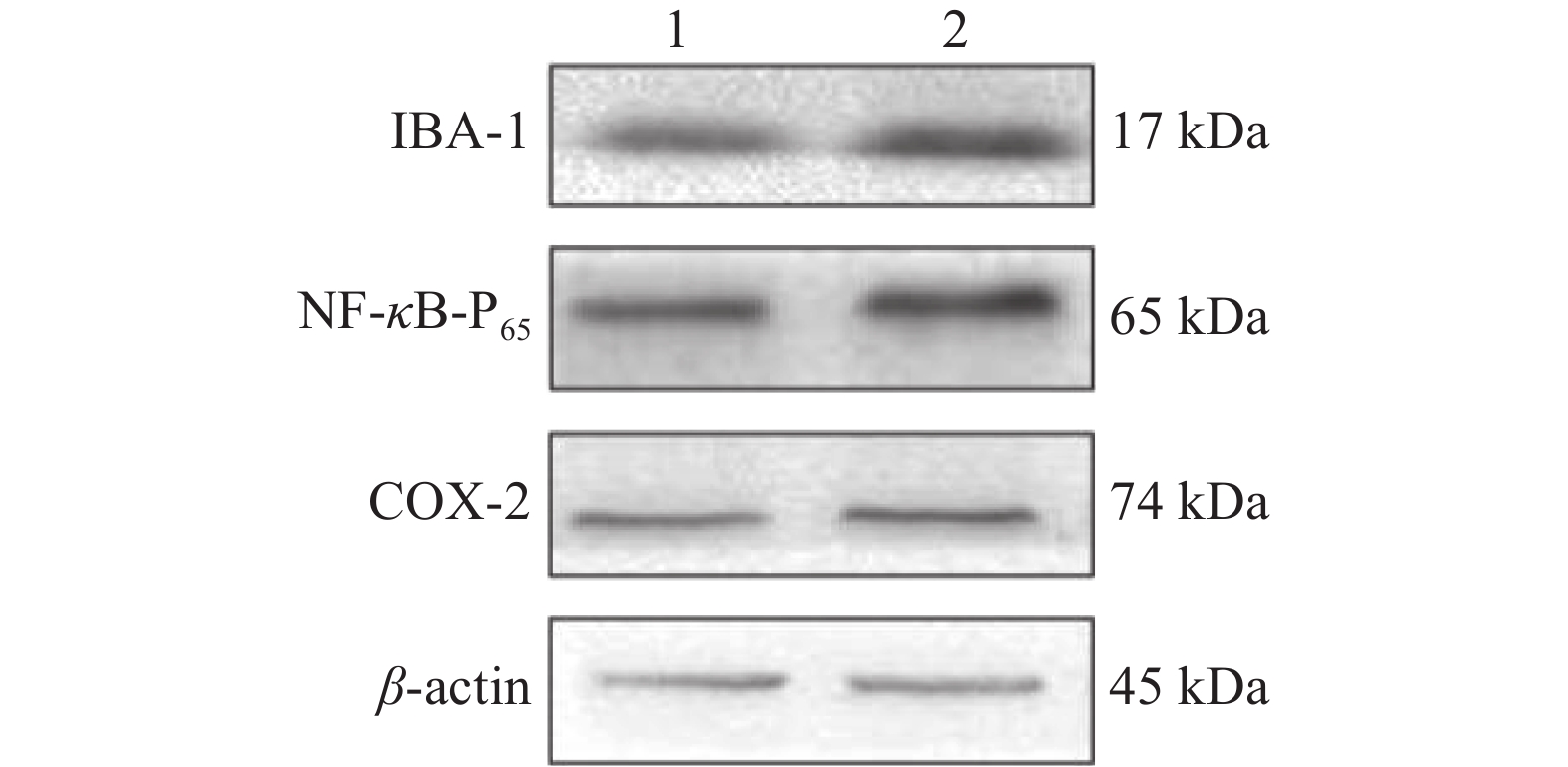
注:1:对照组;2:砷暴露组 图 4 砷暴露对小鼠海马IBA-1、COX-2、NF-κBp65蛋白表达影响 |
|
表 2 砷暴露对小鼠海马IBA-1、NF-κB p65、COX-2蛋白表达影响(
|
结果显示,与对照组比较,砷暴露组小鼠海马IBA-1、NF-κBp65和COX-2蛋白表达水平均明显增加(P < 0.05)。
2.7 NaAsO2对小鼠海马组织中IL-6和TNF-α含量影响对照组、砷暴露组小鼠海马组织中IL-6和TNF-α含量分别为(43.37 ± 1.11)、(198.46 ± 9.93)pg/mL和(93.61 ± 3.18)、(604.00 ± 25.02)pg/mL;与对照组比较,砷暴露组小鼠海马组织中IL-6和TNF-α含量均明显升高,差异有统计学意义(t = − 36.521、− 36.908,P < 0.01)。
3 讨 论砷毒性的重要靶点为神经系统,研究发现砷可以在脑内蓄积[7],慢性砷暴露与神经退行性疾病相关,如阿尔茨海默病、帕金森病等[9]。血脑屏障(blood brain barrier,BBB)由脑内毛细血管网与胶质细胞组成,是维护脑内环境稳定,阻止有害物质进入脑的屏障。砷可以通过改变血脑屏障的通透性在脑内蓄积介导神经炎症反应[2, 10]。Morris水迷宫实验是评估啮齿动物空间学习与记忆的常用方法[11]。本研究结果显示,小鼠饮水砷暴露后,学习记忆损伤,小鼠海马出现超微结构和病理改变。提示,慢性砷暴露小鼠模型建立成功。小胶质细胞作为脑内唯一的实质细胞,在神经炎症和免疫调节中起着重要作用[3]。IBA-1为小胶质细胞的标志物,本研究结果显示,与对照组比较,砷暴露组小鼠海马IBA-1绿色荧光表达明显增加,出现小胶质细胞活化形态的经典改变,即分枝状消失,胞体变圆,呈“阿米巴样”。提示,慢性砷暴露小鼠学习记忆能力损伤与小胶质细胞活化有关。
小胶质细胞的活化在阿尔兹海默症、帕金森病等神经退行性病变中起着重要作用。活化的小胶质细胞通过释放IL-6、TNF-α等促炎性细胞因子诱导神经元死亡[12]。慢性神经退行性疾病(如阿尔茨海默症)中NF-κB在神经元和胶质细胞中被激活[13]。NF-κB在学习和记忆等过程中发挥重要作用,其中NF-κB p65为炎症信号通路关键开关[14]。被激活的NF-κB通过细胞质进入细胞核,表达下游的COX-2和TNF-α[15]。COX-2是前列腺素合成过程中的重要限速酶,在神经炎症介导的学习记忆损伤中起着重要作用[16],是小胶质细胞活化的标志之一[5]。张宗奇等[17]研究发现脂多糖诱导的小鼠及原代小胶质细胞神经炎症模型中,COX-2蛋白表达升高。本研究结果显示,砷暴露组小鼠海马NF-κB p65、COX-2蛋白表达上调,IL-6和TNF-α含量明显高于对照组。推测慢性砷暴露小鼠学习记忆能力损伤与海马区小胶质细胞活化,激活NF-κB p65上调COX-2,分泌促炎性因子IL-6和TNF-α导致神经毒性有关。其详细机制还需要进一步的深入研究。
| [1] | Wasserman GA, Liu X, Parvez F, et al. A cross-sectional study of water arsenic exposure and intellectual function in adolescence in Araihazar, Bangladesh[J]. Environ Int, 2018, 118: 304–313. DOI:10.1016/j.envint.2018.05.037 |
| [2] | Mo TT, Dai H, Du H, et al. Gas chromatography-mass spectrometry based metabolomics profile of hippocampus and cerebellum in mice after chronic arsenic exposure[J]. Environ Toxicol, 2019, 34(2): 103–111. DOI:10.1002/tox.v34.2 |
| [3] | Wolf SA, Boddeke HW, Kettenmann H. Microglia in physiology and disease[J]. Annu Rev Physiol, 2017, 79: 619–643. DOI:10.1146/annurev-physiol-022516-034406 |
| [4] | Zhou T, Huang Z, Sun X, et al. Microglia polarization with M1/M2 phenotype changes in rd1 mouse model of retinal degeneration[J]. Front Neuroanat, 2017, 11: 77. DOI:10.3389/fnana.2017.00077 |
| [5] | Plastira I, Bernhart E, Goeritzer M, et al. 1-Oleyl-lysophosphatidic acid (LPA) promotes polarization of BV-2 and primary murine microglia towards an M1-like phenotype[J]. J Neuroinflammation, 2016, 13(1): 205. DOI:10.1186/s12974-016-0701-9 |
| [6] | Hein AM, O'banion MK. Neuroinflammation and memory: the role of prostaglandins[J]. Mol Neurobiol, 2009, 40(1): 15–32. DOI:10.1007/s12035-009-8066-z |
| [7] | Dai H, Xia YY, Han TH, et al. Effect of chronic arsenic exposure on mouse brain tissue and serum metabolomics[J]. Nan Fang Yi Ke Da Xue Xue Bao, 2016, 36(9): 1192–1197. |
| [8] | Bai L, Tang Q, Zou Z, et al. m6A Demethylase FTO regulates dopaminergic neurotransmission deficits caused by arsenite[J]. Toxicol Sci, 2018, 165(2): 431–446. DOI:10.1093/toxsci/kfy172 |
| [9] | 关怀, 朴丰源. 砷神经发育毒性及机制研究进展[J]. 中国公共卫生, 2015, 31(04): 538–540. |
| [10] | Singh V, Kushwaha S, Gera R, et al. Sneaky entry of IFNgamma through arsenic-induced leaky blood-brain barrier reduces CD200 expression by microglial pro-inflammatory cytokine[J]. Mol Neurobiol, 2019, 56(2): 1488–1499. DOI:10.1007/s12035-018-1155-0 |
| [11] | Vorhees CV, Williams MT. Assessing spatial learning and memory in rodents[J]. ILAR J, 2014, 55(2): 310–332. DOI:10.1093/ilar/ilu013 |
| [12] | Andreasson KI, Bachstetter AD, Colonna M, et al. Targeting innate immunity for neurodegenerative disorders of the central nervous system[J]. J Neurochem, 2016, 138(5): 653–693. DOI:10.1111/jnc.13667 |
| [13] | Mattson MP. NF-kappaB in the survival and plasticity of neurons[J]. Neurochem Res, 2005, 30(6 – 7): 883–893. DOI:10.1007/s11064-005-6961-x |
| [14] | 周彬, 吴琳, 凌叶盛, 等. 人参皂苷Rb1通过抑制NF-κB p65介导的炎症和氧化应激改善内皮细胞复制性衰老[J]. 中山大学学报: 医学版, 2018, 39(06): 835–843. |
| [15] | Natarajan K, Abraham P, Kota R, et al. NF-κB-iNOS-COX2-TNF α inflammatory signaling pathway plays an important role in methotrexate induced small intestinal injury in rats[J]. Food and chemical toxicology, 2018, 118: 766–783. DOI:10.1016/j.fct.2018.06.040 |
| [16] | Sil S, Ghosh T. Role of cox-2 mediated neuroinflammation on the neurodegeneration and cognitive impairments in colchicine induced rat model of Alzheimer's Disease[J]. J Neuroimmunol, 2016, 291: 115–124. DOI:10.1016/j.jneuroim.2015.12.003 |
| [17] | 张宗奇, 付岩, 杨拼, 等. 桂皮醛对小胶质细胞激活和COX-2表达的影响[J]. 中药药理与临床, 2017, 33(03): 34–38. |
 2019, Vol. 35
2019, Vol. 35


