2. 中国科学院武汉病毒研究所
埃博拉病毒病,又称埃博拉出血热,属丝状病毒科,有扎伊尔型、本迪布焦型、苏丹型、莱斯顿型和塔伊森林型5个亚型,其中扎伊尔型毒力最高,引起2014年西非埃博拉重大疫情的即为该类型[1 – 2]。截至2016年4月,世界共报告病例28 616例,死亡病例11 310个。作为新发和烈性传染病的代表之一,埃博拉病毒病有以下特点:(1)1976年首次爆发,并于2014年再次爆发并有史以来规模最大;现仍在西非地区持续蔓延,且未来仍有爆发可能;(2)埃博拉病毒致死率高达90 %,被世界卫生组织(World Health Organization,WHO)定义为最高级别烈性病毒(4级);(3)疫情波及全球[3 – 4]。本研究收集2007 — 2017年间的埃博拉病毒研究论文,对该病毒研究现状和发展态势进行分析,为我国埃博拉病毒病及其他新发和烈性传染病防治和国家生物安全政策制定提供参考。
1 资料与方法 1.1 数据来源论文数据来自Web of Science数据库,检索式为TS = (”ebola”),检索时间范围:1900 — 2017,检索索引:SCI-EXPANDED,数据检索时间为2017年7月26日。
1.2 方法论文数据清洗和文献计量分析使用Thomson Data Analyzer软件。科学知识图谱部分,论文共引分析使用CiteSpaceⅤ进行分析和结果可视化,共词和聚类分析使用VOSViewer进行研究热点和趋势分析。
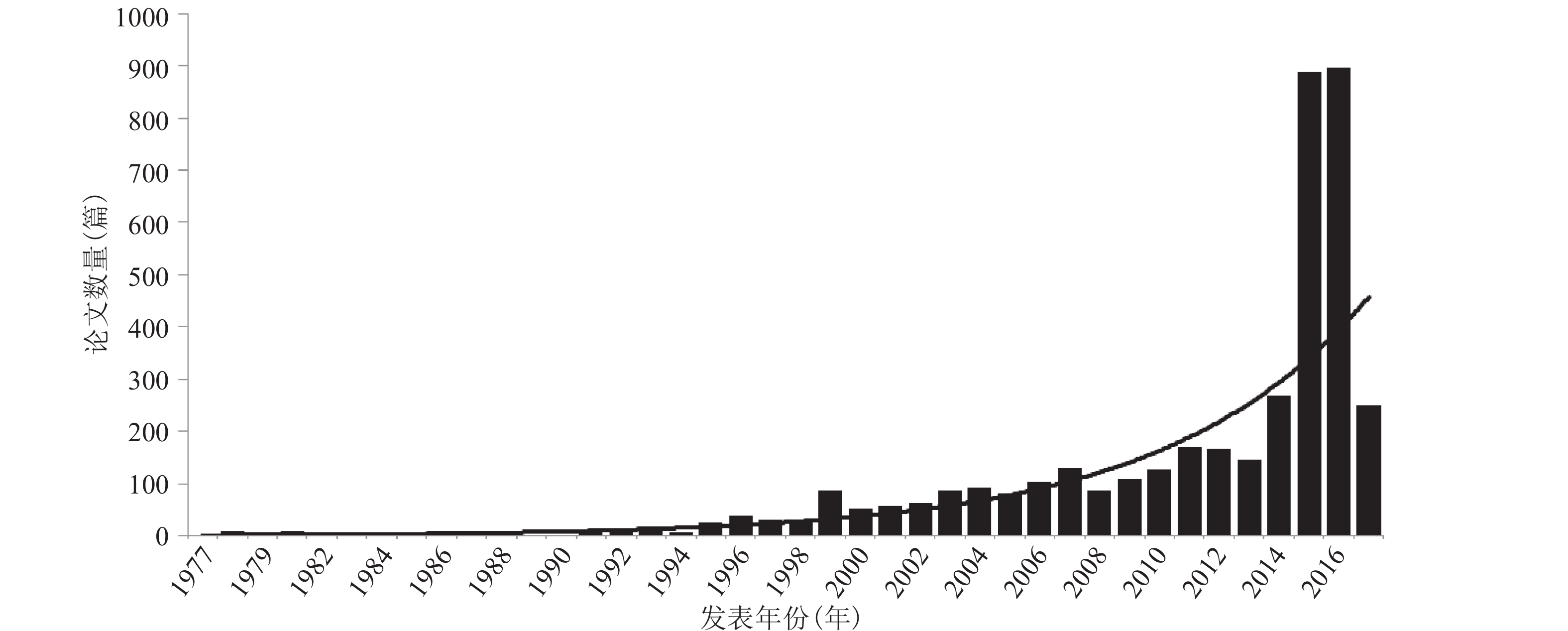
2 结 果 2.1 埃博拉病毒研究论文发表概况(图1)
|
图 1 1977 — 2017年世界埃博拉病毒研究论文发表概况 |
本文共检索到埃博拉病毒领域科技论文4 086篇,发表时间分布上可分为3个阶段:1977 — 1994,期间的相关文章很少,平均每年5.8篇;1995 — 2013,2005年之前数量均 < 100篇,2006 — 2013年维持在100~200篇;2014 — 2017,2014年开始文章数量增长迅速;2015年发表文章887篇,为2014年的3倍多。论文增长背后反映出近年来,尤其是2014年西非大规模埃博拉疫情以后,世界各国已意识到埃博拉病毒病作为新发和烈性传染病的风险和潜在的生物安全威胁。
2.2 埃博拉病毒研究领域的重要国家(表1、图2)| 表 1 埃博拉病毒研究领域的重要前10个国家及其文章影响力 |

|
图 2 埃博拉病毒研究领域国家间合作网络 |
(1)国家排名:美国文章数量遥遥领先,发表文章2 313篇,占总量的56.6 %;英国、德国、加拿大、法国在世界前5名之列;中国发表文章221篇,排名第6;我国自2003年首次发表埃博拉病毒论文,在该领域起步较晚。(2)论文影响力:美国总被引频次排名第1,但篇均被引频次位于德国、瑞士和法国之后;我国总被引频次和篇均被引频次分别排第9和第10,学术影响力落后于美国和欧洲等发达国家。(3)国际合作:美国在该领域国际合作网络中处重要中心地位;美国、加拿大、英国、法国、德国、日本等发达国家间合作很紧密;除美国外,我国与加拿大、英国、塞拉利昂、澳大利亚和新加坡有合作。
2.3 埃博拉病毒研究论文共被引分析(图3)

|
注:图中圆圈越大表明论文被引越多。中心度值大的文章也在图中以紫色圆圈突显。 图 3 CiteSpaceV绘制的埃博拉病毒论文共引图谱 |
通过CiteSpace得到2007 — 2017年间埃博拉研究论文的共引图谱,包括节点数255个、连线数719个。基于该网络可知,(1)高被引论文。高被引文章一定程度上反映了其在该领域中的重要地位。近10年间被引频次排名第1的是2011年Feldmann等[5]《柳叶刀》上的文章,系统介绍了埃博拉病毒病的流行病学、生态学、临床表现、发病机制、诊断、治疗和预防。其次排第2和第3的是2014年3月几内亚等地发生大规模出血热后《New England Journal of Medicine》同期发表的2篇论文。一篇是Baize等[6]通过全基因组测序、系统进化分析及结合临床数据确定了几内亚疫情的病原体是扎伊尔型病毒;另一篇是Aylward等[4]对2014年3月至9月期间的4 010例感染病例进行分析并对今后的疫情发展进行了预测。(2)重要转折性文章。CiteSpace中高中心度(centrality)的文章表明在本领域中具有转折性作用。中心度最高的是2007年Feldmann等[7]研究了一种重组水泡性口炎病毒载体疫苗,在豚鼠和小鼠感染埃博拉病毒24 h后使用分别可达50 %和100 %的保护效果,更重要的是对8只的恒河猴中使4只得到了保护。其次是2010年Geisbert等[8]提供了一种在非人灵长类动物中使用小干扰RNA成功实现埃博拉病毒保护的方法。这些文章为当时的埃博拉病毒病疫情防治提供了可能方法,在新发和烈性传染病的治疗领域具有重要意义,也侧面表明埃博拉及新发和烈性传染病治疗研究是近年来的热点研究方向。
2.4 埃博拉病毒领域研究热点识别和趋势分析(图4)

|
图 4 VOSViewer绘制的埃博拉病毒论文共词图谱(上图)和关键词年度分布图(下图) |
(1)领域热点方向:用论文中出现频次10次以上的关键词绘制关键词共现图谱,得到6个聚类,代表该领域的6个主要研究方向:①病毒的传播、流行病学和病毒进化研究。主要关键词有outbreak、transmission、West-Africa、epidemiology、fruit bats、evolution、sequence alignment、phylogenetic analysis等。病毒的传播和流行病学,以及病毒的进化研究是理解病毒遗传基础、追踪病毒来源和预防病毒爆发的有效方法[6]。②病毒遗传机制研究。主要关键词有replication、transcription、expression、RNA、nucleocapsid proteins、VP40、sequence、gene等。埃博拉病毒基因组为单股负链RNA,约长18.9 kb,能编码核衣壳蛋白及VP35、VP40、VP30、VP24、糖蛋白(glycoprotein,GP)和RNA聚合酶等7个结构蛋白,其中VP40与病毒成熟释放有关,RNA聚合酶在RNA转录成信使RNA和基因组复制中发挥重要作用[9]。③病毒病原学和进入细胞机制研究。主要关键词有glycoprotein、Niemann-Pick C1(NPC1)、identification、envelope glycoprotein、crystal-structure、entry、receptor、binding、in-vivo、membrane-fusion。介导病毒进入细胞和埃博拉病毒致病性的主要是由唯一的表面包膜蛋白GP决定的[10]。胆固醇转运蛋白NPC1也是埃博拉病毒感染宿主细胞的重要因素,其缺失突变或使用小分子抑制剂会使细胞对埃博拉病毒产生抗性[11]。④致病机理和宿主细胞免疫反应及疫苗开发。主要关键词有nonhuman-primates、vaccine、pathogenesis、guinea-pigs、antibodies、immune-responses、monkeys、mouse model、T-cell responses、vectors、attenuated recombinant vaccine、safety等。小鼠和猴子动物模型在本研究方面应用广泛[7]。目前尚无批准上市的埃博拉病毒病疫苗,处于研发中的疫苗主要分2类:非复制型和复制型。前者安全性较高,如灭活疫苗,但需较长时间诱导机体免疫,一般在暴露前使用以起到预防作用。后者包括减毒疫苗和复制型重组疫苗,如重组痘病毒载体疫苗、重组水泡性口炎病毒载体疫苗等,有一定安全隐患,一般在感染后使用,或用于处置疫情和应对生物恐怖袭击[9]。⑤治疗方法和药物开发。主要关键词有therapy、T-705 Favipiravir、antiviral、treatment、small-molecule inhibitors、convalescent plasma、ribavirin、ZMapp、drugs等。如抗病毒药物法匹拉韦(favipiravir,T-705)[12],2014年由日本富士胶卷控股公司和美国MediVector公司向美国FDA提交申请。BCX4430[13]属小分子腺苷类似物,能整合进病毒RNA使其空间构型改变,从而严重影响后续转录翻译过程。由美国马普生物制药公司生产的重组单克隆抗体合成药Zmapp实验结果表明可对感染埃博拉病毒后的猕猴达到100 %的治愈疗效[14]。⑥病毒检测。主要关键词有diagnosis、RT-PCR、PCR、rapid detection、blood、ELISA、quantification、IgG等。病毒的快速检测对预防和及早治疗具有重要意义,目前针对埃博拉病毒的实验室诊断方法主要有两类:抗原和抗体检测,主要采用ELISA法;检测病毒核酸,主要采用RT-PCR法[15]。(2)研究趋势:从关键词的平均年份分布情况可知,病毒复制、表达等遗传机制(②)和宿主细胞进入机制(③)是该领域早期的研究方向,但其中埃博拉病毒NPC1蛋白的研究仍然是近年来的研究热点。近3年研究热点主要集中在埃博拉病毒的快速监测(⑥)、传播和流行病学(①)、治疗方案和药物研发(⑤)方面。
3 讨 论新形势下国家总体安全观已突破传统领域,拓展至生物安全范畴,美国等已将生物安全上升到国家战略层面[16]。据我们前期的调研不难发现,美、法、英、日等国均已早早建立了生物安全Ⅳ级实验室(P4实验室)[17],为其开展包括埃博拉病毒在内的新发和烈性传染病原研究提供了有利的科研平台。2015年我国已建成首个P4实验室—中国科学院武汉国家生物安全实验室,也将为我国埃博拉病毒及新发和烈性传染病的研究开启新篇章。
我国虽未发生大规模埃博拉疫情,但埃博拉病毒是WHO定义的4级病毒,并存在被滥用为生物恐怖剂的危险;我国是最大的发展中国家,人口众多、公共卫生设施仍较落后,与世界各国来往日益频繁的国际环境下,应对埃博拉及其他新发和烈性传染病疫情的形势更加严峻。我国今后应在加强埃博拉病毒基础研究、加快治疗药物和疫苗研发、加强国际合作等方面进一步部署,加强烈性病原实验室的生物安全监管以及对社会公众的新发和烈性传染病科普教育和宣传[18 – 19]。
本研究以埃博拉病毒为契机,今后将逐步结合多方面科学数据和信息对埃博拉病毒及新发和烈性传染病进行系统研究,为我国总体国家安全战略、重大科技计划和社会经济发展提供政策支撑和理论依据,为建设运行首个P4实验室发挥参谋智库作用。
| [1] | 陈叶, 王萍, 刘芳炜, 等. 埃博拉出血热研究进展[J]. 中国公共卫生, 2017, 33(1): 170–172. |
| [2] | Gatherer D. The 2014 Ebola virus disease outbreak in West Africa[J]. Journal of General Virology, 2014, 95: 1619–1624. DOI:10.1099/vir.0.067199-0 |
| [3] | 唐浏英, 陈化新. 埃博拉病毒分子生物学和免疫学研究进展[J]. 中国公共卫生, 2001, 17(2): 92–94. DOI:10.3969/j.issn.1001-9561.2001.02.006 |
| [4] | Aylward B, Barboza P, Bawo L, et al. Ebola virus disease in West Africa – the first 9 months of the epidemic and forward projections[J]. New England Journal of Medicine, 2014, 371(16): 1481–1495. DOI:10.1056/NEJMoa1411100 |
| [5] | Feldmann H, Geisbert TW. Ebola haemorrhagic fever[J]. Lancet, 2011, 377(9768): 849–862. DOI:10.1016/S0140-6736(10)60667-8 |
| [6] | Baize S, Pannetier D, Oestereich L, et al. Emergence of Zaire Ebola virus disease in Guinea[J]. New England Journal of Medicine, 2014, 371(15): 1418–1425. DOI:10.1056/NEJMoa1404505 |
| [7] | Feldmann H, Jones SM, Daddariodicaprio KM, et al. Effective post-exposure treatment of Ebola infection[J]. PLoS Pathog, 2007, 3(1): e2. DOI:10.1371/journal.ppat.0030002 |
| [8] | Geisbert TW, Lee AC, Robbins M, et al. Postexposure protection of non-human primates against a lethal Ebola virus challenge with RNA interference: a proof-of-concept study[J]. Lancet, 2010, 375(9729): 1896–1905. DOI:10.1016/S0140-6736(10)60357-1 |
| [9] | 程颖, 刘军, 李昱, 等. 埃博拉病毒病:病原学、致病机制、治疗与疫苗研究进展[J]. 科学通报, 2014, 59(30): 2889–2899. |
| [10] | Chandran K, Sullivan NJ, Felbor U, et al. Endosomal proteolysis of the Ebola virus glycoprotein is necessary for infection[J]. Science, 2005, 308(5728): 1643–1645. DOI:10.1126/science.1110656 |
| [11] | Marceline C, John M, Tao R,et al. Small molecule inhibitors reveal Niemann-Pick C1 is essential for Ebola virus infection[J]. Nature, 2011, 477(7364): 344–348. DOI:10.1038/nature10380 |
| [12] | Sissoko D, Laouenan C, Folkesson E, et al. Experimental treatment with favipiravir for Ebola virus disease (the JIKI Trial): a historically controlled, single-arm proof-of-concept trial in Guinea[J]. PLoS Med, 2016, 13(3): e1001967. DOI:10.1371/journal.pmed.1001967 |
| [13] | Warren TK, Wells J, Panchal RG, et al. Protection against filovirus diseases by a novel broad-spectrum nucleoside analogue BCX4430[J]. Nature, 2014, 508(7496): 402–405. DOI:10.1038/nature13027 |
| [14] | Qiu X, Wong G, Audet J, et al. Reversion of advanced Ebola virus disease in nonhuman primates with ZMapp[J]. Nature, 2014, 514(7520): 47–53. DOI:10.1038/nature13777 |
| [15] | 李昱, 任翔, 刘翟, 等. 埃博拉病毒病:流行病学、生态学、诊断、治疗及控制[J]. 科技导报, 2014, 32(24): 15–24. DOI:10.3981/j.issn.1000-7857.2014.24.001 |
| [16] | 田德桥, 朱联辉, 黄培堂, 等. 美国生物防御战略计划分析[J]. 军事医学, 2012, 36(10): 772–776. |
| [17] | 章欣. 生物安全4级实验室建设关键问题及发展策略研究 [D]. 中国人民解放军军事医学科学院, 2016. |
| [18] | 林仲, 严延生, 曾超英. 实验室生物安全法制建设现状与展望[J]. 中国公共卫生, 2007, 23(4): 439–440. DOI:10.3321/j.issn:1001-0580.2007.04.071 |
| [19] | 任静朝, 张光辉, 段广才, 等. 基层医生及乡村居民对新发传染病信息需求调查[J]. 中国公共卫生, 2016, 32(2): 179–183. |
 2019, Vol. 35
2019, Vol. 35


