2. 广东省疾病预防控制中心;
3. 暨南大学病原生物学系
症候群监测作为传统疾病监测的补充,近年已成为备受关注传染病监测技术,而其中病原谱的检测有助于提高传染病监测的敏感性和特异性。发热伴出血症候群是以发热( ≥ 37.5℃,病程 ≤ 3周)并伴有以下2个或以上临床表现(皮肤出血点活紫癜、粘膜出血点、鼻衄、咯血、咳血、血便、贫血、血小板低于正常水平并持续减少、其他出血表现)的一系列疾病的总称[1]。临床上引起发热伴出血的疾病有:登革热(dengue fever)、肾综合征出血热(hemorrhagic fever with renal syndrome, HFRS)、新疆出血热、发热伴血小板减少综合症(severe fever with thrombocytopenia syndrome, SFTS)、鼠疫、流脑、人钩端螺旋体(leptospirosis,LS)病、猪链球菌病和恙虫病(Orientia tsutsugamushi, Ot)等,病原包括病毒和细菌2大类,病毒包括登革病毒(dengue virus, DENV)、汉坦病毒(Hantaan virus, HTNV)、新疆出血热病毒和新布尼亚病毒(new bunyavirus, NBYV)等,细菌包括鼠疫杆菌、脑膜炎奈瑟菌、LS、猪链球菌和立克次体等。近几十年来,广东省除了新疆出血热、发热伴血小板减少综合症和鼠疫未见报告外,其他病原体引起的疾病每年均有报道。为进一步了解广东省近年发热伴出血症候群病原体感染情况,掌握病原体流行特征和规律,同时也为基层医院临床诊断提供科学依据,本研究于2016年3 — 12月,对广东省内3个地市的哨点医院开展发热伴出血症候群病原谱的监测和调查。
1 材料和方法 1.1 监测点医院的设置和研究对象的选择选择广东省云浮、阳江和汕头3个地市中的6家二级及以上的医院作为哨点医院,将符合《发热伴出血症候群监测技术方案》(2012版)[1]中的发热伴出血症候群病例定义的所有住院病例作为研究对象。
1.2 标本采集和处理于2016年3 — 12月采集病例急性期全血标本5 mL,室温放置30 min,3 000 r/min离心10 min,吸取上层血清分装至2 mL螺旋口管,放– 20 ℃冰箱保存,4 ℃条件下定期运输至广东省疾病预防控制中心开展检测。
1.3 IgM/IgG抗体检测登革病毒抗体检测使用捕获酶联免疫吸附法(enzyme-linked immunosorbent assay, ELISA)(澳大利亚PanBiogo公司试剂盒);恙虫病东方体IgM和IgG抗体检测使用胶体金免疫层析法(韩国IMMUNEMed公司试剂盒);HFRS HTNV抗体检测使用间接ELISA(德国EUROIMMUN公司试剂盒);发热伴血小板减少综合症NBYV IgM/IgG抗体检测使用双抗体夹心ELISA(中国无锡鑫连鑫公司试剂盒);LS抗体检测使用双抗体夹心ELISA(中国上海泛柯公司试剂盒)。
1.4 登革病毒中和抗体检测BHK-21细胞和Ⅰ~Ⅳ型DENV均为为本室保存。将BHK-21细胞制备成4 × 105/mL的细胞悬液,铺24孔板,每孔加入500 μL,置于5 % CO2培养箱中37 ℃培养,待其长至80~90 %时使用。上述ELISA检测DENV抗体阳性样本血清56 ℃灭活30 min。取20 μL血清按1 : 10、1 : 20倍比稀释至1 : 320,向每个稀释孔分别加入100 μL的200 PFU(plaque forming unit,空斑形成单位)/mL的Ⅰ、Ⅱ、Ⅲ和Ⅳ型DENV标准株混匀,同时设立2孔阳性对照,37 ℃中和作用1 h。弃去24孔板细胞培养液,每孔依次加入200 μL的中和液,放置37 ℃、5 % CO2培养箱中吸附2 h后,每孔加入1 mL 2.0 %的羧甲基纤维素(美国SIGMA公司)。培养4 d后进行固定、染色,观察空斑形成状态并计数。中和空斑的数量达50 %以上的血清稀释度作为中和抗体的效价。
1.5 LS 显微镜凝集试验将我国LS 15群15型代表株接种于Korthof或EMJH等适宜培养基中,28 ℃培养5 ~7 d备用。上述检测抗体阳性血清56 ℃灭活30 min,用生理盐水1︰400稀释。反应板每孔加入50 μL稀释血清,再分别加入50 μL 15个代表株培养液。摇匀后37 ℃孵育1 h。用接种环挑取反应液及对照,放置载物玻片上暗视野显微镜下观察凝集情况。当出现++凝集(即视野中50 % LS被凝集)时判断为LS抗体阳性。
1.6 恙虫病东方体DNA提取及核酸检测(表1)DNA核酸提取使用试剂盒(德国QIAGEN公司),操作简述如下:向100 μL血清中加入20 μL蛋白酶K,用磷酸缓冲液(phosphate-buffered saline, PBS)调制220 μL,加入200 μL AE缓冲液56 ℃孵育10 min,加入200 μL无水乙醇沉淀核酸,然后上柱结合,用AW1和AW2分别清洗硅胶柱,最后用200 μL AE洗脱DNA,– 20 ℃保存备用。恙虫病东方体56 kDa抗原基因部分序列用巣式PCR进行扩增,试剂盒(德国QIAGEN公司)。第1轮PCR反应体系为:HotStarTaq Master Mix 12.5 μL,DNA模板10 μL,上游引物JG-OtF584(10 pmol/L)1μL,下游引物RTS9(10 pmol/L)1 μL补充水至25 μL;反应条件为:94 ℃ 15 min,接下来94 ℃ 解链1 min,50 ℃退火 1 min,72 ℃延伸1 min,共35个循环,最后72 ℃延伸5 min。第2轮PCR反应体系为:HotStarTaq Master Mix 12.5 μL,第1轮PCR产物1 μL,上游引物F(10 pmol/L,下游引物RTS8(10 pmol/L)L补充水至25 μL,反应条件同前。PCR产物1 %琼脂糖凝胶电泳,紫外灯下观察结果,扩增条带大小与目的片段大小一致割胶测序。
| 表 1 恙虫病东方体巢式PCR引物 |
1.7 恙虫病东方体分子分析和系统进化分析
使用Mega 6.0软件的邻位相连法(neighbor-joining, NJ)中maximum composite likelihood模型构建系统进化树。
2 结 果 2.1 标本采集2016年共采集282份临床样本,其中阳江130份,云浮106份,汕头46份。男性129例,女性153例,男女性别比1 : 1.2,所有标本采集时间主要在3 — 12月,1 — 2月无标本。
2.2 IgM/IgG抗体检测(表2)登革热共检测标本282份,检测DENV IgM/IgG抗体阳性13份,其中IgM阳性11份,IgM和IgG均阳性2份,阳性率4.61 %;恙虫病东方体共检测标本282份,检测恙虫病东方体IgM/IgG抗体阳性70份,其中IgM阳性33份,IgG阳性1份,IgM和IgG均阳性36份,阳性率24.84 %;肾综合症出血热共检测标本282份,检测HTNV IgM/IgG抗体阳性10份,其中IgM阳性3份,IgG阳性6份,IgM和IgG均阳性1份,阳性率3.55 %;发热伴血小板减少综合症共检测标本254份,检测NBYV仅IgG抗体阳性1份,阳性率0.39 %;钩端螺旋体病检测标本199份,LS抗体阳性65份,其中IgM阳性33份,IgG阳性25份,IgM和IgG均阳性7份,阳性率32.66 %。
| 表 2 广东省2016年发热伴出血症候群相关病IgM/IgG抗体检测 |
2.3 DENV中和抗体检测
为进一步明确DENV抗体的真实性,对ELISA检测阳性的13份标本分别用DENV I~IV进行中和实验,结果显示共有6份标本中和抗体阳性,其中5份血清对Ⅱ型DENV具有中和效果,中和效价在1 : 10~1 : 20之间;1份血清对4型别的DENV均有中和作用,中和效价均为1 : 20。
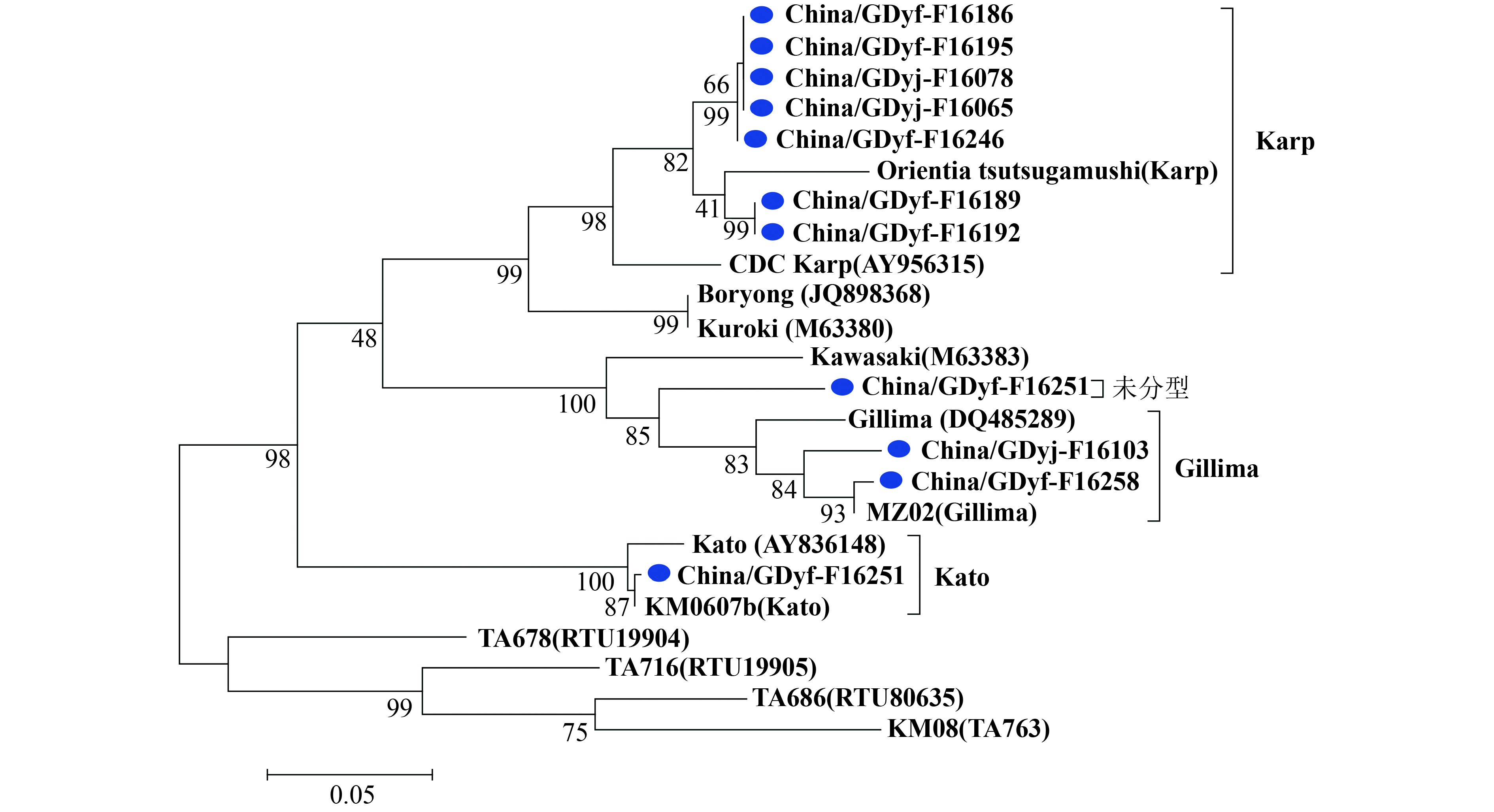
2.4 恙虫病东方体核酸检测(图1)在282份标本中,对其中49份临床诊断疑似恙虫病和70份IgM/IgG抗体阳性的病例共119份样本进行核酸检测,结果11份核酸阳性,阳性率9.24 %(11/119)。将核酸阳性样本进行测序,获得的序列与来自GenBank中10个基因型的13个代表株的序列进行分子分型和进化分析(图1)。分子分型结果显示:11株序列属于4个不同的基因型,其中云浮5株(F16186,F16195,F16246,16189,16192)和阳江2株(F16065,16078)同属Karp基因型,云浮F16258株和阳江F16103株同属Gillima基因型,云浮F16191株属于Kato基因型,云浮F16251株位于Kato和Gillima之间,由于较低的Bootstrap值而不能进行有效分型。分子进化结果显示:11株序列5个不同的进化分支中,其中同属Karp基因型7株序列分别位于2个不同的进化簇中,其它4株序列位于3个不同的进化簇中。
|
图 1 恙虫病东方体56 kDa抗原基因系统进化树 |
2.5 LS显微镜凝集试验
对以上4种病原所有检测项目均为阴性的血清样本进行LS抗体筛查,共检测标本199份,发现65份阳性标本,其中IgM阳性33份,IgG阳性25份,IgM和IgG均阳性7份。随后通过血清凝集实验对上述LS抗体阳性样本进行复核,结果6份阳性样本。
3 讨 论引起发热伴出血症候群的病原体有很多,本次研究由于受到经费的限制,根据广东省疫情历年监测情况,本研究重点选择以下5种病原体,包括登革病毒、汉坦病毒、钩端螺旋体、新布尼亚病毒和恙虫病东方体进行检测,这5种病原体均可引起血小板减少,甚至出血,部分临床症状相近或相似,在临床诊断中需要进行鉴别诊断和实验室的确诊。钩端螺旋体和恙虫病东方体感染率较高,分别为32.66 %和24.82 %;登革病毒和汉坦病毒感染率相对较低,分别为4.61 %和3.55 %;新布尼亚病毒感染率为0.39 %。辽宁的监测显示汉坦病毒感染率为45.9 %,新布尼亚病毒感染率为31.5 %[2]。目前发热伴血小板减少综合症在广东尚未发现本地病例,在本次研究中也对其病原体新布尼亚病毒进行了筛查,目的是评估广东人群中存在新布尼亚病毒感染的风险。本次筛查仅发现1例新布尼亚病毒IgG抗体阳性,而IgM抗体阴性,推测可能为既往感染或交叉反应,需要进一步扩大范围和增加样本量筛查,结合广东省疫情监测情况评估,广东省由新布尼亚病毒感染导致发热伴血小板综合症病例的风险较低。目前,国内由NBYV引起的发热伴血小板减少综合症病例主要发生在湖北、江苏、安徽、辽宁等中部北部地区,目前广东省主要为输入病例[3–4]。研究显示,蜱虫是NBYV的传播媒介[5],当患者病毒血液中病毒载荷很高时,可以通过密切接触、血液等引起人传人[6]。
汕头DENV抗体阳性率明显高于阳江和云浮,与广东省历年登革热疫情相符。DENV蚀斑减少中和实验和LS显微镜凝集实验可以对其抗体进行确认,可信度高。在此次研究中,为了排除ELISA检测中出现的假阳性,根据上述2种疾病的诊断标准[7–8]进行了复核。经检测登革热和人钩端螺旋体病分别有6份标本中和抗体阳性或凝集实验阳性。其中1例DENV抗体对Ⅰ、Ⅱ、Ⅲ、Ⅳ型病毒均有中和作用,可能由于采样时间正处于病毒感染早期,体内抗体水平较高[9],中和实验时存在交叉反应。世界卫生组织规定的登革热确诊标准包括:发热、皮疹等基本登革热症状;出血体征;血小板降低( ≤ 100 × 109 /L);病毒分离和血清学检测阳性;恢复期的血细胞比容较治疗前下降至少20 %[10]。由于很多患者并未出现典型的临床体征,所以可靠的实验室检测仍然十分重要[11]。
恙虫病东方体是一种古老的病原体,在我国已经存在很久,1952年中国大陆首次在广东报道[12 – 13]。本次发病伴出血症状监测的病例恙虫病东方体阳性率达24.82 %,与广东省的疫情是相符的,即使未按照法定传染病报告,全省医疗机构每年报告的恙虫病病例数达1 000例左右,并呈现逐年增加的趋势[14]。目前恙虫病东方体的基因分型多以56 kD表面蛋白基因作为目的基因,全球由此获得基因型有20多种,主要包括Karp、Kato、Gilliam、TA763、TA678、TA716、Kawasaki、Kuroki、Shimokoshi等。据现有文献报道,我国福建、广东地区以Karp型为主,江苏北部、山东地区以Kawasaki型为主[15 – 17]。本次研究共发现4个基因型,主要是Karp,其次是Gillima和Kato, 有一株与Kawasaki具有较高的同源性[18],但由于Boostrap值较低,本次研究未将其进行分型,提示广东省恙虫东方体存在多种基因型并呈散发状态。恙虫病传播的主要媒介为恙螨[19]。作为典型临床症状的焦痂溃疡等可以辅助诊断[20]。
本次研究对广东省出现的发热伴出血症候群病例对主要的传染病的病原体进行了抗体和核酸的检测,对这些病原体在广东的感染状况进行了初步的了解,为临床的诊断提供了实验依据[21]。由于各地医务人员在标本的采集,诊断标准的把握,以及检验过程中试剂和方法的选择上都存在一定的不足,可能给本次研究带来不利影响。本次研究仅选择3个地市医院,分布在广东省的东西北部,对于有21个地市的广东省来说,代表性略显不够,在以后的研究中值得注意和改进。
| [1] | 中华人民共和国卫生部. 发热伴出血症候群监测方案[R]. 中华人民共和国卫生部, 2012. |
| [2] | 张洁, 王子江, 李鑫, 等. 辽宁省2012 — 2013年发热伴出血症候群监测分析[J]. 中国公共卫生, 2014, 30(6): 822–824. DOI:10.11847/zgggws2014-30-06-45 |
| [3] | 吕沐天, 孙颖, 刘沛, 等. 发热伴血小板减少综合征布尼亚病毒研究进展[J]. 微生物学杂志, 2013, 33(2): 86–88. |
| [4] | 李德新. 发热伴血小板减少综合征布尼亚病毒概述[J]. 中华实验和临床病毒学杂志, 2011, 25(2): 81–84. |
| [5] | Yu XJ, Liang MF, Zhang SY, et al. Fever with thrombocytopenia associated with a novel bunyavirus in China[J]. New England Journal of Medicine, 2011, 364(16): 1523–1528. DOI:10.1056/NEJMoa1010095 |
| [6] | Gai ZT, Liang MF, Zhang SY, et al. Person-to-person transmission of severe fever with thrombocytopenia syndrome bunyavirus through blood contact[J]. Clinical Infectious Diseases An Official Publication of the Infectious Diseases Society of America, 2012, 54(2): 249–253. DOI:10.1093/cid/cir776 |
| [7] | 中华人民共和国卫生部. 登革热诊断标准(WS 216-2008)[S]. 中华人民共和国卫生部, 2008. |
| [8] | 中华人民共和国卫生部. 钩端螺旋体诊断标准(WS 290-2008)[S]. 中华人民共和国卫生部, 2008. |
| [9] | 赵彩彦, 甄真, 周俊英, 等. 感染性疾病首诊手册[M]. 人民军医出版社, 2010. |
| [10] | World Health Organization. Global strategy for dengue prevention and control, 2012 – 2020[Z]. Geneva: World Health Organization, 2012. |
| [11] | 叶子, 黄应雄, 蒋鹏, 等. 2014年广州地区158例登革热住院患者临床特征分析[J]. 中华危重病急救医学, 2015, 27(4): 300–305. |
| [12] | 李珉珉, 王珊珊, 李健, 等. 广东省重要岛屿恙虫病东方体血清流行病学调查[J]. 中国病原生物学杂志, 2008, 3(10): 743–744. |
| [13] | Kelly DJ, Richards AL, Temenak J, et al. The past and present threat of rickettsial diseases to military medicine and international public health[J]. Clin Infect Dis, 2002, 34(Suppl 4): S145–S169. |
| [14] | 彭志强, 钟豪杰, 梁文佳. 广东省2006—2011年恙虫病流行病学分析[J]. 华南预防医学, 2013, 39(1): 57–58. |
| [15] | 郭恒彬. 我国恙虫病立克次体(恙虫病东方体)分型研究近况[J]. 中国人兽共患病杂志, 2000, 16(3): 79–80. |
| [16] | 肖寒, 方倩. 珠海市恙虫病东方体基因型研究[J]. 中国人兽共患病学报, 2015, 31(2): 139–142. |
| [17] | 张云, 吴光华, 邓小昭, 等. 东南沿海地区地理景观与恙虫病流行特征关系[J]. 中国公共卫生, 2010, 26(2): 174–175. DOI:10.11847/zgggws2010-26-02-26 |
| [18] | 周海燕, 何凤屏, 罗君, 等. 粤北山区域恙虫病自然疫源地的研究[J]. 分子诊断与治疗杂志, 2011, 3(6): 398–401. |
| [19] | 张萌, 王显军, 赵仲堂. 中国恙虫病流行态势及预防控制[J]. 中华流行病学杂志, 2011, 32(4): 419–423. |
| [20] | 王跃兵, 杨向东, 杨发莲, 等. 不明原因发热病人钩端螺旋体和巴尔通体感染调查[J]. 实用预防医学, 2015, 22(4): 430–432. |
| [21] | 林玫, 梁大斌, 董柏青, 等. 症候群监测系统构建及效果评价[J]. 中国公共卫生, 2014, 30(1): 43–46. DOI:10.11847/zgggws2014-30-01-13 |
 2018, Vol. 34
2018, Vol. 34


