2. 沈阳医学院2014级临床本科;
3. 沈阳医学院2013级临床本科;
4. 沈阳医学院2015级临床本科
慢性乙醇中毒已是全球性社会问题,可引起多种疾病,其中以乙醇性脑病较多见[1]。乙醇具有脂溶性和亲神经性,可迅速通过血脑屏障和神经细胞膜。海马是学习记忆的关键脑区,是调控学习记忆功能的结构基础。研究表明:乙醇引起的脑功能损害在海马中较为显著[2],乙醇可抑制海马神经元的成熟分化,导致学习记忆功能失调[3]。Phosphatidylinositol-3-kinase/protein kinase B/mammalian target of rapamycin (PI3K/Akt/mTOR) 信号通路在长时记忆的形成中具有重要作用[4]。在雄性小鼠的伏隔核中,AKT的激活参与了乙醇引起的学习记忆的下降[5]。一些治疗乙醇中毒药物[如metabotropic glutamate receptorsm(GluR5)拮抗剂],对成年雄性小鼠具有一定作用,但对于成年雌性小鼠作用却不明显[6]。由此推测:小鼠海马PI3K/Akt/mTOR信号通路可能参与乙醇对小鼠学习记忆的影响,且存在性别差异。本研究拟采用Morris水迷宫对雌雄小鼠慢性乙醇摄入引起的认知功能改变进行评价,并通过Western blot法检测雌雄小鼠海马结构PI3K/Akt/mTOR信号通路相关蛋白的表达差异,为揭示慢性乙醇中毒影响认知功能提供新的分子机制。
1 材料与方法 1.1 实验动物及分组雌、雄8w龄昆明种小鼠(辽宁长生生物技术有限公司)120只,体质量(30 ± 3)g,清洁级,自由摄食、饮水。经1 w适应期饲养,将雌、雄小鼠随机各分成4组(对照组及低、中、高剂量乙醇组),每组15只。低、中、高剂量组乙醇浓度分别为12.5 %、25 %、50 %,对照组为等量蒸馏水。每天于早8点对小鼠进行灌胃给药(0.1 mL/10 g),连续9 w。
1.2 主要试剂及仪器乙醇(分析纯,≥ 99.7 %,北京化工厂),根据实验所需浓度每天灌胃给药前临时配制;sodium dodecylsulphate-polyacrylamide gel electrophoresis(SDS-PAGE)试剂盒、bicinchoninic acid(BCA)蛋白提取试剂盒及BCA蛋白浓度测定试剂盒(KeyGEN BioTECH);抗p-mTOR(ser2448)单克隆抗体(Immunoway);抗p-Akt(ser473)单克隆抗体(Abcam);β-actin单克隆抗体、羊抗兔IgG-HRP(KeyGEN BioTECH);HRP化学发光底物液(Thermo)。Morris水迷宫(成都泰盟科技有限公司);低温超速离心机(德国Heraeus Sepatech公司);ELx800酶标仪(美国BioTek公司);Heros-MoleTL2020高通量组织研磨仪(北京鼎号源科技有限公司);Bio-Rad电泳仪、转膜仪(美国Bio-Rad公司);MF-ChemiBIS2.0凝胶成像系统(以色列DNR公司);M200 PRO多功能酶标仪(瑞士Tecan公司)。
1.3 方法 1.3.1 Morris水迷宫小鼠行为学检测乙醇给药后第63 d,使用Morris水迷宫跟踪分析系统对各组小鼠进行定位航行及空间探索实验,检测其学习和记忆能力。(1)定位航行实验(反映空间记忆的获得能力):于实验第63 d,停止给药。对各组小鼠进行水迷宫训练5 d,每天训练2次(上午10点,下午15点),每次60 s。将小鼠面朝池壁放入水中,同时启动记录装置,通过该系统的图像分析软件可获得小鼠在水中的逃避潜伏期。小鼠找到并爬上平台停留5 s以上定义为有效,若小鼠入水后60 s内未能找到并爬上平台,则将其引导至平台上停留10 s,此时逃避潜伏期记录为60 s。每次训练完成后,迅速将小鼠擦干,防止低体温。每天各小鼠逃避潜伏期用2次训练的均值表示。(2)空间探索实验(检测空间记忆的保持能力):实验第6 d撤去平台,将小鼠从固定象限中点面朝池壁放入水中,记录其60 s池内活动情况,通过该系统的图像分析软件获得小鼠在有效区的停留距离。
1.3.2 取材完成空间探索实验后立即断头处死小鼠,冰上分离左侧海马,置于 – 80 ℃保存。
1.3.3 Western blot检测各组小鼠海马结构p-Akt、p-mTOR蛋白相对表达取小鼠海马组织,加入组织裂解液150 μL匀浆,12 000 r/min离心5 min,取上清液,采取BCA法测定蛋白浓度(按照试剂盒说明操作)。取20 μg样品于6 %的分离胶中进行SDS-PAGE电泳分离(上层为5 %浓缩胶),170 mA湿转140 min,转膜后将polyvinylidene fluoride(PVDF)膜置于5 %脱脂奶粉中室温振荡封闭1 h,Tris-buffered saline/Tween(TBST)漂洗3次,每次10 min,按实验要求分别加入抗p-Akt单克隆抗体(1 : 2 000)、抗p-mTOR单克隆抗体(1 : 2 000)4 ℃孵育过夜,TBST漂洗4次,每次10 min,再与辣根过氧化酶标记的山羊抗兔IgG(1 : 5 000)室温振荡孵育1 h,TBST漂洗3次,每次10 min,将horseradish peroxidase(HRP)化学发光底物液覆盖在PVDF膜上,室温孵育5 min,放置于凝胶成像系统摄片,并用Image J软件进行蛋白印迹条带灰度的定量分析。每个样品测定3次,求得平均吸光度值进行统计分析。将使用抗β-actin单克隆抗体(1 : 1 500)获得的β-actin蛋白印迹条带作为加样内参。
1.4 统计分析采用GraphPad Prism 5软件进行统计分析,数据以
Morris水迷宫定位航行实验结果表明:各组雌鼠第5 d逃避潜伏期均值较本组第1 d均值明显缩短(P < 0.05)。空间探索实验结果表明:50 %乙醇组与对照组相比有效区停留距离明显减短,差异有统计学意义( P < 0.05)。
|
表 1 各组雌鼠Morris水迷宫学习记忆行为学检测结果(
|
2.1.2 不同浓度乙醇对雄鼠学习记忆的影响(表2)
Morris水迷宫定位航行实验结果表明:各组雄鼠第5 d逃避潜伏期均值较本组第1 d均值明显缩短(P < 0.05)。空间探索实验结果表明:25 %乙醇组、50 %乙醇组与对照组相比有效区停留距离明显减短,差异有统计学意义( P < 0.05)。
|
表 2 各组雄鼠Morris水迷宫学习记忆行为学检测(
|
2.1.3 不同乙醇对雄雌小鼠空间记忆影响的差异比较(图1)
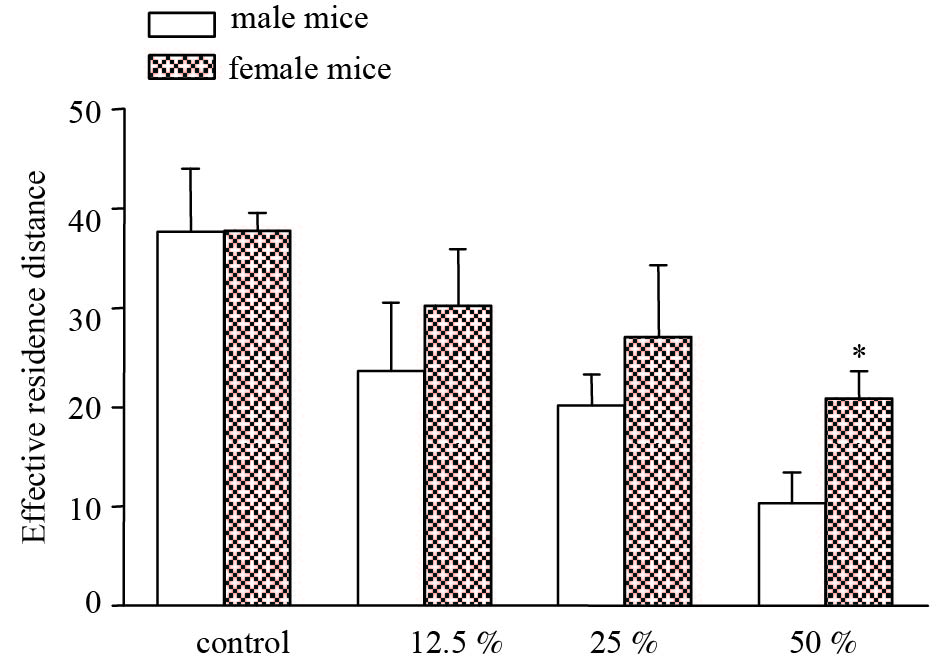
Morris水迷宫空间探索结果表明:与相同给药浓度的雄鼠比较,12.5 %乙醇组、25 %乙醇组雌鼠的有效区停留距离稍增加,但差异无统计学意义。50 %乙醇组雌鼠的有效区停留距离明显增加,差异有统计学意义(P < 0.05)。
|
注:50 %乙醇组雌雄鼠比较,*P < 0.05 图 1 雌雄小鼠有效区停留距离比较 |
2.2 Western blot方法检测mTOR信号通路中相关蛋白的表达 2.2.1 不同浓度乙醇对雌雄鼠海马结构p-Akt蛋白表达的影响(图2)
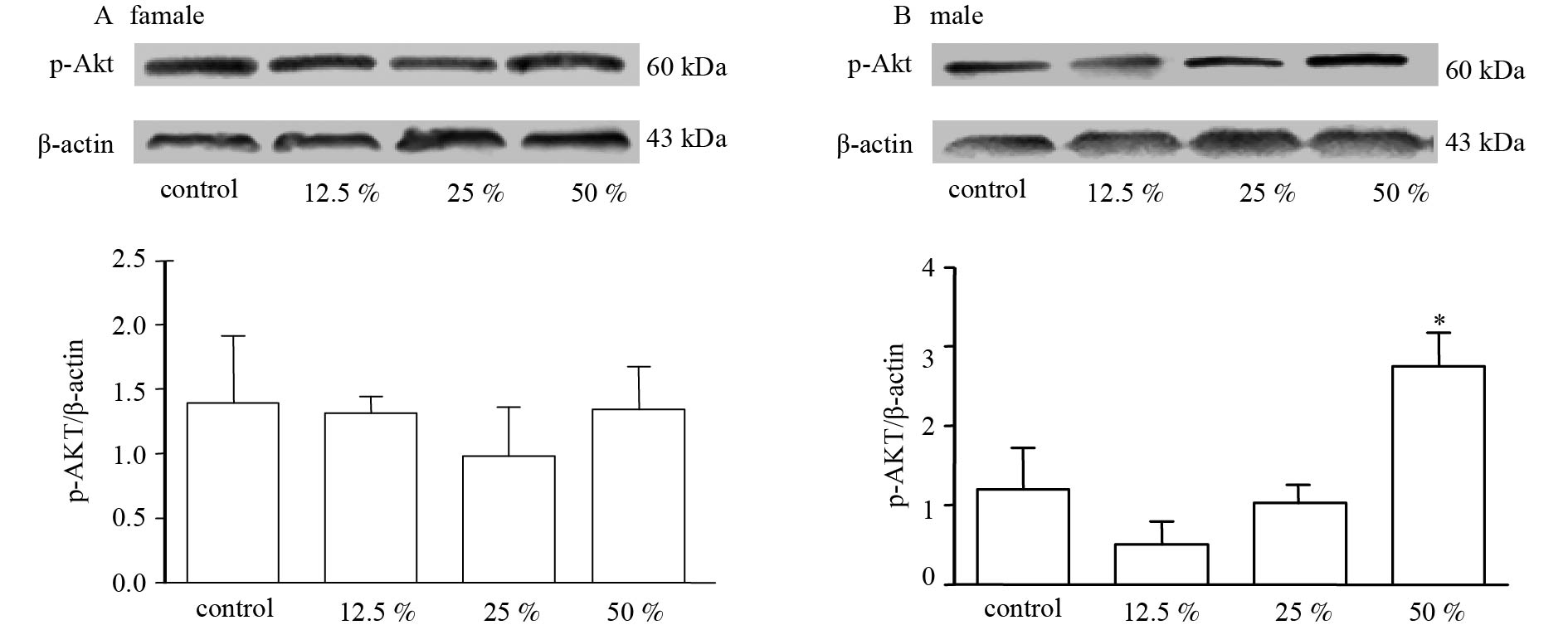
对慢性乙醇染毒的雄雌小鼠进行海马p-Akt蛋白检测:对照组与各乙醇染毒组小鼠均显示出特异性的p-Akt蛋白条带,分子量均为60 kDa。将各组目的蛋白条带与对应的 β-actin条带进行灰度对比分析,计算出p-Akt蛋白的相对表达量。与对照组相比,12.5 %及25 %乙醇组雌鼠p-Akt蛋白表达稍有降低,50 %乙醇组雌鼠p-Akt蛋白表达稍有增加,差异均无统计学意义(图2A)。与对照组相比,50 %乙醇组雄鼠p-Akt蛋白表达明显升高,差异有统计学意义(P < 0.05)。
|
注:50 %乙醇组雄鼠与其对照组相比,*P < 0.05 图 2 雌雄小鼠海马结构内p-Akt蛋白表达的差异 |
2.2.2 不同浓度乙醇对雌雄鼠海马结构p-mTOR蛋白表达的影响(图3)
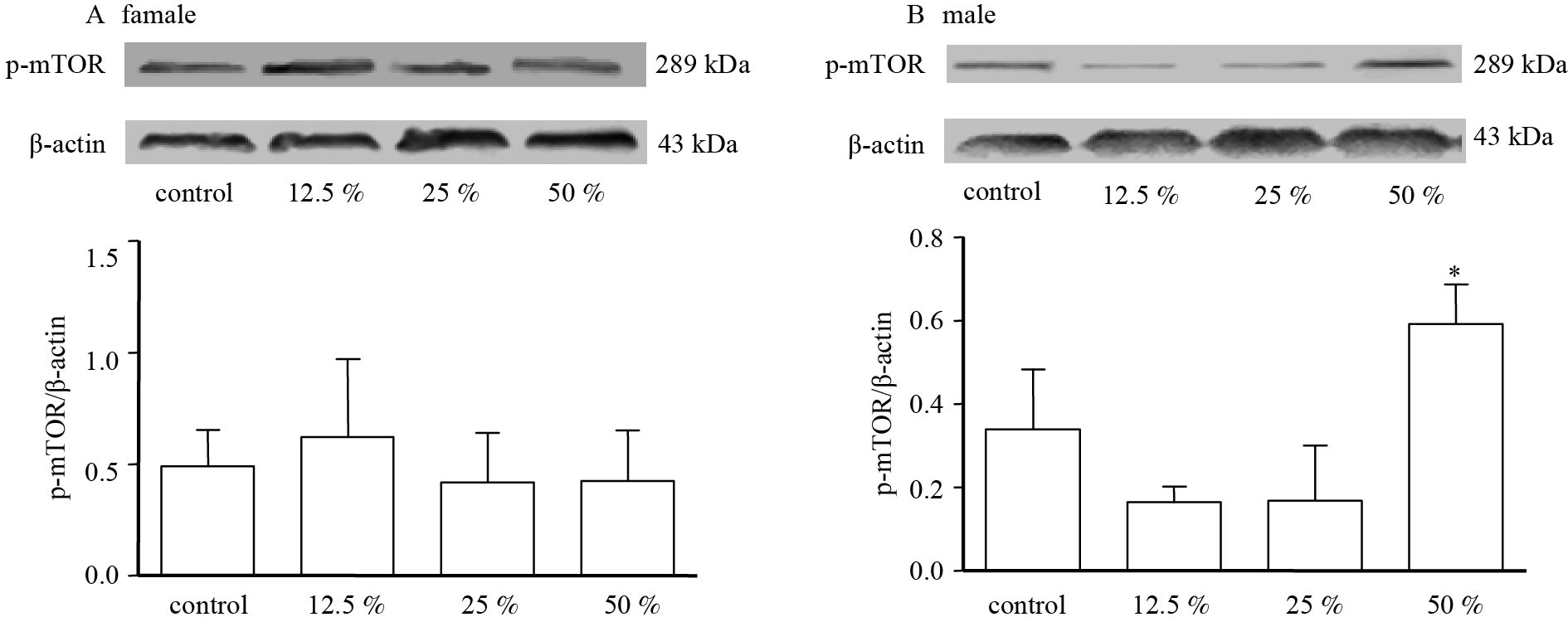
对慢性乙醇染毒的雄雌小鼠进行海马p-mTOR蛋白检测:对照组与各乙醇染毒组小鼠均显示出特异性的p-mTOR蛋白条带,分子量为289 KD。将各组目的蛋白条带与对应的 β-actin条带进行灰度对比分析,计算出p-mTOR蛋白的相对表达量。与对照组相比,12.5 %乙醇组雌鼠p-mTOR蛋白表达稍有增加,25 %及50 %乙醇组雌鼠p-mTOR蛋白表达稍有降低,差异均无统计学意义。与对照组相比,12.5 %及25 %乙醇组雄鼠p-mTOR蛋白表达稍有降低,但差异无统计学意义;50 %乙醇组雄鼠p-mTOR蛋白表达明显增加,差异有统计学意义(P < 0.05)。
|
注:50 %乙醇组雄鼠与其对照组相比,*P < 0.05 图 3 雌雄小鼠海马结构内p-mTOR蛋白表达的差异 |
3 讨 论
哺乳动物雷帕霉素靶蛋白(mTOR)属磷脂酰肌醇3激酶(PI3K)蛋白家族成员,在PI3K-Akt-mTOR信号通路中,mTOR是一种参与翻译调控和突触可塑性的蛋白激酶,在合成蛋白质翻译的起始阶段起到了重要作用。激活的Akt直接作用于mTOR,调控细胞生长与增殖,而Ser473位点的磷酸化是Akt激活的必要条件。海马结构是参与学习记忆的重要脑区,海马功能的不对称性是有关记忆形成和记忆维持的重要因素[7]。Samara[8]等对大鼠海马进行的蛋白组学研究发现:某些蛋白在左侧海马表达较右侧为多,且左侧海马神经保护作用较强。此外,在记忆痕迹的形成和信息传递方面,左侧海马占有优势[9]。研究表明:mTOR信号通路参与生长素诱导的海马神经干细胞的增殖,从而影响学习记忆[10]。在成年雄鼠,过度活化的mTOR可破坏神经元的形态,使树突棘的密度减少,损害空间记忆功能[11]。
本研究通过Morris水迷宫实验发现:各浓度组雌雄小鼠第5d逃避潜伏期较第1天明显缩短;与对照组相比,25 %乙醇组雄鼠及50 %乙醇组雌雄小鼠有效区停留距离明显减少。这表明:各组小鼠虽然都具有一定的学习能力,但25 %乙醇慢性染毒对雄鼠的空间记忆能力有损伤,50 %乙醇慢性染毒对雄雌鼠空间记忆能力均有损伤。通过Western blot方法进一步研究发现:50 %乙醇组雄鼠海马结构内p-Akt,p-mTOR蛋白表达均较对照组明显升高,而雌鼠无显著性差异。这表明:50 %乙醇慢性染毒对雄鼠学习记忆的影响可能与海马内mTOR通路蛋白表达的变化有关。Liu[12]等对大鼠神经元PC12细胞进行乙醇染毒发现:乙醇染毒组的细胞活性降低与p-Akt水平升高相关。此外,对小鼠NG108-15细胞进行乙醇染毒研究发现:乙醇可增加此细胞p-AKT蛋白的表达水平,并诱导mTOR信号通路的激活[13]。慢性乙醇暴露导致脑内mTOR通路磷酸化水平上调,可能引起自噬溶酶体系统受到抑制[14],而抑制自噬可加重乙醇诱导的神经元损伤[15]。
不同摄入乙醇方式及不同乙醇浓度对机体造成的影响具有性别差异[16 – 17]。小鼠自由饮用乙醇的条件下,雌鼠饮用乙醇后的运动活性及对乙醇的耐受力较雄鼠强[18]。Cozzoli等发现[19]:在慢性乙醇中毒的小鼠中,mTOR抑制剂能通过mTOR信号通路使雄鼠的伏隔核内的乙醇浓度降低,但对雌鼠无作用。本研究发现:50 %乙醇组雌鼠比同浓度组雄鼠有效区停留距离长;50 %乙醇组雄鼠海马结构内p-Akt,p-mTOR蛋白表达的变化与雌鼠不同。提示慢性乙醇中毒引起雌雄小鼠学习记忆下降的程度不同,且海马内mTOR信号通路相关蛋白的变化存在性别差异。
综上所述,慢性乙醇中毒对学习记忆的影响存在性别差异,mTOR信号通路可能参与此过程。学习记忆相关机制复杂,至于何种因素通过何种途径导致雌鼠海马内mTOR信号通路相应蛋白变化不明显,有待于进一步研究。
| [1] | de la Monte SM, Kril JJ. Human alcohol-related neuropathology[J]. Acta Neuropathol, 2014, 127(1): 71–90. DOI:10.1007/s00401-013-1233-3 |
| [2] | Rossimó C, Moscosocastro M, Ruizmedina J, et al. Memory impairment and hippocampus specific protein oxidation induced by ethanol intake and 3,4-methylenedioxymethamphetamine (MDMA) in mice[J]. J Neurochem, 2013, 125(5): 736–746. DOI:10.1111/jnc.12247 |
| [3] | Chung HY, Chang CT, Young HW, et al. Ethanol inhibits retinal and CNS differentiation due to failure of cell cycle exit via an apoptosis-independent pathway[J]. Neurotoxicol Teratol, 2013, 38: 92–103. DOI:10.1016/j.ntt.2013.05.006 |
| [4] | 随力, 任杰. mTOR在记忆功能中的作用[J]. 中国药理学通报, 2011, 27(6): 748–751. |
| [5] | Neasta J, Hamida SB, Yowell QV, et al. AKT signaling pathway in the nucleus accumbens mediates excessive alcohol drinking behaviors[J]. Biol Psychiatry, 2011, 70(6): 575–582. DOI:10.1016/j.biopsych.2011.03.019 |
| [6] | Cozzoli DK, Strong-Kaufman MN, Tanchuck MA, et al. The effect of mGluR5 antagonism during binge drinking on subsequent ethanol intake in C57BL/6J mice: sex- and age-induced differences[J]. Alcohol Clin Exp Res, 2014, 38(3): 730–738. DOI:10.1111/acer.2014.38.issue-3 |
| [7] | Kessels RP, de Haan EH, Kappelle LJ, et al. Varieties of human spatial memory: a meta-analysis on the effects of hippocampal lesions[J]. Brain Res Rev, 2001, 35(3): 295–303. DOI:10.1016/S0165-0173(01)00058-3 |
| [8] | Samara A, Vougas K, Papadopoulou A, et al. Proteomics reveal rat hippocampal lateral asymmetry[J]. Hippocampus, 2011, 21(1): 108–119. DOI:10.1002/hipo.v21.1 |
| [9] | Klur S, Muller C, Pereira dVA, et al. Hippocampal-dependent spatial memory functions might be lateralized in rats: an approach combining gene expression profiling and reversible inactivation[J]. Hippocampus, 2009, 19(9): 800–816. DOI:10.1002/hipo.v19:9 |
| [10] | Kim C, Kim S, Park S. Neurogenic effects of ghrelin on the hippocampus[J]. Int J Mol Sci, 2017, 18(3): 588. DOI:10.3390/ijms18030588 |
| [11] | Bockaert J, Marin P. mTOR in brain physiology and pathologies[J]. Physiol Rev, 2015, 95(4): 1157–1187. DOI:10.1152/physrev.00038.2014 |
| [12] | Liu L, Sun T, Feng X, et al. Nerve growth factor protects against alcohol-induced neurotoxicity in PC12 cells via PI3K/Akt/mTOR pathway[J]. Alcohol Alcohol, 2017, 52(1): 12–18. DOI:10.1093/alcalc/agw077 |
| [13] | Fu X, Guo Z, Gao C, et al. Long-term alcohol-induced activation of mammalian target of rapamycin is a key risk factor of epilepsy[J]. Med Sci Monit, 2016, 22: 3975–3980. DOI:10.12659/MSM.897018 |
| [14] | 张硕, 冯娟. 自噬在乙醇介导神经毒性中的保护作用及机制[J]. 临床与病理杂志, 2015, 35(5): 854–864. DOI:10.3978/j.issn.2095-6959.2015.05.032 |
| [15] | Luo J. Autophagy and ethanol neurotoxicity[J]. Autophagy, 2014, 10(12): 2099–2108. DOI:10.4161/15548627.2014.981916 |
| [16] | Fontaine CJ, Patten AR, Sickmann HM, et al. Effects of pre-natal alcohol exposure on hippocampal synaptic plasticity: sex, age and methodological considerations[J]. Neurosci Biobehav Rev, 2016, 64: 12–34. DOI:10.1016/j.neubiorev.2016.02.014 |
| [17] | Koss WA, Frick KM. Sex differences in hippocampal function[J]. J Neurosci Res, 2017, 95(1-2): 539–562. DOI:10.1002/jnr.23864 |
| [18] | Gallego X, Cox RJ, Funk E, et al. Voluntary exercise decreases ethanol preference and consumption in C57BL/6 adolescent mice: sex differences and hippocampal BDNF expression[J]. Physiol Behav, 2015, 138: 28–36. DOI:10.1016/j.physbeh.2014.10.008 |
| [19] | Cozzoli DK, Kaufman MN, Nipper MA, et al. Functional regulation of PI3K-associated signaling in the accumbens by binge alcohol drinking in male but not female mice[J]. Neuropharmacology, 2016, 105: 164–174. DOI:10.1016/j.neuropharm.2016.01.010 |
 2018, Vol. 34
2018, Vol. 34


