H7N9禽流感病毒是能感染禽类的亚型甲型病毒之一[1]。血凝素(hemagglutinin,HA)蛋白主要功能是与宿主细胞表面特异性受体结合,介导病毒进入胞浆,刺激机体产生中和性抗体[2]。HA蛋白能否裂解关系到该病毒的致病力,对蛋白酶裂解的敏感性直接影响到病毒的毒力。低致病性毒株裂解位点处有1个或2个碱性氨基酸,一般只引起局部感染。中国台湾和广东已出现裂解位点突变的高致病特性H7N9毒株[3 – 4]。神经氨酸酶(neuraminidase,NA)蛋白主要作用是促进流感病毒侵染、复制、成熟及释放等,所以NA蛋白成为开发新抗流感药物的靶点[5]。本研究通过对广西壮族自治区南宁市2017年2月18日发生的1例H7N9禽流感病毒株A/01/ 2017 HA和NA基因序列同源比对构建系统发育树,了解南宁市首例本土人感染H7N9禽流感病毒株的遗传变异及溯源,为H7N9禽流感病毒监测、防控及疫苗株的开发提供科学依据。
1 材料与方法 1.1 样本来源H7N9禽流感病毒株A/01/2017(H7N9)来源于2017年2月18日广西壮族自治区南宁市西乡塘疾病预防控制中心对不明原因肺炎病例(重症患者:李某,女性,42岁,职业为个体经营卖活鸡、活鸭,2017年2月11日发病)采集的下呼吸道痰液,经南宁市疾病预防控制中心国家级流感网络实验室逆转录聚合酶链反应( reverse transcriptionPCR,RT-PCR)试验鉴定,H7N9核酸阳性标本。
1.2 RNA提取和RT-PCR扩增(表1)参照卫计委公布的《人感染H7N9禽流感疫情防控方案》[6]检验。RNA提取试剂盒和RT-PCR试剂和反转录试剂盒均购于德国QIAGEN公司,按说明书操作。PCR扩增产物经毛细管电泳检测后,委托生工生物工程(上海)股份有限公司完成。
| 表 1 引物名称和序列 |
1.3 生物信息学分析HA和NA基因序列和氨基酸序列
将获得的H7N9禽流感病毒株HA和NA基因序列,NCBI数据库BLAST比对下载20株毒株序列,利用生物信息学软件NTI 10.1、ClustalX 2.0、Mega 5.1进行同源比对构建系统进化树,分析毒株HA蛋白受体结合位点、裂解位点、飞沫传播关键氨基酸位点、糖基化位点、抗原决定簇位点及NA蛋白耐药位点、糖基化位点、致病及毒力位点等关键氨基酸位点。通过生物在线软件http://www.cbs.dtu.dk/services/NetNGlyc/预测糖基化位点变化情况。
2 结 果 2.1 病例基本情况李某,女性,42岁,个体经营活鸡、活鸭并宰杀销售,2017年2月11日发病,腹部痛,发热2 d后住院治疗。2月18日采样,经南宁市疾病预防控制中心国家级流感网络实验室RT-PCR实验鉴定,H7N9核酸阳性,2月19日死亡。采集患者经营摊位环境样本以及密切接触者的咽拭子标本,检验结果有环境标本H7N9核酸阳性,密接人员H7N9核酸阴性。
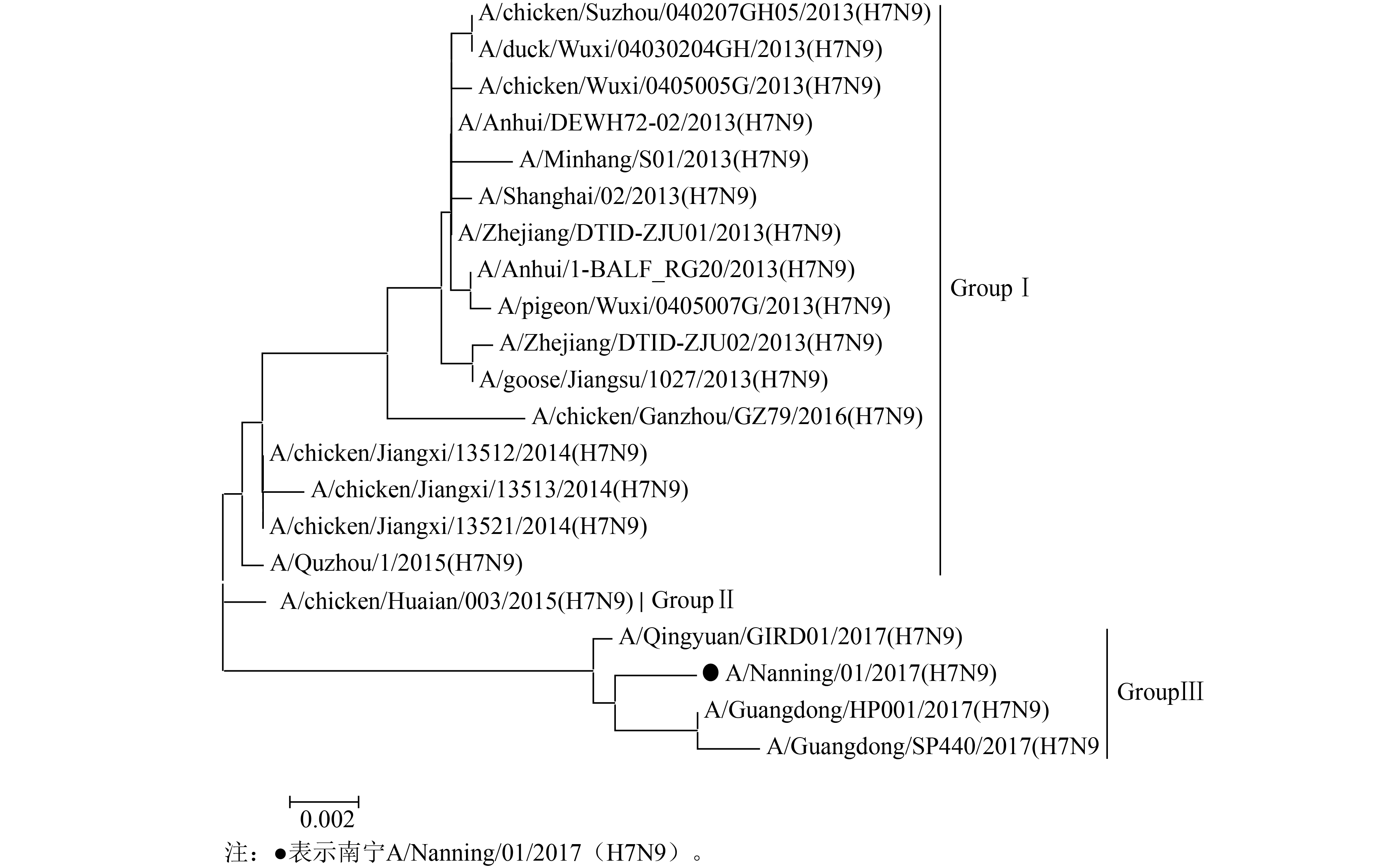
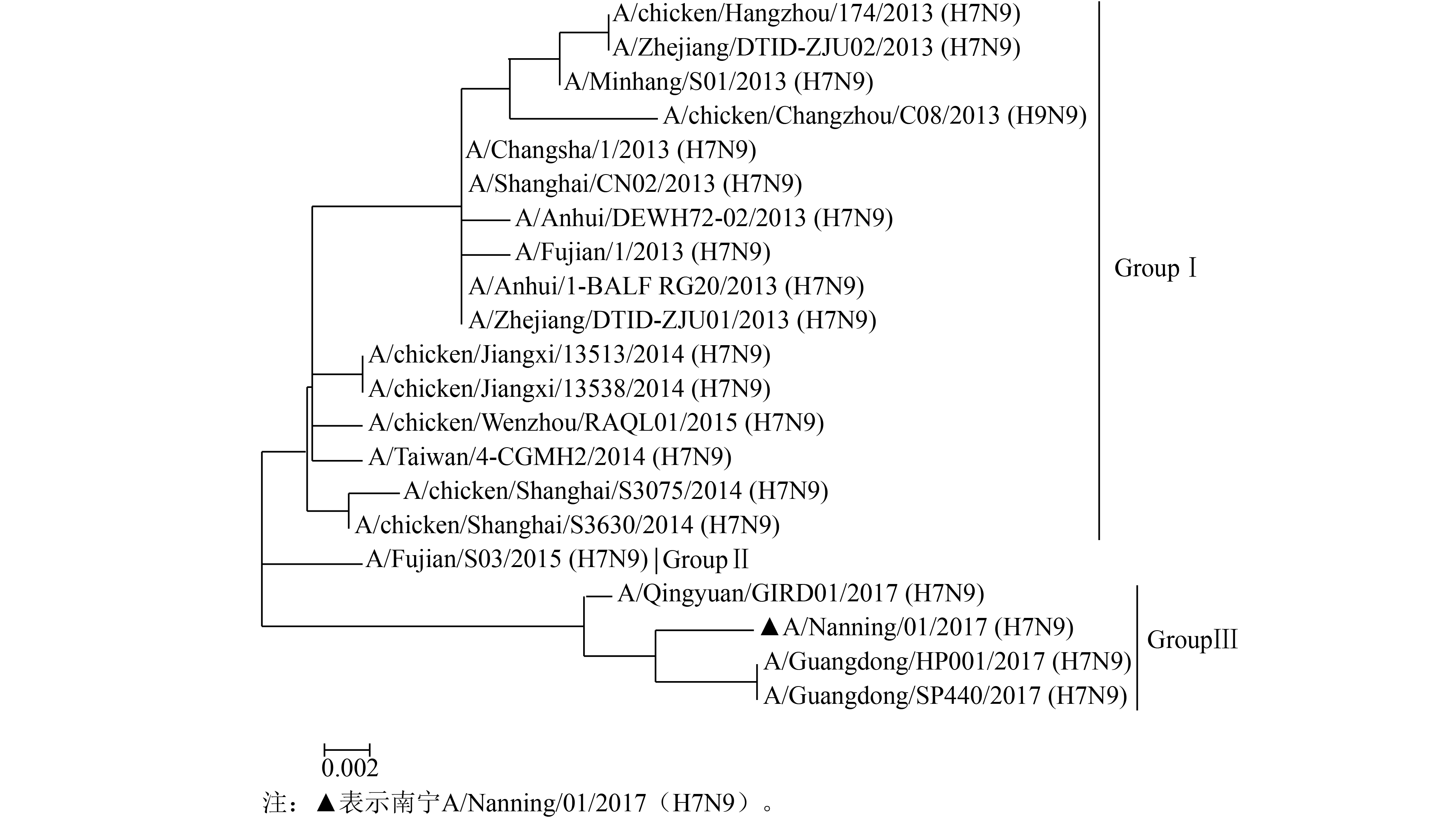
2.2 A/Nanning/01/2017(H7N9)禽流感病毒HA和NA系统发育树分析(图1、2)南宁市H7N9禽流感病毒HA基因长1 695 bp,编码564个氨基酸,前9个氨基酸为信号肽,本文的氨基酸位点为了和文献报道中的氨基酸位点一致,信号肽亦不列入下文氨基酸序列长度,HA基因核苷酸同源性为97.2 %~99.5 %,和A/Guangdong/HP001/2017(H7N9)株同源性最高。与A/Shanghai/02/2013(H7N9)株HA基因比对在1 016 bp位点插入一段12个碱基序列(AACGGACTGCGA),构建的HA基因系统进化树结果如图1所示。从图1可以看出进化树中毒株分化主要分长三角分支和珠三角分支,A/Nanning/01/2017(H7N9)HA在珠三角分支上进化,符合我国禽流感病毒流行性特征。南宁市H7N9禽流感病毒NA基因长1 398 bp,编码465个氨基酸,核苷酸同源性为97.4 %~99.2 %,和A/Qingyuan/GIRD01/2017(H7N9)NA同源性最高。构建的HA基因系统进化树结果如图2所示。从图2可以看出进化树中毒株分化为3个独立分支,但第二分支较少,主要分长三角分支和珠三角分支,A/Nanning/01/2017(H7N9)NA在珠三角分支上进化,符合全国禽流感病毒地域流行性特征。
|
图 1 南宁市2017年A(H7N9)禽流感病毒HA基因进化树 |
|
图 2 南宁市2017年A(H7N9)禽流感病毒NA基因进化树 |
2.3 HA蛋白关键氨基酸位点突变情况分析(表2)
2017年前国内流行的H7N9禽流感HA裂解位点均为PEIPKGR↓GLF,含有2个碱性氨基酸,为低致病性特点。A/Nanning/01/2017(H7N9)株HA蛋白裂解位点329位氨基酸由甘氨酸(G)突变为精氨酸(R)(G329R),330位点插入4个氨基酸由脯氨酸–谷氨酸–异亮氨酸–脯氨酸–赖氨酸–甘氨酸–精氨酸↓甘氨酸–亮氨酸–苯丙氨酸(PEIPKGR↓GLF)突变为脯氨酸–谷氨酸–缬氨酸–脯氨酸–精氨酸–赖氨酸–精氨酸–苏氨酸–赖氨酸–丙氨酸–精氨酸↓甘氨酸–亮氨酸–苯丙氨酸(PEVPKRKRTAR↓GLF),含有5个碱性氨基酸,且含有4个连续的碱性氨基酸,使其具有高致病性禽流感病毒的生物特征,毒力相关位点225由天冬氨酸(D)突变为甘氨酸(G)(D225G)。受体结合位点186和流行毒株一致,均突变为缬氨酸(V),120–环(123~128位氨基酸)的125位点由丙氨酸(A)突变为缬氨酸(V)(A125V)、127位点由丝氨酸(S)突变为天冬酰胺(N)(S127N)位点和180–螺旋(178~185位氨基酸)的178位由异亮氨酸(I)突变为缬氨酸(V)(I178V),但关键的226位点谷氨酰胺没有发生突变(226Q),病毒可能与人呼吸道上皮细胞α2–6半乳糖苷唾液酸(SAα2–6Gal)受体的结合能力没有增强,但226位点突变并不是禽流感病毒感染人类的充分条件。飞沫传播关键氨基酸位点只有160发生突变,由苏氨酸突变为谷氨酸(T160A),所以没有出现这3种突变组合158D/224赖氨酸(K)/226亮氨酸(L)、110酪氨酸(Y)/160丙氨酸(A)/226亮氨酸(L)/228色氨酸(S)和196精氨酸(R)/226亮氨酸(L)/228色氨酸(S),尚未获得飞沫传播的重要条件,人传人可能性较小。HA均含有5个保守的潜在糖基化位点,分别为30NGTK、46NATE、249NDTV、421NWTR和493NNTY。
| 表 2 南宁市H7N9禽流感病毒株HA蛋白氨基酸突变位点分析 |
2.4 NA关键氨基酸位点突变情况分析(表3)
A/Nanning/01/2017(H7N9)株与野生型N9相比,NA蛋白在69位缺失了谷氨酰胺–异亮氨酸–丝氨酸–天冬酰胺–苏氨酸(QISNT)5个氨基酸,这是水禽到陆禽的一种适应性突变,可能增强病毒对哺乳动物的毒性和促进繁殖,毒力相关位点322(322S)位点没有发生突变。NA保守的酶活性中心位点119R、120E、152D、153R、200N、226R、229E、245D、276H、278E、279E、294R、332D、351K、427E 15个氨基酸均未发生突变,特别是2个最关键位点276(对应本文中的271H位点)和294(对应本文中的289R位点)都没有发生突变,294位点对底物和NA抑制剂的结合很重要,294位点是赖氨酸的NA蛋白活性比精氨酸的低,294位点的突变会导致病毒NA抑制剂产生不同程度的耐药性,此毒株保留了病毒对NA抑制剂的敏感性,说明NA抑制剂还可在患者中使用。7个潜在糖基化位点42NCSR、52NTSQ、63NETN、66NITN、82NLTK、142NGTI和197NASA均相对保守,致病及毒力相关位点未发生突变。
| 表 3 南宁市H7N9禽流感病毒株NA蛋白氨基酸突变位点分析 |
3 讨 论
尽管禽流感病毒具有种属屏障,但偶然也会感染人,已发现感染人的亚型主要有H5N1、H5N6、H7N2、H7N3、H7N7、H9N2、H10N8、H6N1和H7N9,其中H5N1和H7N9对禽类及人有较高的致病性。H7N9禽流感病毒是一种三原重组的新病毒,由于人及其他动物对该病毒完全缺乏免疫力,使病毒易于在自然界传播[7 – 8]。人感染后风险极大,死亡率可达40%,目前没有H7N9禽流感人传播人之的报道,但有数宗家庭聚集性案例,提示H7N9禽流感病毒存在有限人传人的可能[9]。
2017年2月南宁市出现首例本土人感染H7N9禽流感病毒,HA基因和NA基因系统进化分析表明A/Nanning/01/2017(H7N9)株与广东省珠三角地区A/Guangdong/HP001/ 2017(H7N9)、A/Guangdong/SP440/2017(H7N9)和A/Qingyuan/GIRD01/2017(H7N9)株高度同源。广西毗邻广东,一直存在活禽贸易,况且广东2017年初关闭活禽交易市场。推测南宁此株H7N9禽流感可能是通过广东禽类运输贸易传染,也可能是和广东被同样的禽类传染。该病毒HA蛋白裂解位点一个氨基酸发生突变和插入4个氨基酸,由2个碱性氨基酸突变为含5个碱性氨基酸,具备了高致病性禽流感病毒的分子特征。因为HA对蛋白酶裂解的敏感性直接影响到病毒的毒力,碱性氨基酸越多,越容易被组织细胞内的蛋白酶识别和裂解,从而具有高致病性。毒力相关位点(D225G)的突变,也可使毒株毒力增强[10 – 11]。HA蛋白与人呼吸道上皮细胞SA-a2、6-Gal受体结合位点只有186位点发生了变异(G186V),可能不具备受体高效结合的分子基础,但提示病毒已经向哺乳动物传播进化[12];未发生飞沫传播关键氨基酸组合突变,对南宁患者密切接触者检验,结果H7N9核酸阴性,没有发生人传人疫情,与于玉凤等[13]研究结果一致。我国内地已报道由裂解位点突变的高致病性H7N9禽流感变异病毒感染患者26例,其中13例死亡,造成5.7万羽鸡死亡,超过30万羽鸡被扑杀。NA蛋白丢失5个氨基酸(QISNT),毒力可能增强,耐药性位点未发生氨基酸变化,糖基化位点均相对保守,毒株对奥司他韦类药物敏感,还可继续使用,但对H7N9禽流感疫苗的研发带来了新的挑战[14 – 15]。
南宁市首例H7N9禽流感患者是暴露于活禽环境中并直接接触活禽感染,在外环境监测时发现有H7N9核酸阳性标本,政府部门采取活禽市场清洗、消毒、休市等措施,控制了疫情的蔓延。专家称零存栏(“禁止活禽过夜”的日日清)措施效果显著,可阻断不同来源和批次禽类间的接触,降低禽流感病毒传播和重组的机率[16]。加大对禽类从业人员宣传教育,提高个人防护意识,降低禽流感感染的风险。但随着越来越多的城市活禽市场关闭和疫区宰杀数量的下降,病毒会沿着家禽运输和交易的路线隐性传播,范围也会不断扩大。禽流感病毒若要突破种属障碍能够成功跨种感染人,必定会有蛋白质关键氨基酸位点发生突变。因此,加强对H7N9禽流感病毒的变异监测,从分子水平掌握禽流感病毒的流行规律和致病机制,可为H7N9禽流感的预防控制提供科学依据。
| [1] | 修文琼, 郑奎城. 新型H7N9禽流感病毒研究进展[J]. 中国人兽共患病学报, 2014, 30(6): 636–644. |
| [2] | 张继荣, 姚青, 高玉婧. 人感染H7N9病毒血凝素基因分析[J]. 家畜生态学报, 2016, 37(7): 68–72. |
| [3] | Suguitan AL Jr, Matsuoka Y, Lau YF, et al. The multibasic cleavage site of the hemagglutinin of highly pathogenic A/Vietnam/1203/2004(H5N1) avian influenza virus acts as a virulence factor in a host-specific manner in mammals[J]. Journal of Virology, 2012, 86(5): 2706–2714. DOI:10.1128/JVI.05546-11 |
| [4] | Yang JR, Liu MT. Human infection caused by an avian influenza A (H7N9) virus with a polybasic cleavage site in Taiwan, 2017[J]. Journal of the Formosan Medical Association, 2017, 116(3): 210–212. DOI:10.1016/j.jfma.2017.02.011 |
| [5] | 孙一桐, 金能智, 张海蓉, 等. A/H7N9流感病毒神经氨酸酶进化分析[J]. 病毒学报, 2014, 30(1): 44–50. |
| [6] | 中华人民共和国国家卫生和计划生育委员会. 人感染H7N9禽流感疫情防控方案第三版[EB/OL]. (2014 – 01 – 27). http://www.nhfpc.gov.cn/zwgk/wtwj/201401/8c1828375a7949cd85454a76bb84f23a.shtml. |
| [7] | Nidom CA, Takano R, Yamada S, et al. Influenza A (H5N1) viruses from pigs, Indonesia[J]. Emerging Infectious Diseases, 2010, 16(10): 1515–1523. DOI:10.3201/eid1610.100508 |
| [8] | Gao R, Cao B, Hu Y, et al. Human infection with a novel avian-origin influenza A (H7N9) virus[J]. New England Journal of Medicine, 2013, 368(20): 1888–1897. DOI:10.1056/NEJMoa1304459 |
| [9] | Jie Z, Xie J, He Z, et al. Family outbreak of severe pneumonia induced by H7N9 infection[J]. American Journal of Respiratory Critical Care Medicine, 2013, 188(1): 114–115. DOI:10.1164/rccm.201304-0797LE |
| [10] | Zhang F, Bi Y, Wang J, et al. Human infections with recently-emerging highly pathogenic H7N9 avian influenza virus in China[J]. Journal of Infection, 2017, 75(1): 71–75. DOI:10.1016/j.jinf.2017.04.001 |
| [11] | Zhu W, Zhou J, Li Z, et al. Biological characterisation of the emerged highly pathogenic avian influenza (HPAI) A (H7N9) viruses in humans, in mainland China, 2016 to 2017[J]. European Communicable Disease Bulletin, 2017, 22(19): 1–5. |
| [12] | Shi Y, Zhang W, Wang F, et al. Structures and receptor binding of hemagglutinins from human-infecting H7N9 influenza viruses[J]. Science, 2013, 342(6155): 243–247. DOI:10.1126/science.1242917 |
| [13] | 于玉凤, 郭晓兰, 王颖, 等. H7N9禽流感病毒对人类致病的分子基础分析[J]. 中山大学学报, 2013, 34(5): 657–665. |
| [14] | 陈国清, 王瑶, 李春香, 等. 2016年盐城市1例人感染H7N9禽流感病毒HA, NA基因变异分析[J]. 现代预防医学, 2016, 43(19): 3604–3608. |
| [15] | Wu Y, Bi Y, Vavricka CJ, et al. Characterization of two distinct neuraminidases from avian-origin human-infecting H7N9 influenza viruses[J]. Cell Research, 2013, 23(12): 1347–1355. DOI:10.1038/cr.2013.144 |
| [16] | 刘静雯, 刘慧, 陆剑云, 等. 广州市2013 — 2015年人感染H7N9禽流感外环境监测结果分析[J]. 中国公共卫生, 2016, 32(10): 1382–1386. DOI:10.11847/zgggws2016-32-10-22 |
 2018, Vol. 34
2018, Vol. 34


