贝氏柯克斯体(Coxiella burnetti, C.burnetti)是一种高度多形的专性细胞内寄生革兰阴性菌,对外界物理和化学因素抵抗力强,可通过污染的土壤、灰尘或动物排泄物气溶胶进行传播,传染性极强,目前已被世界反恐组织列为生物战剂之一[1-2]。贝氏柯克斯体可引起人和牛羊等家畜发生急慢性寇热(Q fever),该病是在世界范围内分布最为广泛的一种人畜共患自然疫源性疾病[3-4]。Q热在临床上因缺乏特异的症状常被误诊为其他疾病。本研究建立针对贝氏柯克斯体的快速可视化环介导等温扩增(loop-mediated isothermal amplification, LAMP)方法,为实现Q热的早期诊断打下基础。
1 材料与方法 1.1 主要仪器与试剂Loopamp LA-320C实时浊度仪、LAMP法DNA扩增试剂盒(北京蓝谱公司),羟基萘酚蓝(hydroxynaphthol blue, HNB)(美国Sigma公司),ABI 7500 Fast实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction, qPCR)仪(美国Applied Biosystems公司),pGEM-T载体(美国Promega公司),SanPrep柱式质粒小量抽提试剂盒(上海生工公司),Premix Ex TaqTM、Takara TaqTM、dNTP mixture(2.5 μM)、DL 1 000 DNA Marker(大连宝生物公司)。
1.2 样品贝氏柯克斯体新桥株、立氏立克次体R株、斑点热立克次体、普氏立克次体E株和加拿大立克次体的基因组DNA由军事医学科学院五所馈赠。恙虫病Ot地方株由南京军区军事医学研究所实验室感染小白鼠传代保存。
1.3 方法 1.3.1 重组质粒的构建与扩增根据NCBI公布的贝氏柯克斯体特有的htpAB基因相关重复序列(IS1111a)(GenBank:M80806.1, CDS:89-1108, 1020 bp),由上海生工公司进行体外基因合成,将目的片段连接pGEM-T载体,并通过双酶切和测序验证构建质粒的准确性。将重组质粒转化DH 5α感受态细胞,并在溶菌肉汤(lysogeny broth,LB)液体培养基中进行扩增,12 h后抽提菌液质粒,测定其浓度和纯度,并计算拷贝数,计算公式为:拷贝数=质粒浓度(g/μL)×加样体积×阿氏常数/(质粒总长度×1个bp的平均分子量)。
1.3.2 LAMP引物设计与合成(表 1)| 表 1 贝氏柯克斯体的LAMP引物序列 |
针对上述合成的IS1111a基因保守序列,采用在线引物设计软件Primer Explorer software 4.0(http://primerexplorer.jp/elamp4.0.0/index.html)设计3套LAMP引物,每套引物包括2条外引物(F3、B3)、2条内引物(FIP、BIP)及1条/2条环引物(LF、LB),由上海生工公司进行合成和纯化。
1.3.3 LAMP最佳引物筛选以抽提的贝氏柯克斯体重组质粒为模板,将合成的3套LAMP引物分别用LAMP法DNA扩增试剂盒进行扩增,反应体系为:2×反应缓冲液12.5 μL,引物混合液(FIP、BIP各16 μmol/L,F3、B3各2 μmol/L,LF、LB各8 μmol/L)2.5 μL,Bst DNA聚合酶1 μL,模板2 μL,加超纯水至25 μL。使用Loopamp LA-320C实时浊度仪进行孵育,反应条件为63 ℃ 60 min,80 ℃ 5 min。每次反应均设超纯水为阴性对照。通过浊度仪实时观察扩增曲线,选择浊度最高、扩增速率最快的一组引物为最佳引物进行后续反应。
1.3.4 HNB指示剂浓度的优化在上述反应体系中加入HNB颜色指示剂,使其终浓度分别为120、150和200 μmol/L,每个浓度分别设1个阳性反应管和1个阴性对照管,反应结束后比较两管颜色的变化,选择差异最明显的一组为最佳HNB浓度,建立可视化LAMP反应体系。
1.3.5 LAMP特异性检测将贝氏柯克斯体重组质粒和贝氏柯克斯体新桥株、恙虫病Ot地方株、立氏立克次体R株、斑点热立克次体、普氏立克次体E株、加拿大立克次体的基因组DNA分别作为模板,同时设超纯水为阴性对照,按照上述建立的可视化LAMP反应体系在浊度仪中进行扩增,反应结束后肉眼观察反应管内颜色变化,并与浊度仪结果进行对比,检测LAMP方法的特异性。
1.3.6 LAMP敏感性检测将贝氏柯克斯体重组质粒进行10倍梯度的倍比稀释,分别作为模板在浊度仪中进行LAMP扩增,同时设超纯水为阴性对照,反应结束后观察各管颜色变化,并与浊度仪结果对比,检测LAMP方法的敏感性。
1.3.7 普通聚合酶链反应(polymerase chain reaction,PCR)检测针对IS1111a基因序列,用Primer Premier 5.0软件设计普通PCR引物,由上海生工公司进行合成,引物序列为:上游引物5′-GGG TTA AGC GTG CTC AGT ATG TAT C-3′,下游引物5′-CCA TCG TGA GTC CGT ATT CTT GC-3′(360 bp)。将贝氏柯克斯体重组质粒的10倍梯度倍比稀释液分别作为模板进行PCR扩增,反应体系为:上游引物和下游引物(10 μmol)各0.5 μL,10×Buffer 2.5 μL,dNTP Mixture(2.5 μmol/L)2 μL,Takara Taq酶0.3 μL,模板2 μL,加超纯水至25 μL。反应条件:95 ℃ 3 min;94 ℃ 50 s,60 ℃ 55 s,72 ℃ 1 min,35个循环;72 ℃ 10 min,4 ℃保存。将PCR产物进行凝胶电泳成像,确定普通PCR检测的敏感性。
1.3.8 实时荧光定量PCR检测采用文献报道的针对IS1111a基因的实时荧光定量PCR引物及探针序列[5],由上海生工公司进行合成。将贝氏柯克斯体重组质粒的10倍梯度倍比稀释液分别作为模板在ABI 7500 Fast实时荧光定量PCR仪中进行qPCR扩增,反应体系为:Premix Ex TaqTM 10 μL, 上游引物和下游引物(10 μM)各0.4 μL,荧光探针(10 μmol/L)0.8 μL,ROX 0.4 μL,模板2 μL,加超纯水至20 μL。反应条件:95 ℃ 10 s;95 ℃ 5 s,60 ℃ 35 s,40个循环。观察qPCR检测的敏感性。
2 结果 2.1 重组质粒鉴定将体外合成的重组质粒用SalI/ApaI内切酶进行双酶切,酶切产物凝胶电泳显示在1 080 bp和3 000 bp处各有一条清晰条带,与目的片段和pGEM-T载体长度相符,将目的片段进行切胶回收后送测序,结果与送交合成的片段完全吻合,证明贝氏柯克斯体重组质粒构建成功。将重组质粒转化DH 5α感受态细胞,并在LB液体培养基中进行扩增,12 h后抽提质粒DNA,测得OD 260/OD 280为1.73,浓度为160 ng/μL,代入拷贝数计算公式得到贝氏柯克斯体重组质粒的拷贝数为3.6×1010拷贝/μL。
2.2 LAMP最佳引物筛选(图 1)
|
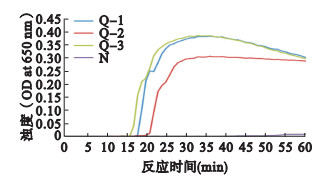
注:Q-1:第1套引物;Q-2:第2套引物;Q-3:第3套引物;N:阴性对照。 图 1 3套LAMP引物实时扩增曲线 |
用合成的3套LAMP引物分别在浊度仪中进行LAMP扩增,反应结束后观察实时扩增曲线,结果显示3套引物均可成功诱发特异性LAMP扩增,其中第2套引物的浊度值最低,为0.3,且扩增速率最慢,在20 min开始有扩增产物出现,在28 min接近峰值,而第1套引物和第3套引物的浊度值均为0.38,第3套引物在16 min开始有扩增产物,在24 min接近峰值,第1套引物在18 min开始有扩增产物,在26 min接近峰值,故选取第3套引物进行后续反应。
2.3 HNB指示剂浓度优化(图 2)
|
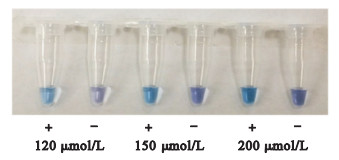
图 2 HNB最佳浓度筛选 |
在LAMP反应体系中加入HNB颜色指示剂,使其终浓度分别为120、150和200 μmol/L,反应前颜色均为紫罗兰色,反应结束后比较颜色变化,加入重组质粒的3个反应管颜色均变为天蓝色,而阴性对照管仍为紫罗兰色,其中HNB浓度为150 μmol/L的一组阳性反应管和阴性反应管颜色对比最为明显,故选取150 μmol/L进行后续可视化LAMP反应。
2.4 LAMP特异性检测(图 3)
|
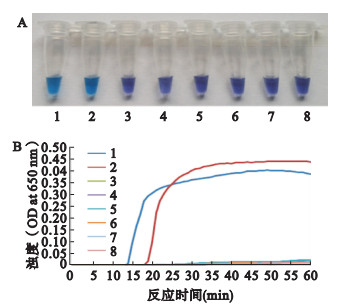
注:A:HNB显色;B:实时浊度图;1:贝氏柯克斯体重组质粒;2:贝氏柯克斯体新桥株;3:恙虫病Ot地方株;4:立氏立克次体R株;5:斑点热立克次体;6:普氏立克次体E株;7:加拿大立克次体;8:阴性对照。 图 3 LAMP特异性检测 |
将贝氏柯克斯体重组质粒和贝氏柯克斯体新桥株、恙虫病Ot地方株、立氏立克次体R株、斑点热立克次体、普氏立克次体E株、加拿大立克次体的基因组DNA分别作为模板进行可视化LAMP反应。除贝氏柯克斯体重组质粒和贝氏柯克斯体新桥株反应管颜色变为天蓝色(图 3A),实时浊度图显示有扩增曲线外(图 3B),其余5种病原体均呈阴性反应,证明该可视化LAMP方法检测贝氏柯克斯体的特异性为100%。
2.5 敏感性检测(图 4)
|
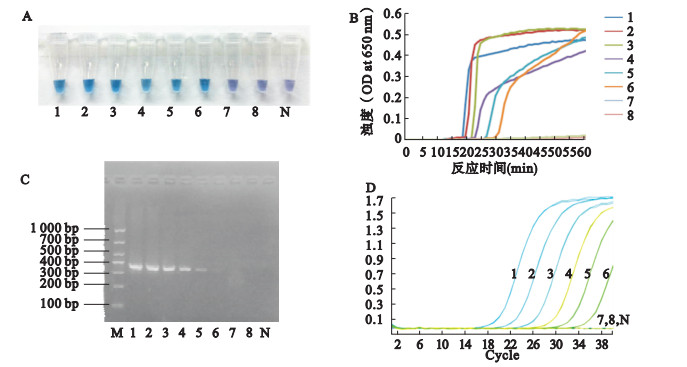
注:A:HNB显色;B:实时浊度图;C:普通PCR;D:实时荧光定量PCR;1:3.6×107拷贝/μL;2:3.6×106拷贝/μL;3:3.6×105拷贝/μL;4:3.6×104拷贝/μL;5:3.6×103拷贝/μL;6:3.6×102拷贝/μL;7:3.6×101拷贝/μL;8:3.6×100拷贝/μL;N:阴性对照;M:DL 1000 DNA marker。 图 4 敏感性检测 |
将贝氏柯克斯体的重组质粒进行10倍梯度的倍比稀释,共10管,取浓度为3.6×107拷贝/μL至3.6×100拷贝/μL的八管分别作为模板进行HNB可视化LAMP扩增,结果发现3.6×107拷贝/μL至3.6×102拷贝/μL的反应管变为天蓝色,其余仍为紫罗兰色,说明LAMP扩增的最低检测限为3.6×102拷贝/反应(图 4A)。浊度仪实时扩增曲线结果(图 4B)和HNB显色结果一致,各浓度梯度质粒的出峰时间介于20~40 min。将同样的质粒模板分别进行普通PCR扩增及qPCR扩增,结果发现两者检测贝氏柯克斯体的最低限分别为3.6×103拷贝/反应和3.6×102拷贝/反应(图 4C、4D)。因此,可视化LAMP扩增法的敏感度等同于qPCR扩增,均高于普通PCR扩增。
3 讨论自1962年中国分离到首例贝氏柯克斯体毒株后,中国已在15个省市的23个地区先后发现了Q热病例。在一项回顾性调查中,研究者发现来自12所医院的500例社区获得性肺炎患者中有44例呈贝氏柯克斯体抗体阳性[6],这些病例在初次诊断中均被误诊为普通肺炎,说明中国目前对Q热的诊断尚未引起足够的重视,而缺乏敏感、准确的早期诊断方法也是导致Q热被误诊的重要原因之一。由于Q热大多发生在有牛、羊等家畜生活的农村偏远地区,而这些地区往往缺乏先进的诊疗设备,因此,建立一种简单快捷、敏感特异的贝氏柯克斯体检测方法对于提高中国Q热检出率、加强疾病防控具有重大的现实意义。LAMP是由Notomi等[7]在2000年建立起来的一种核酸检测方法,该法针对目标序列设计了4条或6条引物,可在60~65 ℃的等温条件下1 h内实现靶基因109倍的扩增。LAMP方法操作简单,仅需一个简单的恒温装置即可完成,具有极高的灵敏度和特异性,结合钙黄绿素或HNB等颜色指示剂可肉眼判断反应结果,非常适合于野外快速诊断[8-9]。目前该方法已应用于多种病原微生物的检测[10-11]。
本研究以贝氏柯克斯体特有的htpAB转座酶基因上的一个重复性插入序列IS1111a为检测靶标,该序列在各个贝氏柯克斯体毒株中均较为保守,且在基因组上拷贝数高,因此针对该序列设计引物检测灵敏度较高,大多数基于PCR扩增的Q热检测法也均以该基因为靶标[5, 12-13]。利用构建的重组质粒,建立贝氏柯克斯体的HNB可视化LAMP检测方法,该方法可成功检出1964年由俞树荣等[14]从重庆铃头血蜱中分离到的贝氏柯克斯体新桥株,同时可区分恙虫病、斑点热等其他立克次体感染,具有高度特异性。此外,通过条件优化,本研究建立的HNB可视化LAMP方法最低可检测到3.6×102拷贝/反应,敏感性和qPCR相当,较普通PCR检测提高了一个数量级。同时,该HNB-LAMP法的检测时间为20~40 min,要大大小于qPCR法的75 min和普通PCR法的3 h,且脱离了对精密温控仪器的依赖,更适合于基层单位和疫情现场开展病原检测。然而,本研究报道的灵敏度要略低于其他研究者采用电泳法检测LAMP产物的灵敏度,如Pan和Chen针对IS1111a基因建立的LAMP检测方法的灵敏度分别为1拷贝/反应和25拷贝/反应[15-16]。但电泳法需在反应结束后开盖进行操作,高浓度的LAMP产物可能产生气溶胶,造成环境污染,导致后续实验易出现假阳性,且电泳法操作繁琐耗时,不适合在疫情现场展开。
因此,本研究建立的LAMP方法可敏感和特异地检测贝氏柯克斯体,只需简单的恒温装置即可完成,反应结束后直接肉眼判断结果,操作方便快捷,20~40 min内可判定是否存在贝氏柯克斯体感染,非常适用于基层单位开展日常监测和疫情暴发现场的病原快速诊断。但后续还需要收集更多的临床样本来进一步评估其实际诊断价值。
| [1] | Angelakis E, Raoult D. Q fever[J]. Vet Microbiol, 2010, 140(3-4): 297–309. DOI:10.1016/j.vetmic.2009.07.016 |
| [2] | Dorko E, Rimarova K, Pilipcinec E. Influence of the environment and occupational exposure on the occurrence of Q fever[J]. Cent Eur J Public Health, 2012, 20(3): 208–214. |
| [3] | EI-Mahallawy H, Lu G, Kelly P, et al. Q fever in China:a systematic review, 1989-2013[J]. Epidemiol Infect, 2015, 143(4): 673–681. DOI:10.1017/S0950268814002593 |
| [4] | Cong W, Meng QF, Shan XF, et al. Coxiella burnetii(Q fever)infection in farmed ruminants in three northeastern provinces and Inner Mongolia Autonomous Region, China[J]. Vector Borne Zoonotic Dis, 2015, 15(8): 512–514. DOI:10.1089/vbz.2015.1789 |
| [5] | Schneeberger PM, Hermans MH, van Hannen EJ, et al. Real-time PCR with serum samples is indispensable for early diagnosis of acute Q fever[J]. Clin Vaccine Immunol, 2010, 17(2): 286–290. DOI:10.1128/CVI.00454-09 |
| [6] | 程仕虎, 刘又宁, 李朝霞, 等. 44例被误诊为普通性肺炎的Q热柯克斯体肺炎病人的回顾性分析[J]. 科学技术与工程, 2007, 7(10): 2335–2339. DOI:10.3969/j.issn.1671-1815.2007.10.038 |
| [7] | Notomi T, Okayama H, Masubuchi H, et al. Loop-mediated isothermal amplification of DNA[J]. Nucleic Acids Res, 2000, 28(12): E63. DOI:10.1093/nar/28.12.e63 |
| [8] | Zhang J, Zhu J, Ren H, et al. Rapid visual detection of highly pathogenic Streptococcus suis serotype 2 isolates by use of loop-mediated isothermal amplification[J]. J Clin Microbiol, 2013, 51(10): 3250–3256. DOI:10.1128/JCM.01183-13 |
| [9] | Zhang J, Feng Y, Hu D, et al. Rapid and sensitive detection of H7N9 avian influenza virus by use of reverse transcription-loop-mediated isothermal amplification[J]. J Clin Microbiol, 2013, 51(11): 3760–3764. DOI:10.1128/JCM.01907-13 |
| [10] | 姚文山, 吴家林, 沙丹, 等. 霍乱弧菌毒力基因LAMP方法快速检测[J]. 中国公共卫生, 2015, 31(1): 67–69. DOI:10.11847/zgggws2015-31-01-20 |
| [11] | 易海华, 赵金伟, 房超, 等. 志贺菌环介导等温扩增检测方法建立[J]. 中国公共卫生, 2011, 27(3): 380–382. DOI:10.11847/zgggws2011-27-03-64 |
| [12] | Boden K, Wagner-Wiening C, Seidel T, et al. Diagnosis of acute Q fever with emphasis on enzyme-linked immunosorbent assay and nested polymerase chain reaction regarding the time of serum collection[J]. Diagn Microbiol Infect Dis, 2010, 68(2): 110–116. DOI:10.1016/j.diagmicrobio.2010.06.001 |
| [13] | Panning M, Kilwinski J, Greiner-Fischer S, et al. High throughput detection of Coxiella burnetii by real-time PCR with internal control system and automated DNA preparation[J]. BMC Microbiol, 2008, 8: 77. DOI:10.1186/1471-2180-8-77 |
| [14] | Wen BH, Yu SR, Yu GQ, et al. Analysis of proteins and lipopolysaccharides from Chinese isolates of Coxiella burnetii with monoclonal antibodies[J]. Acta Virol, 1991, 35(6): 538–544. |
| [15] | Pan L, Zhang L, Fan D, et al. Rapid, simple and sensitive detection of Q fever by loop-mediated isothermal amplification of the htpAB gene[J]. PLoS Negl Trop Dis, 2013, 7(5): e2231. DOI:10.1371/journal.pntd.0002231 |
| [16] | Chen HW, Ching WM. Development of loop-mediated isothermal amplification assays for rapid and easy detection of Coxiella Burnetii[J]. J Microbiol Methods, 2014, 107: 176–181. DOI:10.1016/j.mimet.2014.07.039 |
 2017, Vol. 33
2017, Vol. 33


