胃癌是最常见的消化道恶性肿瘤之一,尽管胃癌的发病率和死亡率在过去的几十年里有所下降,但仍然是一个重大的公共健康问题,占癌症死亡人数中第4位[1]。胃癌的发生发展是多因素参与复杂过程,细胞凋亡的调控机制发生紊乱是胃癌形成过程中重要机制之一。姜黄素是中药姜黄的主要活性成分之一,具有抗氧化生物学效应、提高免疫力、抗血管生成、抗炎、降脂等作用,在多种恶性肿瘤的治疗中发挥着重要作用[2-6]。研究发现姜黄素还可抑制多种转录活化因子,包括:转录因子激活蛋白-1(activator protein-1, AP-1)、核转录因子(nuclear factor-kappa B, NF-κB)等信号转导蛋白。Livin蛋白可通过核转录因子信号通路诱导纤粘蛋白调控前列腺癌细胞的转移和侵袭。Caspase-3作为重要的凋亡执行因子,是细胞调亡过程中的关键蛋白酶,caspase-3一旦激活,细胞调亡将不可避免。本研究旨在观察姜黄素在诱导胃癌细胞凋亡过程中的作用及机制。结果报告如下。
1 材料与方法 1.1 主要试剂与仪器SGC-7901人胃癌细胞(南华大学实验室苏琦教授馈赠);1640培养基(美国Hyclone公司);细胞计数试剂盒8(cell counting kit-8,CCK-8)(上海翌圣生物科技有限公司);0.25%胰蛋白酶、二甲基亚砜(dimethyl sulfoxide, DMSO)、冻存液(美国Sigma-Aldrich公司);PI染色液(上海Biosharp公司);兔抗人p65抗体(一抗)(上海生工生物工程股份有限公司);兔抗人caspase-3抗体(一抗)(沈阳万类生物科技公司);兔抗人livin抗体、羊抗鼠抗体(美国Abcam公司);姜黄素,纯度98%(上海丽臣商贸有限公司)。酶标仪(芬兰Thermo Labsystems公司);垂直电泳槽及电泳电源、凝胶成像系统(美国BIO-RAD公司);FC-500流式细胞仪(美国Beckman公司)。
1.2 细胞培养SGC-7901细胞用10%胎牛血清培养,放入37 ℃、5%CO2培养箱中,待培养皿细胞贴壁并达到90%时,0.25%胰酶消化,镜下观察大多数贴壁细胞由梭形逐渐变为圆形(若细胞未漂起,可轻轻拍打瓶壁)时终止消化,按1:2传代,于37 ℃、5%CO2培养箱中继续培养;24~48 h换液1次。
1.3 指标与方法 1.3.1 细胞活力检测采用CCK-8法,将对数生长期的贴壁细胞,用胰酶消化后,用培养基配制成所需浓度的单细胞悬液,按每孔1 000个细胞加入到96孔细胞培养板中,37 ℃、5%CO2条件下预贴壁12 h后分别加入不同浓度姜黄素,0(对照组)、10、20、40、60、80、100 μmol/L,每个浓度设置5个复孔,分别培养24、48、72 h后倾去上清;加入CCK-8液,37 ℃培养1 h后用酶标仪在450 nm波长条件下测定吸光度(A)值;计算细胞活力(%)。
1.3.2 细胞凋亡率及细胞周期检测采用流式细胞术法,将对数生长期的贴壁细胞,胰酶消化后,用培养基配制成所需浓度的单细胞悬液,按每孔3 000个细胞加入到6孔细胞培养板中,并编号为1、2、3、4孔;待细胞数量达到106个/孔后,向1孔中加入2 mL 1 640培养基,分别向2、3、4孔中加入20、40、60 μmol/L姜黄素,放入37 ℃、5%CO2培养箱中;24 h后用0.2 mL胰酶消化、重悬细胞在室温下,2 000 r/min,离心5 min,收集细胞。Annexin V-FTTC混匀,上机前5 min加入5 μL PI染色,上机检测。
1.3.3 细胞内NF-κB、livin和caspase-3蛋白表达检测采用Western blot法,细胞培养于6孔板中,分别加入20、40、60 μmol/L姜黄素处理后,用细胞裂解液裂解细胞得胞质蛋白,用二喹啉甲酸(bicinchoninic acid, BCA)法检测蛋白浓度。取10 μL蛋白上样到10%十二烷基硫酸钠-聚丙酰胺凝胶,电泳、转移至聚偏二氟乙烯膜,5%脱脂牛奶室温下封闭2 h,分别用抗NF-κB抗体(1:500),抗livin抗体(1:500) 和抗caspase-3抗体(1:300),4 ℃孵育过夜;以β-actin为内参,用辣根过氧化物酶标记的二抗孵化1 h,Tris吐温缓冲液(Tris buffered saline with Tween-20,TBST)洗膜3次,电化学发光显影,用凝胶成像系统显色采集图像。
1.4 统计分析采用SPSS 18.0软件进行统计分析,组间比较采用方差分析,两两比较采用单因素配对样本t检验,P < 0.05为差异有统计学意义。
2 结果 2.1 姜黄素对SGC-7901细胞增殖活力影响(图 1)
|
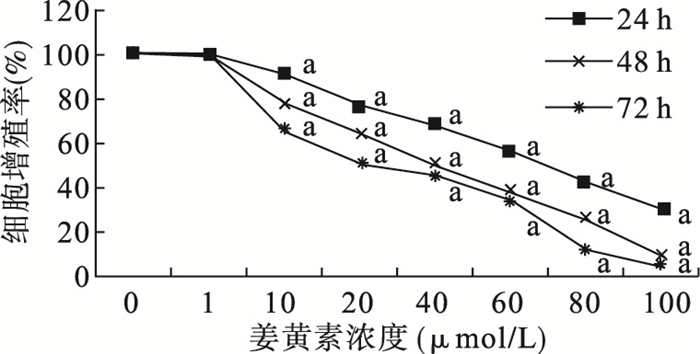
注:0:对照组;1:DMSO组;a P < 0.01。 图 1 姜黄素对SGC-7901细胞增殖活力影响 |
与对照组比较,各剂量姜黄素组SGC-7901细胞增殖活力均受到抑制(P < 0.05);呈剂量依赖性(r=0.901,P < 0.01) 与时间依赖性(r=0.389,P= < 0.01);IC50为63.2 μmol/L,考虑后续实验中姜黄素浓度对细胞作用,后续实验分别选择20、40、60 μmol/L 3个浓度组作为剂量组。
2.2 姜黄素对SGC-7901细胞凋亡影响对照组、20、40、60 μmol/L姜黄素组SGC-7901细胞凋亡率分别为2.8%、7.7%、13.4%、20.7%;与对照组比较,各剂量姜黄素组SGC-7901细胞凋亡率明显升高,差异有统计学意义(P < 0.05)。
2.3 姜黄素对SGC-7901细胞周期影响(表 1)| 表 1 姜黄素对SGC-7901细胞周期影响 |
与对照组比较,20、40、60 μmol/L姜黄素组SGC-7901周期G1期比例明显增加,S期比例下降。提示,一定浓度的姜黄素对细胞周期有明显的阻滞作用,且将细胞周期阻滞在G1期。
2.4 姜黄素对SGC-7901细胞内NF-κB、livin、caspase-3蛋白表达影响(图 2、表 2)
|
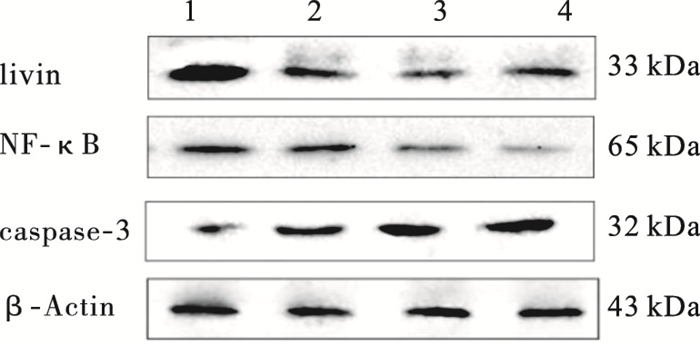
注:1:对照组;2~4:姜黄素20、40、60 μmol/L组。 图 2 姜黄素对SGC-7901细胞NF-κB、livin、caspase-3蛋白表达影响 |
| 表 2 姜黄素对SGC-7901细胞NF-κB、livin、caspase-3蛋白表达影响(x±s,n=5) |
结果显示,与对照组比较,姜黄素20、40、60 μmol/L组SGC-7901细胞内NF-κB和livin蛋白表达明显降低,caspase-3蛋白表达升高。提示,姜黄素可能通过下调NF-κB信号通路及livin蛋白表达,增加caspase-3蛋白表达,从而发挥对SGC-7901细胞抑制作用。
3 讨论凋亡在维持体内细胞或组织平衡中发挥着关键作用,凋亡逃避使肿瘤细胞破坏细胞内环境稳定及对肿瘤药物产生耐药性。抗凋亡分子蛋白抑制肿瘤细胞凋亡和诱导转移,从而增加肿瘤的侵袭性[7]。本研究结果显示,随着姜黄素浓度增加,SGC-7901细胞凋亡率增加,细胞增殖活力下降,呈剂量和时间依赖关系;处于G1期的SGC-7901细胞数目明显增加,且S期的细胞数目下降。提示,姜黄素对SGC-7901细胞增殖具有抑制作用,且主要发生在G1期。
核转录因子NF-κB几乎在所有肿瘤细胞中均有表达,同时抑制大部分的肿瘤细胞凋亡。研究表明姜黄素通过诱导肿瘤坏死因子(tumor necrosis factor, TNF)、H2O2从而抑制NF-κB的活性。姜黄素可增加乳腺癌细胞对氟尿嘧啶(5-fluorouracil, 5-FU)的敏感性,通过胸苷酸合成酶独立下调NF-κB的活性,从而促进乳腺癌细胞凋亡[8]。姜黄素可能通过增强抗氧化作用及抑制脂质过氧化反应,对四氯化碳诱导的肝纤维化具有干预作用[9]。在Burkitt淋巴瘤中,姜黄素可通过抑制磷脂酰肌醇3激酶/白激酶B(phosphatidylinositol-3 kinase/protein kinase B, PI3K/AKT)信号通路及其下游调节器NF-κB信号通路增加放疗敏感性,促进淋巴瘤细胞凋亡[10]。5-FU可增加NF-κB/ PI-3K/Src信号通路活性,使得多种肿瘤细胞对5-FU产生耐药。姜黄素可通过抑制IκBα的磷酸化阻断NF-κB信号通路,促进细胞凋亡,抑制细胞增殖,增加细胞对5-FU的敏感性,增加食管鳞癌细胞的凋亡[11]。Livin可作用于NF-κB和其下游的相关信号通路纤连蛋白(fibronectin, FN)和CXC趋化性细胞因子受体4(CXC chemokine receptor 4, CXCR4),在前列腺癌组织中livin蛋白高表达可促进FN和CXCR4表达,这可能与livin蛋白调控NF-κB有关[12];livin蛋白通过NF-κB信号通路诱导纤粘蛋白调控前列腺癌细胞的转移和侵袭[13]。本研究结果显示,姜黄素可下调胃癌细胞内NF-κB表达,可能与细胞livin蛋白(凋亡抑制蛋白)密切相关。
近年研究发现,多种肿瘤细胞中表达细胞凋亡抑制蛋白(inhibitor of apoptosis proteins,IAPs),现已确定IAPs家族包含8个成员,cIAP1、cIAP2、XIAP、ILP-2、NAIP、BRUCE、survivin及livin蛋白[14]。Livin是新近发现的一个IAP家族成员,在细胞凋亡、生长及细胞周期调控中可能扮演重要角色。Livin在正常成人的大多数终末组织中(除胎盘)低表达或不表达,而在多数恶性肿瘤中高表达。因此,livin可能成为抗肿瘤治疗的一个潜在靶点。研究证实抗凋亡机制可能与caspase下游的caspase-3、caspase-7与IAPS的N端重复序列结构域(baculovirus IAP repeats domain BIR)结合相关[15-17]。Livin可通过抑制线粒体来源的胱冬肽酶激活剂(second mitochondria-derived activator of caspase, SMAC)释放发挥抗凋亡作用,通过TGF β(transforming growth factor beta)激活性激酶1(transforming growth factor-beta-activated kinase-1, TAK1) 和c-Jun氨基末端激酶1(c-Jun N-terminal kinases 1, JNK1) 信号通路抑制细胞凋亡[18-19]。Livin蛋白C端环指结构可引起caspase蛋白的降解从而发挥抗凋亡作用[20]。在食管癌研究中发现,姜黄素处理食管癌细胞后,SMAC蛋白表达水平升高,激活procaspase-3,发挥其诱导肿瘤细胞凋亡作用[21]。在宫颈鳞状细胞癌研究中,livin蛋白通过下调caspase-3抑制宫颈癌细胞凋亡,从而促进疾病发生、发展[22]。Caspase-3同livin在肺癌组织中呈负相关,livin可能抑制caspase-3活性抑制细胞凋亡[23]。Caspass-3是执行调亡的主要效应分子,被认为是调亡过程中的关键蛋白酶,一旦激活caspass-3,立即发生下游的级联反应,调亡不可避免。caspase-3表达异常可能在多种恶性肿瘤的发生中起重要作用。本研究结果显示,姜黄素可抑制胃癌细胞livin蛋白表达,增加caspase-3蛋白表达。提示,姜黄素促细胞凋亡作用机制可能与下调胃癌细胞内NF-κB表达,抑制livin蛋白表达,激活caspase-3蛋白表达有关。
| [1] | Ferlay J, Steliarovafoucher E, Lortettieulent J. Cancer incidence and mortality patterns in Europe:estimates for 40 countries in 2012[J]. European Journal of Cancer, 2015, 51(9): 1201–1202. DOI:10.1016/j.ejca.2015.05.004 |
| [2] | Saxena V, Hussain MD. Polymeric mixed micelles for delivery of curcumin to multidrug resistant ovarian cancer[J]. J Biomed Nanotechnol, 2013, 9(7): 1146–1154. DOI:10.1166/jbn.2013.1632 |
| [3] | Kim HJ, Park SY, Park OJ, et al. Curcumin suppresses migration and proliferation of Hep3B hepatocarcinoma cells through inhibition of the Wnt signaling pathway[J]. Molecular Medicine Reports, 2013, 8(1): 282–286. |
| [4] | Kaushik G, Kaushik T, Yadav SK, et al. Curcumin sensitizes lung adenocarcinoma cells to apoptosis via intracellular redox status mediated pathway[J]. Indian Journal of Experimental Biology, 2012, 50(12): 853–861. |
| [5] | Mo N, Li ZQ, Li J, et al. Curcumin inhibits TGF-β1-induced MMP-9 and invasion through ERK and Smad signaling in breast cancer MDA-MB-231 cells[J]. Asian Pac J Cancer Prev, 2012, 13(11): 5709–5714. DOI:10.7314/APJCP.2012.13.11.5709 |
| [6] | Singh M, Singh N. Curcumin counteracts the proliferative effect of estradiol and induces apoptosis in cervical cancer cells[J]. Mol Cell Biochem, 2011, 47(1-2): 1–11. |
| [7] | Hartman ML, Czyz M. Anti-apoptotic proteins on guard of melanoma cell survival[J]. Cancer Lett, 2013, 331(1): 24–34. DOI:10.1016/j.canlet.2013.01.010 |
| [8] | Vinod BS, Antony J, Nair HH. Mechanistic evaluation of the signaling events regulating curcumin-mediated chemosensitization of breast cancer cells to 5-fluorouracil[J]. Cell Death Dis, 2013, 26(4): 1–13. |
| [9] | 钟越, 钟秀宏, 孙艳美, 等. 姜黄素拮抗四氯化碳致肝纤维化作用[J]. 中国公共卫生, 2015, 31(4): 447–449. DOI:10.11847/zgggws2015-31-04-19 |
| [10] | Qiao Q, Jiang Y, Li G. Inhibition of the PI3K/AKT-NF-κB pathway with curcumin enhanced radiation-induced apoptosis in human Burkitt's lymphoma[J]. J Pharmacol Sci, 2013, 121(4): 247–256. DOI:10.1254/jphs.12149FP |
| [11] | 田芳, 宋敏, 许培荣, 等. 姜黄素阻断NF-κB信号通路促进食管鳞癌细胞凋亡的体外研究[J]. 癌症, 2008(6): 566–570. |
| [12] | Chen F, Yang DY, Wang SJ. Livin regulates prostate cancer cell invasion by impacting the NF-κB signaling pathway and the expression of FN and CXCR4[J]. Iubmb Life, 2012, 64(3): 274–283. DOI:10.1002/iub.v64.3 |
| [13] | Chen F, Yang DY, Che XY. Livin mediates tumor cell invasion in the DU-145 cell line via NF-κB[J]. Oncol Rep, 2012, 27(6): 2010–2016. |
| [14] | Yan B. Research progress on livin protein:an inhibitor of apoptosis[J]. Mol Cell Biochem, 2011, 357(1-2): 39–45. DOI:10.1007/s11010-011-0873-7 |
| [15] | Kasof GM, Gomes BC. Livin, a novel inhibitor of apoptosis protein family member[J]. J Biol Chem, 2001, 276(1): 3238–3246. |
| [16] | Vucic D, Stennicke HR, Pisabarro MT. ML-IAP, a novel inhibitor of apoptosis that is preferentially expressed in human melanomas[J]. Current Biology, 2000, 10(1): 1359–1366. |
| [17] | Lin JH, Deng G, Huang Q, et al. a novel member of the inhibitor of apoptosis protein family[J]. Biochem Biophys Res Commun, 2000, 279(12): 820–831. |
| [18] | Vucic D, Franklin MC, Wallweber HJ. Engineering ML-IAP to produce an extraordinarily potent caspase 9 inhibitor:implications for Smac-dependent anti-apoptotic activity of ML-IAP[J]. Biochem J, 2015, 385(2): 11–20. |
| [19] | Sanna MG, da Silva Correia J, Ducrey O. IAP suppression of apoptosis involves distinct mechanisms:the TAK1/JNK1 signaling cascade and caspase inhibition[J]. Mol Cell Biol, 2002, 22(1): 1754–1766. |
| [20] | Liu GH, Wang C, Ding YZ. Over of the truncated form of Livin reveals a complex interaction with caspase-3[J]. International Journal Of Oncology, 2013, 42(2): 2037–2045. |
| [21] | Zhao HL, Li H, Zuo LF. Experimental study on the effects of curcumin on the induction of apoptosis in the esophageal epithelia Ec-9706 Cell lines[J]. Journal of the Fourth Military Medical University, 2008, 18(2): 1655–1657. |
| [22] | Xu M, Xia LP, Fan LJ. Livin and caspase-3 are negatively correlated in cervical squamous cell cancer[J]. Eur J Gynaecol Oncol, 2013, 34(2): 152–155. |
| [23] | Hong R, Yu S, Ch en, et al. Expression of livin in tissues of lung cancer and its correlation with the expression of caspase-3[J]. Oncology and Translational Medicine, 2008, 7(7): 383–386. |
 2017, Vol. 33
2017, Vol. 33


