喉癌是发生于上皮细胞的一种头颈部常见恶性肿瘤,在耳鼻咽喉科肿瘤中位列第3位,近年来发病率呈上升趋势[1]。其中喉鳞状细胞癌(laryngeal squamous cell carcinoma,LSCC)是喉癌最常见的病理类型,占>90%。迄今为止,LSCC的病因及发病机制尚不清楚,空气污染、吸烟饮酒、病毒感染、遗传变异等因素可能是LSCC发生的原因,其中抑癌基因的失活与癌基因的激活是主要的病因之一[2-3]。miRNA是一类高度保守的长度约为22 nt非编码RNA分子,被认为是一类新型的癌基因或者抑癌基因,并且miRNA芯片研究表明多种miRNA是LSCC预后及诊断的独立影响因子,在LSCC发生发展中起着癌基因或者抑癌基因作用[4-6]。miR-155是一个典型的多功能基因,可通过与下游靶基因如磷脂酰肌醇3激酶/蛋白激酶B/叉形头转录因子(forkhead box 3a,Foxo3a)、ras同源物基因家族成员A(Ras homolog gene family member A,RhoA)的mRNA3非编码区结合,进而参与造血干细胞、免疫反应、炎症反应、肿瘤发生等生物学过程[7-8]。研究表明miR-155在乳腺癌、肺癌、结肠癌、肝癌、喉癌等多种肿瘤中高表达,并且在其中起着癌基因的作用[7, 9]。但是对于miR-155在喉癌中的具体作用机制尚不清楚,因此本研究通过脂质体转染miR-155 inhibitor,探讨miR-155表达下调后对LSCC细胞Hep2增殖的影响及机制。结果报告如下。
1 材料与方法 1.1 主要试剂与仪器LSCC细胞Hep2(中国科学院细胞库);兔抗细胞周期蛋白A1(cell cycle protein A1,cyclinA1)、cyclinD1、磷脂酰肌醇3激酶(phosphatidylinositol 3 kinase,PI3K)、蛋白激酶B(protein kinase B,AKT)、p-AKT、Foxo3a及甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)单克隆抗体(美国Epitmics公司);辣根过氧化物酶标记山羊抗兔IgG(H+L)、细胞计数试剂盒-8(Cell Counting Kit-8,CCK-8) 试剂盒、annexin V/propidium iodide流式双染试剂盒、细胞周期检测试剂盒(上海碧云天生物技术研究所);胎牛血清、改良杜氏伊格尔培养基(Dulbeccos modified Eagle medium, DMEM)培养基、胰蛋白酶(美国Gbico公司);miR-155 inhibitor及阴性对照(miR-155 NC)(上海吉玛生物有限公司);trizol试剂盒、一步法RT-PCR试剂盒、Lipofectamine 2000(大连宝生生物技术有限公司)。FACSCalibur型流式细胞仪(美国BD公司);迷你双垂直电泳仪、迷你转印电泳仪、ChemiDocTM XRS凝胶成像系统(美国Bio-Rad公司)。
1.2 miRNA转染无血清Opti-MEM® I培养基稀释miR-155 NC、miR-155 inhibitor及Lipofectamine 2000,将两者混匀,室温孵育20~30 min;将miRNA/Lipofectamine 2000复合物加入6孔板培养;6 h以后换成含10%血清的DMEM培养基,并用realtime-PCR检测miR-155的表达。
1.3 miR-155表达检测采用realtime-PCR法,将1×104个Hep2细胞接种于6孔板,转染48 h后,收集细胞;根据trizol试剂盒说明书提取总RNA,采用微量紫外分光光度计检测RNA纯度,通过一步法RT-PCR试剂盒逆转录RNA,进行realtime-PCR扩增,扩增结果利用2-ΔΔCT法进行分析。miR-155上游引物:5′-TAATGCTAATCGTGATAGGG-3′,下游:5′-TTTGGCACTAGCACATT-3′,GAPDH上游引物:5′-AGCCACATCGCTCAGACA-3′,下游:5′-TGGACTCCACGACGTACT-3′;每组设3个平行孔。
1.4 指标与方法 1.4.1 细胞活力检测采用CCK-8法,将5×103个Hep2细胞接种于96孔板,分别转染12、24、36、48、60、72 h后,加入CCK-8,继续培养4 h后,于酶标仪570 nm处测吸光度(A)值,代表细胞活力。
1.4.2 细胞凋亡检测采用annexin V/PI流式双染法,将1×104个Hep2细胞接种于6孔板,转染48 h后,收集细胞,按顺序分别加入结合液,annexin V及碘化丙啶,于1 h内在流式细胞仪上检测细胞凋亡情况。
1.4.3 细胞周期检测采用流式细胞术,将1×104个Hep2细胞接种于6孔板,转染48 h后,收集细胞,加入5 μL终浓度为10 mg/mL的Rnase,37 ℃孵育1 h,再加入碘化丙啶染液,室温下避光染色30 min,用流式细胞仪进行细胞周期检测。
1.4.4 PI3K/AKT/Foxo3a信号通路相关蛋白表达检测采用Western blot法,将1×104个Hep2细胞接种于6孔板,转染48 h后,收集细胞,加入细胞裂解液裂解30 min,离心,小心吸取上清,即可获得总蛋白。根据试剂盒法测定蛋白浓度;蛋白变性,上样,进行十二烷基苯磺酸钠凝胶电泳,湿法转膜30~50 min;一抗溶液(兔抗cyclinA1、cyclinD1、PI3K、AKT、p-AKT、Foxo3a及GAPDH单克隆抗体),稀释度为1:100) 孵育,4 ℃过夜;次日二抗溶液室温孵育1~2 h;在凝胶成像系统中曝光,用Quantity one软件分析各抗体条带灰度值。
1.5 统计分析数据用x±s表示,采用SPSS 17.0软件进行统计分析,组间比较采用t检验,以P<0.05为差异有统计学意义。
2 结果 2.1 miR-155 inhibitor在Hep2细胞中转染效果Realtime-PCR结果显示,miR-155 NC组与miR-155 inhibitor组Hep2细胞中miR-155表达量分别为(1.25±0.10)、(0.34±0.03);与miR-155 NC组比较,miR-155 inhibitor组Hep2细胞中miR-155表达量明显下降,差异有统计学意义(P<0.01)。提示,Hep2细胞转染miR-155 inhibitor成功。
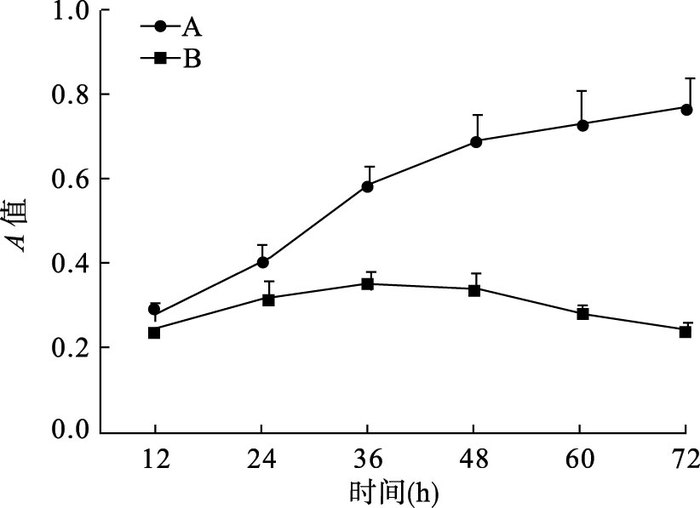
2.2 miR-155 inhibitor对Hep2细胞活力影响(图 1)Hep2细胞转染miR-155 NC及miR-155 inhibitor 24 h后,与miR-155 NC组比较,miR-155 inhibitor组Hep2细胞活力明显降低,差异有统计学意义(P<0.01)。
|
注:A:miR-155 NC组;B:miR-155 inhibitor组;与miR-155 NC组比较,a P<0.01。 图 1 miR-155 inhibitor对Hep2细胞活力影响(CCK-8) |
2.3 miR-155 inhibitor对Hep2细胞凋亡影响(图 2)
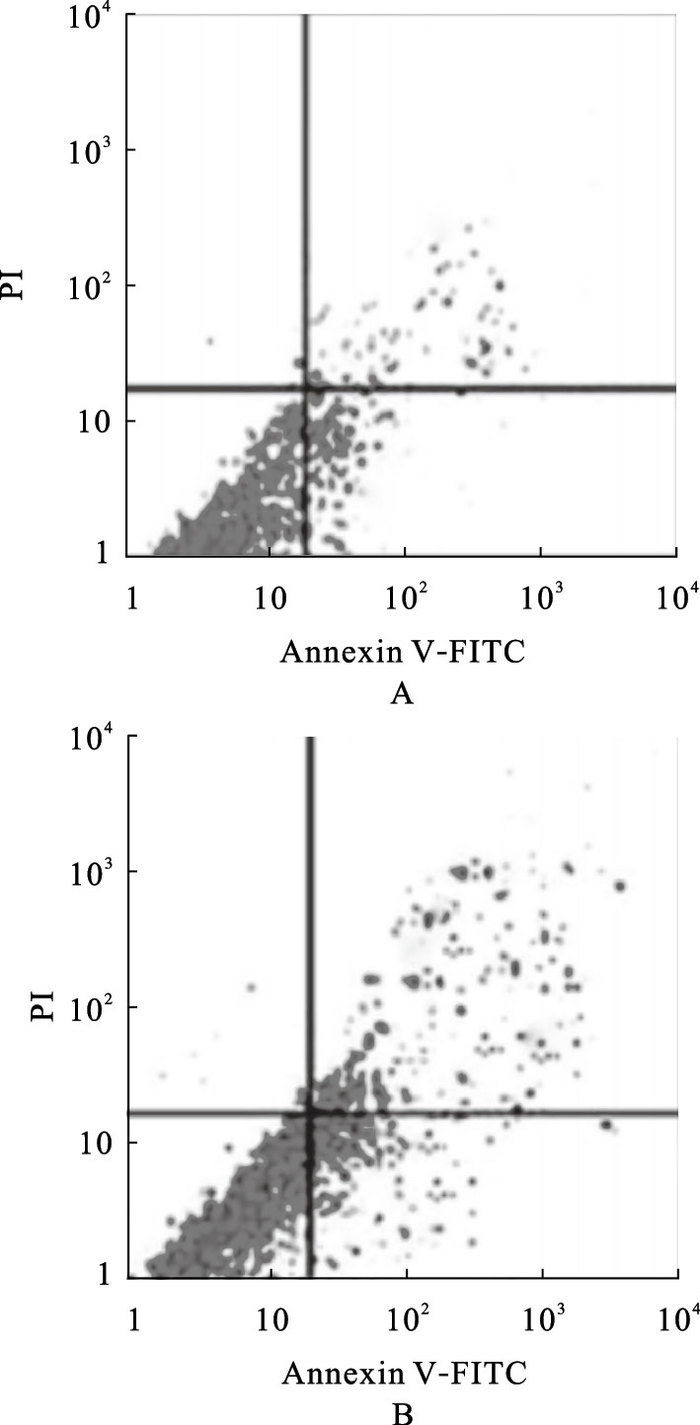
结果显示,miR-155 NC组Hep2细胞早期、晚期凋亡率分别为(3.49±0.38)%、(5.84±0.58)%,miR-155 inhibitor组Hep2细胞早期、晚期凋亡率分别为(12.43±1.20)%、(18.96±1.85)%;与miR-155 NC组比较,miR-155 inhibitor组Hep2细胞早、晚期凋亡率均明显升高,差异均有统计学意义(均P<0.01)。
|
注:A:miR-155 NC组;B:miR-155 inhibitor组。 图 2 miR-155 inhibitor对Hep2细胞凋亡影响 |
2.4 miR-155 inhibitor对Hep2细胞周期影响(表 1)
与miR-155 NC组比较,miR-155 inhibitor组Hep2细胞G1期比例明显增加,差异有统计学意义(P<0.01)。提示,miR-155 inhibitor组Hep2细胞周期阻滞在G1期。
| 表 1 miR-155 inhibitor对Hep2细胞周期影响(x±s,n=3) |
2.5 miR-155 inhibitor对Hep2细胞中周期蛋白表达影响(图 3)
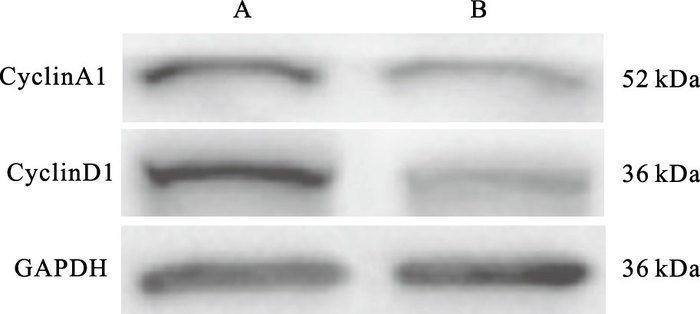
miR-155 NC组Hep2细胞中cyclinA1与cyclinD1表达量分别为(0.47±0.05)、(0.88±0.10),miR-155 inhibitor组Hep2细胞中cyclinA1与cyclinD1表达量分别为(0.18±0.02)、(0.17±0.02);与miR-155 NC组比较,miR-155 inhibitor组Hep2细胞中cyclinA1及cyclinD1表达量下调,差异均有统计学意义(均P<0.01)。
|
注:A:miR-155 NC组;B:miR-155 inhibitor组。 图 3 miR-155 inhibitor对Hep2细胞周期蛋白表达影响 |
2.6 miR-21对Hep2细胞中PI3K/AKT/Foxo3信号通路影响(图 4、表 2)
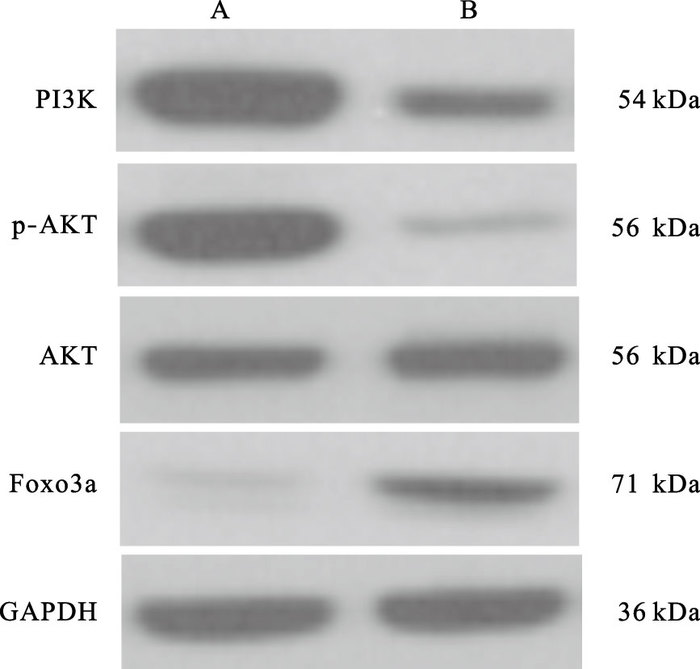
与miR-155 NC组比较,miR-155 inhibitor组Hep2细胞中PI3K、p-AKT表达量下调,Foxo3a表达量上调,差异均有统计学意义(均P<0.01)。
|
注:A:miR-155 NC组;B:miR-155 inhibitor组。 图 4 miR-155 inhibitor对Hep2细胞中PI3K/AKT/Foxo3a信号通路影响 |
| 表 2 miR-155 inhibitor对Hep2细胞PI3K/AKT/Foxo3a信号通路相关蛋白表达影响(x±s,n=3) |
3 讨论
miRNA是一类真核生物中高度保守的非编码RNA分子,通过与靶基因的3'-非翻译区特异性结合,降解靶基因或者抑制靶基因转录,从而调控细胞增殖、凋亡、细胞周期、迁移、侵袭等生物学行为[4-6]。自1993年Lee等在线虫中发现了第1个miRNA(lin-4) 后,2002年Groce也首次报道了miRNA与肿瘤的关系,即在慢性淋巴细胞白血病中miR-15及miR-16表达下调或缺失。后续miRNA与肿瘤的关系引起了广泛兴趣。研究显示头颈部肿瘤组织拥有自己独特的miRNA表达特征及其靶基因,可通过这些miRNA及其靶基因的调控,进而为肿瘤诊断、治疗及预后提供理论依据[10-11]。其中miR-155是一种常见的在多种肿瘤组织中被认为癌基因的miRNA,位于人染色体21q21,是由癌基因-B细胞整合簇(BIC)基因编码产生的,能通过介导Foxo3a、RhoA等多种靶基因表达参与造血干细胞、骨髓干细胞、炎症反应、免疫反应及肿瘤的发生发展过程[7-9]。miR-155在包括LSCC在内的多种肿瘤组织中高表达,如Wang等[12]利用RT-PCR法检测280例LSCC患者及560名年龄、性别相匹配的健康对照,结果表明LSCC组织中miR-155远高于健康对照,曲线下面积(area under the curve, AUC)为0.933,敏感度为82.6%,特异性为89.2%,而且LSCC患者血浆中miR-155表达量也显著高于健康对照,AUC为0.757,敏感度为58.4%,特异性为69.5%。研究还表明miR-155 inhibitor能明显抑制Hep2细胞增殖与迁移,并诱导细胞凋亡[13]。
本研究利用脂质体转染miR-155 inhibitor及miR-155 NC,并采用realtim PCR检测转染效果,结果表明miR-155 inhibitor可明显下调Hep2细胞中miR-155表达,表明miR-155 inhibitor转染成功。本研究结果显示,在转染24、36、48、60、72 h后,miR-155 inhibitor组Hep2细胞活力降低,细胞凋亡率明显增加,与王洋等[13]研究结果一致。提示,miR-155 inhibitor对Hep2细胞活力具有抑制作用,对于细胞的凋亡具有诱导作用。肿瘤细胞的无限增殖来源于细胞周期的不可控制,通过调控细胞周期可一定程度的遏制肿瘤细胞的无限生长。而且细胞周期调控点是常见的抗肿瘤药物靶点,如G1期、G2期等[14-15]。CyclinA1、cyclinD1是与G1期密切相关的细胞周期蛋白,其表达量上调,能加速G1进入S期,进而促进细胞的复制与分裂。本研究结果表明miR-155 inhibitor转染可使Hep2细胞周期阻滞在G1期,并下调cyclinA1、cyclinD1表达,进而遏制Hep2细胞的增殖。
细胞的增殖与凋亡受到多种信号通路调控,PI3K/AKT信号通路则是其中一种,在众多信号通路中发挥着重要作用,参与细胞增殖、凋亡、细胞周期、能量代谢、基因转录等生物学过程[16-17]。在恶性肿瘤组织中PI3K/AKT信号通路被异常激活,反过来促进恶性肿瘤的发展,因而抑制PI3K/AKT信号通路能够促使肿瘤细胞的生长增殖受到抑制并发生程序性死亡[16-17]。当PI3K受外部信号刺激后,将信号传递给AKT,磷酸化的AKT转入细胞核,下调下游多种细胞因子表达,Foxo3a则是其中一种。Foxo3a是叉头转录因子家族的一员,具有鲜明的叉头DNA结合域,能被AKT、血清和糖皮质激素调节蛋白激酶(serum and glucocorticoid-inducible kinase SGK)等蛋白激酶激活,后转入细胞质中,进而失去对细胞凋亡调控的能力。同时Foxo3a亦是miR-55的下游靶基因之一,miR-155对PI3K/AKT信号通路同样具有调控作用[18-20]。本研究结果表明miR-155 inhibitor转染可明显下调PI3K、p-AKT表达,上调Foxo3a蛋白表达。提示,miR-155 inhibitor转染对Hep2细胞增殖具有抑制作用、对细胞凋亡具有促进作用,其机制可能与miR-155表达下调抑制PI3K/AKT信号通路、上调Foxo3a表达有关。
| [1] | 汤玮晶, 陶磊. 喉癌患者术后生存质量的研究进展[J]. 中国眼耳鼻喉科杂志, 2014, 14(2): 124–126. |
| [2] | 王蓓蕾, 徐立红, 袁晖, 等. 喉癌相关基因的研究进展[J]. 中国细胞生物学学报, 2014, 36(9): 1323–1330. |
| [3] | 朱奕, 王胜资. 吸烟相关性喉癌发生机制的研究进展[J]. 中国眼耳鼻喉科杂志, 2015, 15(3): 213–215. |
| [4] | Cybula M, Józefowicz W, Korczyńska M, et al. New miRNA expression abnormalities in laryngeal squamous cell carcinoma[J]. Cancer Biomark, 2016, 16(4): 559–568. DOI:10.3233/CBM-160598 |
| [5] | Zhang Y, Chen Y, Yu J, et al. Integrated transcriptome analysis reveals miRNA-mRNA crosstalk in laryngeal squamous cell carcinoma[J]. Genomics, 2014, 104(4): 249–256. DOI:10.1016/j.ygeno.2014.06.004 |
| [6] | 吴一波, 沈志森, 余星, 等. 喉癌相关miRNA的研究进展[J]. 基础医学与临床, 2012, 32(5): 583–586. |
| [7] | Jurkovicova D, Magyerkova M, Kulcsar L, et al. miR-155 as a diagnostic and prognostic marker in hematological and solid malignancies[J]. Neoplasma, 2014, 61(3): 241–251. DOI:10.4149/neo_2014_032 |
| [8] | Seddiki N, Brezar V, Ruffin N, et al. Role of miR-155 in the regulation of lymphocyte immune function and disease[J]. Immunology, 2014, 142(1): 32–38. DOI:10.1111/imm.2014.142.issue-1 |
| [9] | 蔡婷婷, 王菊勇, 杜志华, 等. microRNA-155与恶性肿瘤的研究进展[J]. 现代肿瘤医学, 2016, 24(14): 2314–2318. DOI:10.3969/j.issn.1672-4992.2016.14.043 |
| [10] | Hudcova K, Trnkova L, Kejnovska I, et al. Novel biophysical determination of miRNAs related to prostate and head and neck cancers[J]. Eur Biophys J, 2015, 44(3): 131–138. DOI:10.1007/s00249-015-1008-y |
| [11] | Salazar C, Nagadia R, Pandit P, et al. A novel saliva-based microRNA biomarker panel to detect head and neck cancers[J]. Cell Oncol (Dordr), 2014, 37(5): 331–338. |
| [12] | Wang JL, Wang X, Yang D, et al. The Expression of microRNA-155 in plasma and tissue is matched in human laryngeal squamous cell carcinoma[J]. Yonsei Med J, 2016, 57(2): 298–305. DOI:10.3349/ymj.2016.57.2.298 |
| [13] | 王洋, 王斌全, 高伟, 等. MicroRNA-155对喉鳞状细胞癌Hep-2细胞株的作用[J]. 中国耳鼻咽喉头颈外科, 2013, 20(6): 285–289. |
| [14] | Vermeulen K, Van Bockstaele DR, Berneman ZN. The cell cycle:a review of regulation, deregulation and therapeutic targets in cancer[J]. Cell Prolif, 2003, 36(3): 131–149. DOI:10.1046/j.1365-2184.2003.00266.x |
| [15] | 李煜, 孔祥文, 楼永军, 等. 癌症研究与临床治疗中的CDK抑制剂[J]. 中国现代应用药学, 2014, 31(9): 1147–1154. |
| [16] | Zhao HF, Wang J, Tony TS. The phosphatidylinositol 3-kinase/Akt and c-Jun N-terminal kinase signaling in cancer:alliance or contradiction? (Review)[J]. Int J Oncol, 2015, 47(2): 429–436. |
| [17] | Toren P, Zoubeidi A. Targeting the PI3K/Akt pathway in prostate cancer:challenges and opportunities (review)[J]. Int J Oncol, 2014, 45(5): 1793–1801. |
| [18] | Zhuang Z, Qin X, Hu H, et al. Down-regulation of microRNA-155 attenuates retinal neovascularization via the PI3K/Akt pathway[J]. Mol Vis, 2015, 21: 1173–1184. |
| [19] | Min M, Peng L, Yang Y, et al. MicroRNA-155 is involved in the pathogenesis of ulcerative colitis by targeting FOXO3a[J]. Inflamm Bowel Dis, 2014, 20(4): 652–659. DOI:10.1097/MIB.0000000000000009 |
| [20] | Ling N, Gu J, Lei Z, et al. microRNA-155 regulates cell proliferation and invasion by targeting FOXO3a in glioma[J]. Oncol Rep, 2013, 30(5): 2111–2118. |
 2017, Vol. 33
2017, Vol. 33
