急性心肌梗死(acute myocardial infarction,AMI)是常见的冠心病之一,主要是由于心肌极度的缺血诱导急性血栓的产生,从而引起血管的闭塞,是中老年人常见的心血管疾病之一,严重者会引起心肌重构甚至心力衰竭[1]。目前AMI的发病机制尚不清楚,但已有研究表明,AMI所引起的心肌细胞凋亡是心肌梗死后所导致的心室重构及心力衰竭的主要原因之一,抑制心肌细胞凋亡对于AMI的发展具有显著的阻断作用[2]。miRNAs是一类具有18-23 nt氨基酸的在进化上高度保守的非编码RNA分子,能与下游靶基因的3′UTR端结合,进而降解靶基因或者调控靶基因的转录,从而调控细胞的生长、分化、增殖、凋亡、迁移等生物学行为[3]。以往研究表明,miRNA能特异性表达于心肌细胞中,与心肌梗死、心肌肥大、心力衰竭、心律失常及心肌重塑等多种心血管疾病密切相关[2, 4-5]。还有研究表明,miR-221在AMI患者心肌组织中高表达,但具体作用机制未知[6-8]。本研究通过建立AMI大鼠模型观察miR-221在AMI大鼠中的表达水平,旨在探讨miR-221对AMI的作用机制。
1 材料与方法 1.1 主要试剂与仪器兔抗Bax (B-cell lymphoma 2-associated X protein)、Bcl-2(B-cellymphoma-2)、PI3K(phosphoinositide 3-OH kinase)、AKT(protein kinase B)、p-AKT(phosphorylated protein kinase B)、GAPDH(glyceraldehyde-3-phosphate dehydrogenase)单克隆抗体(美国Epitmics公司),辣根过氧化物酶标记山羊抗兔IgG(H+L)、BCA试剂盒(上海碧云天生物技术研究所),trizol试剂盒、一步法逆转录-聚合酶链反应(reverse transcription polymerase chain reaction, RT-PCR)试剂盒(美国Invitrogen公司);miR-221 inhibitor(5′-GAAACCCAGCAGACAAUGUAGCU-3′)及miR-221阴性对照(5′-CGAACGUGUCACGUTT-3′)由广州市锐博生物科技有限公司合成;迷你双垂直电泳仪、迷你转印电泳仪(北京六一仪器厂),ChemiDocTM XRS凝胶成像系统(美国Bio-Rad公司),Tecan Infinite F200型多功能酶标仪(瑞士TECAN集团公司),DMI 4000B荧光显微镜(德国Leica公司)。
1.2 实验动物Sprague-Dawley(SD)清洁级雄性大鼠45只,体重(200±20) g,购于上海斯莱克实验动物有限责任公司,动物许可证号:SCXK(沪)2012-0002。在清洁环境下饲养观察,室内温度控制在(23±2)℃,大鼠自由饮食和摄水。
1.3 分组与处理在45只大鼠中随机抽取35只大鼠通过冠状动脉左前降支结扎大鼠建立AMI模型,通过观察心电图记录仪,发现ST段背向上抬高、心律较为缓慢、左心室变白,说明AMI建模成功[2],将其中建模成功的30只大鼠随机分为AMI组、对照组及抑制组,每组各10只,另抽取未建模的10只大鼠设立假手术组采用冠状动脉左前降支穿线不结扎。其中,对照组用携带绿色荧光蛋白(green fluorescent protein,GFP)的慢病毒空载体miR-221阴性对照以4×107病毒数量进行心肌组织局部注射转染,抑制组用携带miR-221 inhibitor慢病毒以4×107病毒数量进行心肌组织局部注射转染,AMI组和假手术组每天给予等量生理盐水,隔日1次连续2周。
1.4 心脏功能检测大鼠治疗2周后,腹腔注射10%水合氯醛进行麻醉,对大鼠行心脏彩超检查并记录左室射血分数(left ventricular ejection fraction,LVEF)、左室长轴缩短分数(left ventricular long axis shortening fraction,FS)、左室舒张末期内径(left ventricular end diastolic diameter,LVDd)、左室收缩末期内径(left ventricular end systolic diameter,LVDs)等相关指标。
1.5 TUNEL(TdT-mediated dUTP-biotin nick end-labeling)法检测心肌凋亡指数(apoptosis index, AI)取大鼠心肌组织,石蜡包埋,切片,磷酸盐缓冲液(phosphate buffer saline,PBS)洗涤,细胞通透液Triton X通透,PBS洗涤,加入TUNEL反应液,于室温下避光孵育60 min,PBS洗涤,加二脒基苯基吲哚[2-(4-amidinophenyl)-6-indolecarbamidine dihydrochloride, DAPI]染色,封片,200倍光镜下观察细胞凋亡情况,凋亡细胞呈棕黄色,AI=(凋亡细胞数/细胞总数)×100%。
1.6 RT-PCR检测miR-221表达量采用trizol试剂盒提取心肌组织中的总RNA,并检测RNA纯度;采用一步法RT-PCR试剂盒将RNA逆转录,同时进行PCR扩增,将扩增产物用于2%琼脂糖凝胶电泳。引物设计如下:miR-221上游引物:5′-GGGCATGAACCTGGCATAC-3′,下游引物:5′-AGGTAGCCTGAAACCCAGCA-3′;磷酸甘油醛脱氢酶(GAPDH)上游引物:5′-AGCCACATCGCTCAGACA-3′,下游引物:5′-TGGACTCCACGACGTACT-3′。引物分别加入25 μL的聚合酶链反应(polymerase chain reaction, PCR)体系中,反应条件为94 ℃变性45 s,59 ℃复性45 s,72℃延伸60 s,共35个循环。
1.7 Western blot检测Bax、Bcl-2、PI3K、p-AKT蛋白表达取大鼠适量心肌组织匀浆并离心,加入细胞裂解液裂解30 min,离心获得上清液,即蛋白样品;采用BCA试剂盒检测蛋白浓度。蛋白样品煮沸变性10 min上样,进行十二烷基苯磺酸钠凝胶电泳1~2 h,转膜30~40 min,5%脱脂奶粉封闭1 h,一抗溶液(兔抗Bax、Bcl-2、PI3K、AKT、p-AKT、GAPDH单克隆抗体,稀释度皆为1: 100)4℃孵育过夜。次日二抗溶液[辣根过氧化物酶标记山羊抗兔IgG(H+L), 稀释度为1:200]室温孵育1 h,滴加化学曝光液,于凝胶成像系统中曝光。
1.8 统计分析数据均以x±s表示,应用SPSS 17.0软件进行统计分析,多组间比较采用单因素方差分析,两两比较采用t检验,以P < 0.05为差异有统计学意义。
2 结果 2.1 不同组别大鼠心肌中miR-221表达(图 1)
|
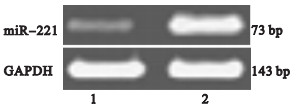
注:1:假手术组;2:AMI造模成功组。 图 1 不同组别大鼠心肌中miR-221表达 |
与假手术组大鼠miR-221表达量(0.18±0.02) 比较,AMI造模成功组大鼠miR-221表达量(1.10±0.12) 明显升高,差异有统计学意义(P < 0.01)。
2.2 miR-221 inhibitor对AMI大鼠心肌中miR-221表达量影响(图 2)

|
注:1:假手术组;2:AMI组;3:对照组;4:抑制组。 图 2 miR-221 inhibitor对AMI大鼠心肌中miR-221表达量影响 |
与假手术组大鼠miR-221表达量(0.18±0.02) 比较,AMI组(1.16±0.12) 和对照组(1.18±0.12) 大鼠的miR-221表达量均升高,差异均有统计学意义(均P < 0.01);抑制组大鼠miR-221表达量(0.30±0.03) 均低于AMI组和对照组大鼠的miR-221表达量,差异均有统计学意义(均P < 0.01)。
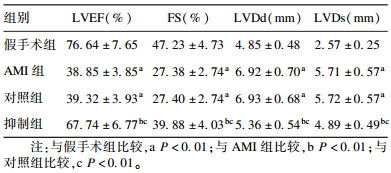
2.3 miR-221 inhibitor对AMI大鼠心脏功能影响(表 1)| 表 1 miR-221对AMI大鼠心脏功能影响(x±s,n=40) |
与假手术组大鼠比较,AMI组和对照组大鼠LVEF和FS均降低,LVDd和LVDs均升高,差异均有统计学意义(均P < 0.01);与AMI组和对照组大鼠比较,抑制组大鼠LVEF和FS均升高,LVDd和LVDs均降低,差异均有统计学意义(P < 0.01)。
2.4 miR-221 inhibitor对AMI大鼠心肌AI影响与假手术组大鼠心肌AI[(2.33±0.22)%]比较,AMI组[(37.36±3.74)%]和对照组[(37.34±3.72)%]大鼠的心肌AI均升高,差异均有统计学意义(均P < 0.01);抑制组大鼠心肌AI[(6.48±0.65)%]和均低于AMI组和对照组大鼠的心肌AI,差异均有统计学意义(均P < 0.01)。
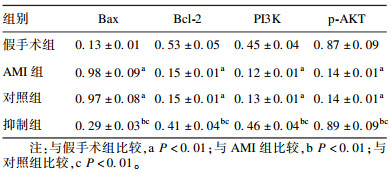
2.5 miR-22对AMI大鼠心肌组织中Bax、Bcl-2、PI3K、p-AKT蛋白表达量影响(表 2)| 表 2 miR-221对AMI大鼠心肌组织中Bax、Bcl-2、PI3K、p-AKT蛋白表达量影响(x±s,n=40) |
与假手术组大鼠比较,AMI组和对照组大鼠Bax蛋白表达量均上调,Bcl-2、PI3K和p-AKT蛋白表达量均下调,差异均有统计学意义(P < 0.01);与AMI组和对照组大鼠比较,抑制组大鼠Bax蛋白表达量均下调,Bcl-2、PI3K和p-AKT蛋白表达量均上调(P < 0.01)。
3 讨论miRNA是一类长度约为18~25 nt高度保守的小RNA,可通过与其靶基因的3′-UTR区域结合调控基因的转录水平,进而调控细胞的生长、增殖、分化、凋亡等生物学行为,从而参与机体的发育、代谢及众多疾病的发生发展[3]。以往对miRNA的研究主要集中于机体的发育情况及肿瘤的发生发展过程中,近些年miRNA在心肌梗死、心力衰竭、心律失常等心血管疾病中的重要作用日益受到关注[9-10]。miR-221是从斑马鱼中发现并克隆的miRNA,此后又在白血病细胞株HL-60中克隆获得。miR-221与miR-222同源,位于染色体p11.3区。现有研究表明miR-221在乳腺癌、胃癌、肺癌、肝癌等肿瘤组织中高表达,因此miR-221被认为是一种抑癌miRNA被进一步的深入研究[11-12]。Coskunpinar等[7]研究证实心肌梗死患者血液中多种循环miRNA表达量升高或者降低,其中循环miR-221表达量最高,为假手术组的3.89倍,且与心肌损伤标志物超敏心肌肌钙蛋白T及GARCE、SYNTAX评分密切相关,提示循环miR-221是心肌梗死早期诊断新的标记物。另有研究也证实miR-221在心力衰竭大鼠心肌组织中高表达[6]。但miR-221在心肌梗死及心力衰竭过程中的作用机制尚不清楚,因此本研究将在此基础上进一步探讨miR-221在AMI大鼠心肌组织中的表达及其作用机制。首先本研究采用冠状动脉左前降支结扎构建AMI模型,并应用RT-PCR法检测大鼠心肌组织中miRGARCE221的表达,结果显示AMI造模成功组大鼠心肌组织中miRGARCE221表达量高于假手术组大鼠,与Coskunpinar等[7]研究结果一致。接着采用心肌组织局部注射慢病毒转染的miRGARCE221阴性对照和miRGARCE221 inhibitor,并应用RTGARCEPCR法证实了miRGARCE221 inhibitor转染的成功,结果显示miRGARCE221 inhibitor能明显下调AMI组和对照组大鼠miRGARCE221的表达量。进一步检测miRGARCE221 inhibitor对大鼠心脏功能的影响,结果显示miR-221 inhibitor能明显升高LVEF和FS,降低LVDd和LVDs,提示miR-221能通过改善大鼠心脏功能进而抑制AMI的损伤。同时还利用TUNEL法检测了miRGARCE221 inhibitor对大鼠心肌细胞凋亡的影响,结果显示miR-221 inhibitor能明显降低AMI组合对照组大鼠的心肌AI。
细胞的凋亡受众多信号通路调控,PI3K/AKT信号通路就是其中一种,其具有抗凋亡通路之称,能通过调控下游多种靶蛋白如Bax和Bcl-2的表达,从而参与调控细胞生长、凋亡、分化、迁移、侵袭及血管生成等过程[13-14]。在心肌梗死大鼠中PI3K/AKT信号通路失活,当激活此信号通路后能明显抑制大鼠心肌功能紊乱及心肌细胞凋亡[15]。同时研究表明miR-221对PI3K/AKT信号通路具有明显的调控作用,同时能够调控下游蛋白Bax及Bcl-2的表达[16-17]。本研究结果显示,miR-221 inhibitor能明显下调AMI组和对照组大鼠的Bax蛋白表达量,上调Bcl-2、PI3K和P-AKT蛋白表达量,提示miR-221 inhibitor能通过激活PI3K/AKT信号通路抑制AMI大鼠心肌细胞的凋亡。
综上所述,miR-221在AMI大鼠心肌组织中高表达,下调miR-221表达可通过激活PI3K/AKT信号通路调控下游蛋白Bax和Bcl-2的表达量,从而抑制AMI大鼠心肌细胞的凋亡。
| [1] | 张力俨, 张翠丽, 富路. 急性心肌梗死药物治疗研究进展[J]. 心血管病学进展, 2011, 32(2): 212–216. |
| [2] | 高威, 钟锋. miR-126对急性心肌梗死大鼠心肌细胞凋亡的影响[J]. 中国比较医学杂志, 2016, 26(7): 57–63. |
| [3] | 周世权, 张艳炜, 董秋实, 等. miRNA与心脑血管病研究进展[J]. 中国公共卫生, 2014, 30(3): 378–380. DOI:10.11847/zgggws2014-30-03-40 |
| [4] | Gambari R, Brognara E, Spandidos DA, et al. Targeting oncomiRNAs and mimicking tumor suppressor miRNAs:new trends in the development of miRNA therapeutic strategies in oncology (review)[J]. Int J Oncol, 2016, 49(1): 5–32. |
| [5] | Nouraee N, Mowla SJ. miRNA therapeutics in cardiovascular diseases:promises and problems[J]. Front Genet, 2015, 6: 232. |
| [6] | Souza RW, Fernandez GJ, Cunha JP, et al. Regulation of cardiac microRNAs induced by aerobic exercise training during heart failure[J]. Am J Physiol Heart Circ Physiol, 2015, 309(10): H1629–1641. |
| [7] | Coskunpinar E, Cakmak HA, Kalkan AK, et al. Circulating miR-221-3p as a novel marker for early prediction of acute myocardial infarction[J]. Gene, 2016, 591(1): 90–96. DOI:10.1016/j.gene.2016.06.059 |
| [8] | Costantino S, Paneni F, Luscher TF, et al. MicroRNA profiling unveils hyperglycaemic memory in the diabetic heart[J]. Eur Heart J, 2016, 37(6): 572–576. DOI:10.1093/eurheartj/ehv599 |
| [9] | Sayed AS, Xia K, Salma U, et al. Diagnosis, prognosis and therapeutic role of circulating miRNAs in cardiovascular diseases[J]. Heart Lung Circ, 2014, 23(6): 503–510. DOI:10.1016/j.hlc.2014.01.001 |
| [10] | 陶瑾, 李素芳, 徐明. MicroRNA:新的心血管疾病生物标志物[J]. 生理科学进展, 2011, 42(5): 335–339. |
| [11] | 程文婷, 傅奕. miR-221的研究进展[J]. 现代肿瘤医学, 2016, 24(3): 473–475. |
| [12] | 邢慧慧, 刘晓峰, 刘长江, 等. miR-221在肿瘤中的研究进展[J]. 医学研究杂志, 2014, 43(8): 14–16. |
| [13] | Yuan MJ, Huang H, Huang CX. Potential new role of the GHSR-1a-mediated signaling pathway in cardiac remodeling after myocardial infarction (review)[J]. Oncol Lett, 2014, 8(3): 969–971. |
| [14] | 陈晨, 殷园园, 武夏芳, 等. 活性氧通过MAPKs和PI3K/AKT通路激活Nrf2研究进展[J]. 中国公共卫生, 2016, 32(6): 870–873. DOI:10.11847/zgggws2016-32-06-41 |
| [15] | Lu C, Wang X, Ha T, et al. Attenuation of cardiac dysfunction and remodeling of myocardial infarction by microRNA-130a are mediated by suppression of PTEN and activation of PI3K dependent signaling[J]. J Mol Cell Cardiol, 2015, 89(Pt A): 87–97. |
| [16] | Xu H, Gu LN, Yang QY, et al. MiR-221 promotes IgE-mediated activation of mast cells degranulation by PI3K/Akt/PLCgamma/Ca(2+) pathway[J]. J Bioenerg Biomembr, 2016, 48(3): 293–299. DOI:10.1007/s10863-016-9659-7 |
| [17] | Ye Z, Hao R, Cai Y, et al. Knockdown of miR-221 promotes the cisplatin-inducing apoptosis by targeting the BIM-Bax/Bak axis in breast cancer[J]. Tumour Biol, 2016, 37(4): 4509–4515. DOI:10.1007/s13277-015-4267-4 |
 2017, Vol. 33
2017, Vol. 33