2. 牡丹江医学院基础医学院
组织器官(肝脏、肾脏、心肌组织等)纤维化引起的器官功能衰竭,已成为危害人类健康的重要原因之一,而人转化生长因子β1(transforming growth factor beta 1,TGF-β1) 在纤维化发生发展中起重要作用[1]。在哺乳动物中,已经克隆出3种TGF-β,分别为TGF-β1、TGF-β2和TGF-β3。虽然它们在体外显示类似的功能,但在纤维化的发生发展中,多由于TGF-β1的过量表达引起细胞外基质(extracelluar matrix,ECM)和胶原蛋白的过度产生、沉积而引起纤维化,因此TGF-β1被认为是器官纤维化的一个关键环节。TGF-β1的生物学功能是通过与其细胞膜上的受体相结合来实现的,其受体包括转化生长因子Ⅰ、Ⅱ、Ⅲ型受体(TβRⅠ、TβRⅡ、TβRⅢ)。TGF-β1首先与TβRⅡ结合,使其二聚化,二聚化的TβRⅡ可使TβRⅠ转磷酸化,引起TGF-β/Smads和非TGF-β/Smads信号转导[2]而调控基因转录。因此,TβRⅡ对于TGF-β1的生物活性是必须的[3-4]。酵母双杂交技术广泛用于检测蛋白质-蛋白相互作用[5-7],用于酵母双杂交系统检测的蛋白质,分别与含有DNA结合结构域酵母双杂交诱饵载体(pGBKT7) 或转录因子的激活结构域酵母双杂交激活载体(pGADT7) 结合,这2种蛋白质的相互作用带来AD(activating domain)和BD(binding domain)结构域共同激活下游的转录基因。本研究从人血液提取RNA,逆转录为cDNA,PCR扩增TGF-β1基因和4个截短型TβRⅡ(TβRⅡ-A、TβRⅡ-B、TβRⅡ-C、TβRⅡ-D),将其分别插入到pGBKT7和pGADT7中,旨在为下一步应用酵母双杂交筛选与TGF-β1相互作用的TβRⅡ的区域提供技术支撑。
1 材料与方法 1.1 主要试剂酵母双杂交载体pGADT7、pGBKT7、大肠杆菌感受态细胞(DH5α)(牡丹江医学院医药研究中心);质粒小提试剂盒、琼脂糖凝胶DNA回收试剂盒(天根生化科技北京有限公司);TRizol® LS Reagent(上海拜力生物科技有限公司);2×Es Taq MasterMix(Dye)(北京康为世纪公司);10×PCR Buffer for KOD-Plus-Neo、2 mM dNTPs、25 mM MgSO4、KOD-Plus-Neo(日本东洋纺公司);Nde I、Bam HI、EcoR I、T4 DNA连接酶、10×T4 DNA连接Buffer(宝生物工程大连有限公司),Transcriptor First Strand cDNA Synthesis Kit(罗氏诊断产品上海有限公司);引物由生工生物工程(上海)股份有限公司合成。
1.2 RNA提取和逆转录人新鲜血液RNA抽提,每0.25 mL血液样品中加入0.75 mL Trizol® LS,混匀;参照TRizol® LS试剂说明书进行样品分离、RNA沉淀、RNA洗涤和悬浮。用紫外分光光度计测量RNA浓度及纯度。RNA样本用Transcriptor First Strand cDNA Synthesis Kit进行逆转录:RNA 1 μg、anchored-oligo[dT]18 Primer 1 μL、random hexamer primer 2 μL、用水补至13 μL,混匀,65 ℃、10 min,冰上2 min,向混合液中加入5×transcriptor RT reaction buffer 4 μL,protector RNase inhibitor 0.5 μL,deoxynucleotide mix 2 μL,transcriptor reverse transcriptase 0.5 μL;逆转录条件为:25 ℃、10 min,50 ℃、1 h,85 ℃、5 min,4 ℃、1 h。
1.3 TGF-β1基因和4种受体基因片段扩增利用引物设计软件设计引物(表 1),以RT产物cDNA为模板,分别以F11 & R22、F1 & R1、F2 & R1、F3 & R1、F4 & R1为引物,PCR扩增TGF-β1基因和TβRⅡ-A, TβRⅡ-B, TβRⅡ-C和TβRⅡ-D基因片段。PCR反应条件:95 ℃预变性5 min,每个循环95 ℃、30 s,55 ℃、30 s,72 ℃、1 min 30 s/50 s,共35个循环,最后72 ℃总延伸5 min。扩增产物经1%琼脂糖电泳后,按照琼脂糖凝胶DNA回收试剂盒说明书做胶回收。
| 表 1 引物序列 |
1.4 酵母双杂交载体构建
经限制性内切酶Nde I和EcoR I酶切pGBKT7质粒和TGF-β1基因片段,以及限制性内切酶Bam HI和EcoR I酶切pGADT7质粒和TBRⅡ-A、TBRⅡ-B、TBRⅡ-C、TBRⅡ-D 4个基因片段,割胶回收,在T4 DNA连接酶作用下16 ℃连接过夜,转化至氯化钙法制备的DH5α中,涂布到含有卡那霉素/氨苄霉素的平板培养基上,37 ℃烘箱过夜培养12 h,挑取单克隆菌落。
1.5 酵母双杂交载体鉴定将挑取的单克隆菌落,在含卡那霉素/氨苄霉素LB(溶菌肉汤)液体培养基培养后,抽提质粒,进行PCR和双酶切鉴定,鉴定正确的阳性菌株送上海生工生物工程有限公司测序。新重组的质粒分别命名为:pGBKT7-TGF-β1和pGADT7-TβRⅡ-A、pGADT7-TβRⅡ-B、pGADT7-TβRⅡ-C、pGADT7-TβRⅡ-D。
2 结果 2.1 目的基因TGF-β1和受体扩增(图 1)
|
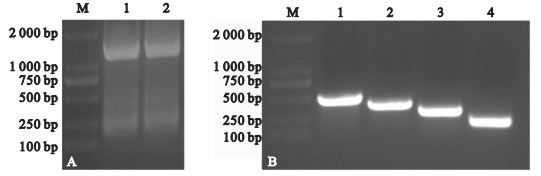
注:A1-2:TGF-β1;B1~4:TβRⅡ-A、B、C、D。 图 1 TGF-β1(A)和TβRⅡ受体(B) PCR扩增产物电泳图 |
以逆转录cDNA为模板和F11 & R22为引物,TGF-β1的PCR扩增产物经1%琼脂糖凝胶电泳检测,结果显示,产物条带大小约为1 200 bp左右,与预期一致(图 1A)。以逆转录cDNA为模板和F1 & R1、F2 & R2、F3 & R3、F4 & R4为引物,PCR扩增产物经1%琼脂糖凝胶电泳检测,结果显示,TβRⅡ-A、TβRⅡ-B、TβRⅡ-C和TβRⅡ-D产物条带大小分别为453、366、276、165 bp左右,与预期一致(图 1B)。
2.2 酵母双杂交载体的PCR鉴定(图 2)
|
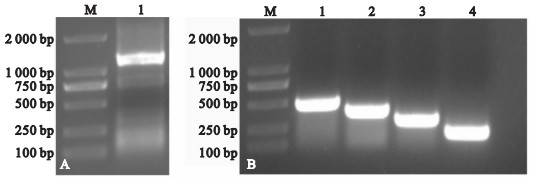
注:A1:TGF-β1质粒;B1~4:TβRⅡ-A、B、C、D质粒。 图 2 TGF-β1和TβRⅡ-A、B、C、D质粒PCR扩增产物电泳图 |
将挑取的克隆菌株DH5α/pGBKT7-TGF-β1加入到Luria-Bertani(LB)液体培养基内摇菌过夜,抽提质粒pGBKT7-TGF-β1为模板,以F11 & R22为引物进行PCR扩增,产物经1%琼脂糖凝胶电泳检测,在1 200 bp处有一明亮单一条带,与预期结果相符(图 2A)。试剂盒抽提DH5α/pGADT7-TβRⅡ-A、B、C、D菌株质粒,质粒为模板,以F1 & R1、F2 & R2、F3 & R3、F4 & R4为引物,产物经1%琼脂糖凝胶电泳检测,分别在453、366、276、165 bp处有一明亮单一条带,与预期结果相符(图 2B)。
2.3 酵母双杂交载体的双酶切鉴定(图 3)
|
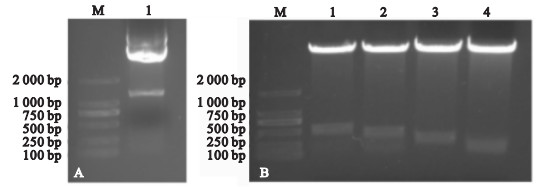
注:A1:TGF-β1质粒;B1~4:TβRⅡ-A、B、C、D质粒。 图 3 TGF-β1和TβRⅡ-A、B、C、D质粒酶切鉴定 |
抽提DH5α/pGBKT7-TGF-β1菌株质粒,经限制性内切酶Nde Ⅰ和EcoR Ⅰ双酶切,酶切产物经1%琼脂糖凝胶电泳检测,结果显示,pGBKT7载体7 300 bp左右和TGF-β1基因片段1 200 bp,分别与预期酶切条带相符(图 3A)。抽提DH5α/pGADT7-TβRⅡ-A、B、C、D菌株质粒,经限制性内切酶Bam HI和EcoR I双酶切,酶切产物经1%琼脂糖凝胶电泳检测,结果显示,pGADT7载体8 000 bp左右和TβRⅡ-A基因片段453 bp、TβRⅡ-B基因片段366 bp、TβRⅡ-C基因片段276 bp、TβRⅡ-D基因片段165 bp目的条带,分别与预期酶切条带相符(图 3B)。
2.4 酵母双杂交载体的DNA测序(图 4)
|
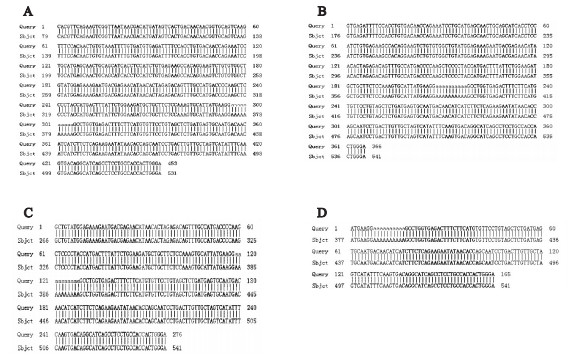
注:A:TβRⅡ-A基因;B:TβRⅡ-B基因;C:TβRⅡ-C基因;D:TβRⅡ-D基因。 图 4 运用NCBI BLAST软件比对pGADT7载体上的TβRⅡ-A、B、C、D序列 |
将试剂盒抽提的pGADT7-TβRⅡ-A、B、C、D菌株质粒送生工生物工程(上海)股份有限公司测序,结果表明插入在pGADT7载体上的序列TβRⅡ-A、TβRⅡ-B、TβRⅡ-C和TβRⅡ-D与Genebank公布的序列相一致。
3 讨论转化生长因子-β(TGF-β)在纤维化过程中发挥关键作用,被公认为是纤维化形成与发展的启动枢纽,TGF-β1的过量表达是诱发纤维化疾病的重要因素,而TGF-β1和TβRⅡ的相互作用在TGF-β1/Smad和TGF-β1/MAPK(mitogen-activated protein kinase)介导的信号通路中发挥着关键作用。因此,如能筛选到与TGF-β1相互作用较强的TβRⅡ,将与野生型TβRⅡ竞争结合过量表达的TGF-β1,弱化野生型TβRⅡ与TGF-β1的相互作用,可起到抗纤维化作用。本研究拟构建TGF-β1和4个截短型人转化生长因子β Ⅱ型受体(TβRⅡ-A、B、C、D)基因片段的酵母双杂交表达载体,构建好的4个截短型人转化生长因子β Ⅱ型受体(TβRⅡ-A、TβRⅡ-B、TβRⅡ-C和TβRⅡ-D)分别对应的氨基酸数为151、122、92、55 aa。
在人血液中提取RNA过程中,置放6 h以上的血液所提取的RNA很容易降解,而用新鲜血液提取RNA降解概率则会减小。同时,RNA洗涤时,加入75%乙醇混匀,4 ℃、14 000 g离心5 min,弃掉上清液,干燥空气中放置5~10 min,需让乙醇全部挥发,以免影响RNA浓度。另外,为防止RNA降解,可以在Trizol® LS中加入异硫氰酸胍。异硫氰酸胍被认为是最有效的RNA酶抑制剂,它在裂解组织的同时也使RNA酶失活。它既可破坏细胞结构使核酸从核蛋白中解离出来,又对RNA酶有强烈的变性作用。因此,当样品为富含RNA酶的组织时,利用它可取得满意的效果[8]。
酵母表达外源基因具有一定的翻译后加工能力,收获的外源蛋白质具有一定程度上的折叠加工和糖基化修饰,性质较原核表达的蛋白质更加稳定,特别适合于表达真核生物基因和制备蛋白质。而目前常用的酵母表达系统之一为巴斯德毕氏酵母,基因可得到高水平的表达[9]。由于TGF-β1基因片段为1 200 bp左右,目的基因片段相对较大,因此TGF-β1与pGADT7连接相对困难,解决的方法主要包括:适当增加基因片段和质粒的摩尔比;增加连接的时间;将目的基因与载体进行梯度连接;涂板后过夜观察固体培养基菌落情况,以增加阳性克隆的出现。本研究结果表明成功构建TGF-β1和4个不同的TβRⅡ基因片段的酵母表达载体,可为进一步运用酵母双杂交系统筛选与TGF-β1相互作用的TβRⅡ的关键区域提供技术支持。
| [1] | Painemal P, Acua MJ, Riquelme C, et al. Transforming growth factor type beta 1 increases the expression of angiotensin Ⅱ receptor type 2 by a SMAD-and p38 MAPK-dependent mechanism in skeletal muscle[J]. Biofactors, 2013, 39(4): 467–475. DOI:10.1002/biof.1087 |
| [2] | Luo BL, Niu RC, Feng JT, et al. Downregulation of secretory leukocyte proteinase inhibitor in chronic obstructive lung disease:the role of TGF-β/Smads signaling pathways[J]. Archives of Medical Research, 2008, 39(4): 388–396. DOI:10.1016/j.arcmed.2008.02.002 |
| [3] | Narimatsu M, Labibi B, Wrana JL, et al. Analysis of Hippo and TGFβ signaling in polarizing epithelial cells and mouse embryos[J]. Differentiation, 2016, 91(4-5): 109–118. DOI:10.1016/j.diff.2016.01.003 |
| [4] | Gu W, Fukuda T, Isaji T, et al. α1, 6-Fucosylation regulates neurite formation via the activin/phospho-Smad2 pathway in PC12 cells:the implicated dual effects of Fut8 for TGF-β/activin-mediated signaling[J]. Faseb Journal, 2013, 27(10): 3947–3958. DOI:10.1096/fj.12-225805 |
| [5] | Ma W, Kilaru S, Collins C, et al. Libraries for two-hybrid screening of yeast and hyphal growth forms in Zymoseptoria tritici[J]. Fungal Genetics and Biology, 2015, 79: 94–101. DOI:10.1016/j.fgb.2015.03.023 |
| [6] | Gao JX, Jing J, Yu CJ, et al. Construction of a high-quality yeast two-hybrid library and its application in identification of interacting proteins with Brn1 in Curvularia lunata[J]. Plant Pathology Journal, 2015, 31(2): 108–114. DOI:10.5423/PPJ.OA.01.2015.0001 |
| [7] | Stynen B, Tournu H, Tavernier J, et al. Diversity in genetic in vivo methods for protein-protein interaction studies:from the yeast two-hybrid system to the mammalian split-luciferase system[J]. Microbiology and Molecular Biology Reviews Mmbr, 2012, 76(2): 331–382. DOI:10.1128/MMBR.05021-11 |
| [8] | 杨利丽, 刘红英, 杨和军, 等. 一种改进的异硫氰酸胍法结合硅胶膜离心吸附柱提取孕妇外周血微量胎儿RNA的方法[J]. 中国生物化学与分子生物学报, 2012, 28(2): 177–181. |
| [9] | 吴蒙, 刘宇鸽, 李改瑞, 等. H5N1禽流感病毒HA与NA基因克隆及分泌表达[J]. 中国公共卫生, 2011, 27(1): 37–39. DOI:10.11847/zgggws2011-27-01-17 |
 2017, Vol. 33
2017, Vol. 33



