铅(lead, Pb)是常见的工业污染物之一,可在人体和动物组织中蓄积,在人体内不易降解,分布极为广泛[1],极低的浓度便可对人体产生毒害。国内外研究表明,Pb能够干扰人体神经、骨骼、免疫等多组织器官的正常代谢和功能运转[2]。铅在人体最主要的靶器官是骨骼,它进入机体后,最终95%均蓄积在骨骼中,半衰期长达5~20年[3],与骨骼发育畸形、骨质疏松、骨关节炎等密切相关[4]。研究表明骨代谢就是成骨细胞形成新骨和破骨细胞吸收旧骨的过程[5]。Wingless protein(Wnt)信号通路是目前骨骼系统相关疾病发病机制和骨代谢研究的新热点,Wnt/β-catenin信号通路在骨重建过程中起重要作用,与成骨细胞分化、增殖和骨形成密切相关,并通过不同途径影响破骨细胞及骨细胞功能[6];Wnt2属于分泌型蛋白家族成员,它通过自分泌或旁分泌作用,与位于细胞膜上的受体蛋白相结合[7],Wnt蛋白在成骨细胞中可通过经典信号通路调节成骨细胞的增殖和分化[8],参与骨发生过程的调节。转录因子1(transcription factor 1, Tcf-1) 是Wnt信号通路核内转录因子,在Wnt信号调控转录过程中起着分子开关作用,它与β-catenin结合后在核内共同调控靶基因,调节成骨细胞的活性和功能[9]。过氧化物酶体增长因子活化受体γ(peroxisome proliferator-activated receptor γ, PPAR-γ)是细胞核受体PPAR家族成员中之一,是重要的成脂分化转录因子,可调节骨髓间充质干细胞直接抑制前成骨细胞分化基因还可抑制Wnt信号通路,在机体生长发育及代谢方面有着十分重要的作用[10]。β-catenin是一种胞质内的糖蛋白, 作为Wnt经典信号通路的起始蛋白和关键分子,直接参与调节成骨细胞形成和骨骼发育[11]。目前铅对骨代谢的影响主要着重于研究通过影响维生素D,钙磷代谢而导致的骨发育异常、骨钙化障碍[12],对于Wnt信号通路中Wnt2、Tcf-1、PPAR-γ基因研究较少。因此,本研究通过观察染铅大鼠骨骼中铅、钙元素和骨组织形态及骨骼中PPAR-γ、Wnt2、Tcf-1和β-catenin的基因表达变化,旨在探讨铅对骨代谢的影响及其机制,为预防和改善铅中毒提供科学依据。结果报告如下。
1 材料与方法 1.1 实验动物21日龄雄性Sprague-Dawley(SD)大鼠,购于北京维通利华实验动物技术有限责任公司,生产许可证号码为:SCXK(京)2012-0001。自然昼夜,节律光照,温度(20±5)℃,相对湿度为40%~60%。基础饲料喂养,自由饮食、饮水。
1.2 主要试剂与仪器Trizol(美国Invitrogen公司),SYBR® Premix Ex TaqTM Ⅱ试剂盒和DNA Marker(大连宝生物公司),醋酸铅(天津金汇太亚化学试剂有限公司)。Optima5300DV型ICP发射光谱仪(美国PE公司),BX 51型生物显微镜(日本Olympus公司),RM2265型切片机(德国LEICA公司),HY-BM1160生物组织包埋机(金华惠友仪器生物有限公司),Mx3000P荧光定量PCR仪(美国Stratagene公司),Eppendorf AG核酸蛋白测定仪(德国Eppendorf公司),DYY-Ⅲ7B型电泳仪(北京市六一仪器厂),BIO-RAD凝胶成像系统(美国BIO-RAD公司)。
1.3 分组与处理大鼠随机分为4组:对照组、低、中、高剂量铅组,每组10只;对照组大鼠饮去离子水;低、中、高剂量铅组大鼠饮水中分别含有0.1%、0.2%、0.3%醋酸铅;饲养60 d后,过夜禁食12 h,称重后,用乙醚将大鼠麻醉处死,取后肢股骨,剔净周围肌肉组织,一部分经固定、脱水、包埋、切片、苏木素-伊红染色(hematoxylin-eosin staining,HE),光镜观察组织形态。另一部分组织迅速存于液氮中,然后在-80 ℃冰箱中保存,待用。
1.4 骨骼中Pb、Ca含量测定取股骨,加入8 mL硝酸和2 mL高氯酸(高氯酸:硝酸=1:4,V:V)静置过夜后于电炉上进行湿法消化,同时作对照管;消化至白色颗粒后用双蒸水定容至25 mL,用电感耦合等离子发射光谱仪测定骨组织中Pb、Ca含量。
1.5 Wnt信号通路因子mRNA表达检测采用荧光定量reverse transcriptase-PCR(RT-PCR)法,按Trizol试剂盒方法提取股骨组织中总RNA,采用琼脂糖凝胶电泳和核酸蛋白测定仪对RNA进行检测。
1.5.1 引物设计与合成应用Primer 5.0软件设计引物,由上海生工生物工程有限公司合成,β-actin上游引物:5′-TACCCAGGCATTGCTGACAG-3′,下游:5′-AGCCACCAATCCACACAGAG-3′,片段长度104 bp;PPAR-γ上游引物:5′-AGGAGCAGAGCAAAGAGGTG-3′,下游:5′-CACAGCAAACTCAAACTTAGGC-3′,片段长度107 bp;Wnt2上游引物:5′-CAACTTGACTTCCCGAGGCA-3′,下游:5′-GTAGGAGTTGTCCAGTCGGC-3′,片段长度171 bp;Tcf-1上游引物:5′-GGCTTACGAGAGGCAGAAGA-3′,下游:5′-TTACTG GGAGAGAGGGTGGTT-3′,片段长度198 bp;β-catenin上游引物:5′-ACACAACCTTTCCCACCATC-3′,下游:5′-GCTTTCCTGATTGCCGTAAG-3′,片段长度154 bp。
1.5.2 荧光定量RT-PCR反应体系为10.0 μL:SYBRPremix Ex TaqTM Ⅱ(2×)5.0 μL,forward primer(10 μmol/L)1.0 μL,reverse primer(10 μmol/L)1.0 μL,cDNA 1.0 μL;dH2O(灭菌双蒸水)2.0 μL;反应条件:95 ℃ 5 min;95 ℃ 5 s;60 ℃ 30 s,50个循环;95 ℃ 15 s,60 ℃ 1 min,95℃ 15 s;反应结束后,计算threshold cycle(Ct)值;然后取样品cDNA 1 μL为模板,按2倍浓度梯度稀释,进行荧光定量PCR反应。结果用MXPro-MX3000P软件(Stratagene公司)自动进行数据分析,绘制标准曲线。以β-actin为看家基因,计算待测基因相对表达量。
1.6 统计分析计量数据以x±s表示,采用SPSS 17.0软件进行统计分析,组间比较进行方差齐性检验后选用单因素方差分析,再用最小显著差法进行均数间的两两比较,以P<0.05为差异有统计学意义。
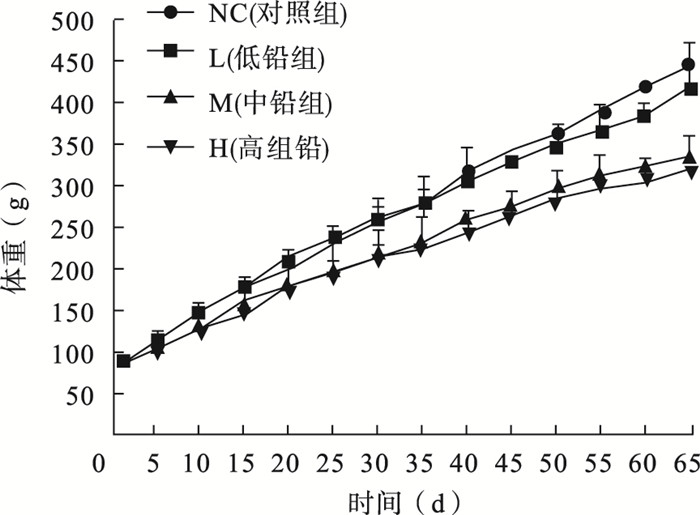
2 结果 2.1 染铅对大鼠体重影响(图 1)
|
图 1 染铅对大鼠体重影响 |
结果显示,低、中、高剂量铅组大鼠体重分别在染铅第35、25、10 d明显低于对照组,差异有统计学意义(P<0.05)。
2.2 染铅对大鼠骨骼中Pb与Ca含量影响(表 1)| 表 1 染铅对大鼠骨骼中Pb与Ca含量影响(mg/g,x±s,n=10) |
与对照组比较,各剂量染铅组大鼠骨骼中铅含量均明显升高,而骨骼中钙含量均明显下降,差异均有统计学意义(P<0.05或P<0.01)。
2.3 染铅对大鼠骨骼组织形态影响(图 2)
|
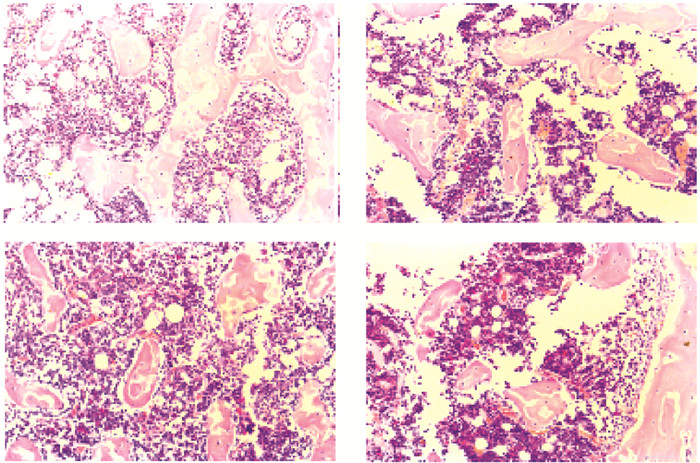
注:A:对照组;B、C、D:低、中、高剂量铅组。 图 2 染铅对大鼠骨组织形态影响(HE,×200) |
对照组大鼠股骨骨小梁丰富、结构相对紧密、饱满,钙盐沉着均匀(图 1A);与对照组比较,低、中剂量铅组大鼠骨小梁相对变薄、变细(图 1B、C);高剂量铅组大鼠股骨骨小梁稀疏、变细、变薄或断裂,骨髓腔相对扩大(图 1D)。
2.4 染铅对大鼠骨骼中Wnt通路因子mRNA表达影响(表 2)| 表 2 染铅对大鼠骨骼中Wnt通路因子mRNA表达影响(x±s,n=10) |
与对照组比较,高剂量铅组大鼠骨骼中PPAR-γ、Wnt2、Tcf-1和β-catenin mRNA表达量均下降,差异有统计学意义(P<0.05或P<0.01);与对照组比较,中剂量铅组大鼠骨骼中β-catenin mRNA表达量下降,差异有统计学意义(P<0.01)。
3 讨论研究表明染铅可改变成骨细胞的形态、增殖速率和生物学标志物等,破坏成骨细胞活性,甚至导致成骨细胞的凋亡;当铅达到一定浓度时,也可改变成骨细胞的增殖功能[13]。当铅在体内蓄积剂量超过一定负荷时人体的自我调节能力被破坏[14],可引起包括钙在内的许多微量元素功能稳态的异常,从而导致多种代谢紊乱。本研究结果表明染铅组大鼠骨骼中Pb含量明显高于对照组,而Ca含量则明显低于对照组。可能与Pb、Ca均为二价离子,具有相似的生理生化性质,Pb与Ca在小肠上皮吸收的过程中,相互间存在竞争拮抗作用,且铅对骨组织高度亲和,导致骨骼中Ca水平变化有关。与已有研究结果一致[15]。
胡雪琴等[16]通过动物模型研究发现,铅暴露可导致大鼠股骨骨质密度稀疏,骨小梁数目锐减,使软骨的成骨作用受到干扰。本研究结果表明染铅组大鼠股骨中骨小梁网状结构被破坏,骨髓腔不明显。提示,由于铅与钙的拮抗作用,铅的存在破坏了骨组织中钙磷平衡,磷酸铅代替了钙盐的沉积,导致骨组织的结构受到损伤[17-18]。
Bodine等[19]研究表明,Wnt信号通路是参与调节骨髓间充质干细胞向成骨细胞分化,抑制成骨细胞的程序性死亡的经典通路。当Wnt与Frizzled蛋白、低密度脂蛋白受体相关蛋白偶联受体5/6(lipoprotein receptor related protein 5/6, LRP5/6) 结合时,β-catenin次磷酸化作用,通路被激活,利于成骨前体细胞向成骨细胞转化,成骨细胞增殖及分化功能加强,骨合成代谢活跃。PPAR-γ激活后参与调节细胞的增殖、分化及凋亡。本研究结果显示,高剂量染铅可降低大鼠骨骼中PPAR-γ、Wnt2、β-catenin及Tcf-1基因mRNA表达。提示,铅能够通过Wnt/β-catenin信号通路影响下游PPAR-γ及Tcf-1基因表达,抑制成骨细胞增殖、分化及破骨细胞功能,进而影响骨形成及骨的重建。
综上所述,染铅可使骨骼中Pb水平升高,Ca含量下降;导致骨组织形态结构损伤,其机制可能与下调Wnt通路中PPAR-γ、Wnt2、β-catenin及Tcf-1基因表达,影响骨细胞增殖和分化有关。
| [1] | 陈永前, 吕晓云. 长期铅暴露后果的研究进展[J]. 医学综述, 2013, 19(10): 1819–1822. DOI:10.3969/j.issn.1006-2084.2013.10.031 |
| [2] | Iavicoli I, Fontana L, Bergamaschi A. The effects of metals as endocrine disruptors[J]. Toxicology and Environmental Health, 2009(03): 206–223. |
| [3] | Hu H, Rabinowitz M, Smith D. Bone lead as a biological marker in epidemiologic studies of chronic toxicity:conceptual paradigms[J]. Environmental Health Perspectives, 1998, 1(106): 1–8. |
| [4] | 刘云忠, 毕树雄, 卫小春. 铅对骨骼的损伤机制及其生物学标志物[J]. 医学综述, 2011, 17(1): 97–99. |
| [5] | 白金, 邹建芳. 铅对骨代谢影响研究进展[J]. 中华劳动卫生职业病杂志, 2010, 28(9): 699–701. |
| [6] | 周军, 何成奇. Wnt/β-catenin信号通路在骨重建中的作用研究进展[J]. 中国康复医学杂志, 2015, 30(5): 513–515. |
| [7] | 李宝新, 李玉坤. Wnt信号通路对骨调节研究新进展[J]. 国际骨科学杂志, 2008, 29(03): 179–181. DOI:10.3969/j.issn.1673-7083.2008.03.013 |
| [8] | 刘艳玲, 李方兵, 赵曦. Wnt信号通路在成骨细胞中的作用:成骨还是破骨[J]. 中国组织工程研究, 2014, 18(33): 5366–5370. DOI:10.3969/j.issn.2095-4344.2014.33.021 |
| [9] | 唐泉, 杨冰, 孙元明. 经典Wnt信号通路对成骨细胞增殖和分化的影响[J]. 天津医药, 2012, 40(2): 187–189. |
| [10] | 裴红霞, 魏启幼, 蒋谊. Cbfα1、PPARγ在骨髓间质干细胞定向分化中的作用及对骨质疏松症的影响的研究[J]. 实用预防医学, 2006, 13(2): 244–247. |
| [11] | 陈锡山, 于燕妮, 易韦, 等. 氟对大鼠成骨细胞W nt3a、β-链蛋白mRNA和蛋白表达的影响[J]. 中华地方病学杂志, 2013, 32(2): 140–145. |
| [12] | 裴丹, 秦书俭. 铅对骨骼系统的影响[J]. 医学综述, 2008, 14(17): 2671–2674. DOI:10.3969/j.issn.1006-2084.2008.17.038 |
| [13] | 靳翠红, 蔡原, 刘秋芳. 铅对大鼠成骨细胞形态学的影响[J]. 毒理学杂志, 2006, 10(3): 183–184. |
| [14] | Anderson C, Danylchuk KD. The effect of chronic low level lead intoxication on the haversion remodeling system in dogs[J]. Lad Invest, 1977, 37(5): 466–469. |
| [15] | 曾造, 赵云强. 微量元素缺乏对儿童健康的影响[J]. 微量元素与健康研究, 2007, 24: 14–16. DOI:10.3969/j.issn.1005-5320.2007.01.007 |
| [16] | 胡雪琴, 糜漫天. 铅对幼年大鼠钙的吸收和骨骼生长的影响[J]. 第三军医大学学报, 2007, 5: 2–4. |
| [17] | 陈修文, 万昌武, 谢春, 等. 氟对大鼠骨组织RBPJ及相关基因表达影响[J]. 中国公共卫生, 2016, 32(2): 195–198. DOI:10.11847/zgggws2016-32-02-18 |
| [18] | 杨青, 陈巾宇, 杨野仝, 等. 肥胖模型大鼠钙代谢和钙营养状态指标的检测及意义[J]. 中国公共卫生, 2015, 31(1): 1–4. DOI:10.11847/zgggws2015-31-01-01 |
| [19] | Bodine PVN, Zhao W, Kharode YP, et al. The Wnt antagonist secreted frizzled-related protein-1 is a negative regulator of trabecular bone formation in adult mice[J]. Molecular Endocrinology, 2004, 18(5): 1222–1237. DOI:10.1210/me.2003-0498 |
 2017, Vol. 33
2017, Vol. 33


