2. 安徽省六安市疾病预防控制中心
小肠结肠炎耶尔森菌是上个世纪80年代以来引起国际社会广泛关注的一种食源性病原菌[1-2],该菌俗称嗜冷菌,广泛分布于自然界,是能在冷藏温度下生长的少数肠道致病菌之一。冷冻冷藏食品受到污染主要与该菌的这种生物学特性有关,加上食品中丰富的营养物质,也为该菌的生长繁殖提供了良好的环境条件。冷冻冷藏食品品种繁多,确保其食品的卫生与安全十分重要。为了解安徽省六安市冷冻冷藏食品卫生现状本研究于2009-2014年采集本地超市销售的冷冻冷藏食品523份,调查小肠结肠炎耶尔森菌污染状况,现将结果报告如下。
1 材料与方法 1.1 标本来源2009-2014年度每年的5-10月在安徽省六安市区几家大型商场、超市食品专柜分批采集冷冻冷藏食品标本,共计523份。无菌手续采集样品后置无菌袋中,2 h内送达实验室。
1.2 主要仪器与试剂2720型Thermal Cycler PCR仪 (美国ABI公司);GelDoc 2000系统凝胶成像仪为 (美国伯乐公司);CHEF-Mapper XA型脉冲场凝胶电泳仪 (美国伯乐公司);耶尔森菌选择琼脂 (CIN)(美国BD公司);API 20E生化鉴定条 (法国生物梅里埃公司);诊断血清 (日本生研株式会社);抗生素敏感纸片 (杭州天和公司);基因检测引物 (上海生工生物工程公司);脉冲场凝胶电泳 (pulsed field gel electrophoresis,PFGE):限制性内切酶Not、XbaI (美国Promega公司);SeakemGold琼脂糖 (美国Cambraex Bio Science Rockland公司);蛋白酶K (德国Merck公司);十二烷基肌氨酸钠 (美国Sigma公司)。以上培养基及试剂均在有效期内使用。
1.3 方法按照1:10比例无菌取样本置10 mL改良磷酸缓冲溶液 (phosphate buffer,PSB) 增菌液中,置4 ℃环境中增菌培养,然后按照《小肠结肠炎耶尔森菌实验室分离与鉴定手册》二版[3]、三版[4]分离鉴定。
1.4 统计分析用SPSS 13.0软件对数据进行统计学处理,采用χ2检验,P < 0.05差异有统计学意义。
2 结果 2.1 生物学检测 (表 1)| 表 1 安徽省六安市冷冻冷藏食品小肠结肠炎耶尔森菌检测 |
2009-2014年共收到送检的冷冻冷藏食品523份,检出小肠结肠炎耶尔森菌104株,阳性检出率为19.89%;其中生食322份,熟食201份,分别检出该菌99株和5株,阳性检出率分别为30.75%和2.49%,差异明显 (χ2=62.03 P < 0.01)。总的看来,2009年未检出小肠结肠炎耶尔森菌,2010年的阳性检出率为10.0%,2011-2014年标本的阳性检出率分别为35.38%、31.67%、27.78%和25.0%。
2.2 生化谱分析分离的小肠结肠炎耶尔森菌均为革兰氏阴性短小球杆状菌,该菌经生物梅里埃API 20E生化系统鉴定并确认。104株菌生化鉴定后发现,小肠结肠炎耶尔森菌有6种生化反应模式,其中生化编码1155723、1155523 2种最为常见,分别占鉴定菌株的51.92%(54/104) 和25.0%(26/104),其他均不多见。O:8型和未定型菌株的生化编码主要有1155723、1155523、1155563 3种,而O:3型菌株的生化编码一般为1015523。
2.3 小肠结肠炎耶尔森菌的血清型分布 (表 2)| 表 2 小肠结肠炎耶尔森菌血清型分布 (株) |
采集的冷冻冷藏食品样本中分离的小肠结肠炎耶尔森菌血清型相对广泛,有5个血清型,其中O:8型34株,最为多见,占32.69%;致病性O:3型和O:9型菌株也均有发现;另外还有54株小肠结肠炎耶尔森菌,运用现有的诊断用品和检测手段均不能鉴定其血清学型别,暂定为未定型菌株。
2.4 抗生素敏感性 (表 3)| 表 3 小肠结肠炎耶尔森菌的药物敏感性 |
分离菌株致病性、非致病性小肠结肠炎耶尔森菌药物敏感性试验,结果显示,这些菌株对左氧氟沙星、哌拉西林、亚胺培南、诺氟沙星、环丙沙星等药物高度敏感,而对临床上频繁使用的氧氟沙星、头孢唑啉等药物出现了抗药性,对复方新诺明、阿莫西林、氨苄西林等几乎不敏感。
2.5 分子生物学检测 2.5.1 聚合酶链反应 (polymerase chain reaction,PCR) 检测foxA基因 (表 4)| 表 4 15株小肠结肠炎耶尔森菌的毒力基因分布 |
选择其中110份冷冻冷藏食品增菌培养,对培养标本同时进行PCR法和常规分离培养法检测小肠结肠炎耶尔森菌的对照性研究,结果PCR法阳性35份,分离培养法阳性34份,阳性检出率分别为31.82%和30.91%, 2种方法的符合率达95.45%(105/110),而PCR法阳性、培养法阴性以及PCR法阴性、培养法阳性的仅有5份标本,不吻合率仅占4.55%,其阳性检出率无明显差异 (χ2=0.021 P>0.05)。
2.5.2 毒力基因检测。PCR检测15株致病性和非致病性小肠结肠炎耶尔森菌毒力基因,发现其中O:3型菌株的毒力基因分布为ail+、ystA+、yadA+、virF+、ystB-,为典型的致病性小肠结肠炎耶尔森菌的基因分布特点,而O:8型和其他血清型菌株均携带ystB基因而不携带上述毒力基因。
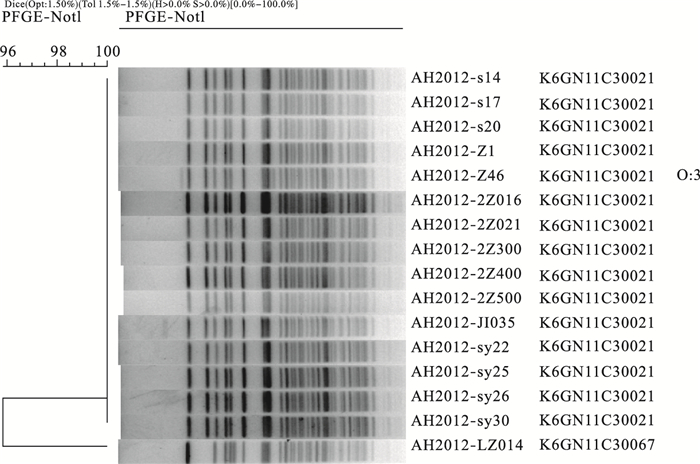
2.5.3 PFGE分子分型 (图 1)
|
注:图中S14、S17、S20为冷冻冷藏食品中分离的O:3型菌株,其余13株来自本地腹泻病人、宿主动物标本[18]。 图 1 16株O3型小肠结肠炎耶尔森菌PFGE带型聚类图 |
PFGE分型鉴定16株O:3型小肠结肠炎耶尔森菌,经Not1内切酶酶切,分型后得到19~20个条带,根据相对分子质量标准Marker H9812的条带范围,应用BioNumeries 6.6软件,选择可识别条带聚类分析,16株小肠结肠炎耶尔森菌分为2种PFGE带型。3株冷冻冷藏食品中分离的O:3型菌株与本地腹泻病人、宿主动物标本分离的O:3型菌株带型聚类图高度一致,相似度在96.0%~100%。
3 讨论小肠结肠炎耶尔森菌病的病原体是小肠结肠炎耶尔森菌,该菌主要通过粪-口途径传播,人与感染动物粪便密切接触,或食用被污染的食品而感染。采集六安市集中销售的冷冻冷藏食品523份标本,检出小肠结肠炎耶尔森菌104株;阳性检出率高达19.89%,远远高于国内相关医学文献的报告[5-7]。结果表明,本地冷冻冷藏食品受到小肠结肠炎耶尔森菌的污染相当严重,尤其是熟食标本中检出致病性O:3型小肠结肠炎耶尔森菌,人们购买熟食食品如果不加热或加热不彻底,势必会造成该菌感染。因此生产单位要做好消毒灭菌,销售单位应将生熟分开,分类储存,整个销售过程应该在卫生、安全的程序中进行,才能确保冷冻冷藏食品的安全。
API 20E生化系统鉴定后发现O:3型菌株的生化编码与其他型别菌株有差异,是由于O:3型菌株缺乏分解利用鸟氨酸的能力,其生化反应的特殊性是否与其不同的抗原结构、菌株的致病性有关,有待于进一步的研究与探讨。这也表明,不同型别菌株对糖、氨基酸等的分解利用有其不同的表现,即使同型菌株的生化反应结果也不完全相同。从血清学鉴定结果来看,本地该菌的血清型分布广泛,O:8型菌株居首位,占分离菌株的32.69%;-美洲、欧洲、日本等国家的致病性0:8型菌株均携带有典型的毒力因子[8-9],而国内的0:8型菌株均不携带毒力因子[2, 10],这种差异尚值得进一步的研究与探讨。实验结果表明,小肠结肠炎耶尔森菌0:3型和0:9型是致病性菌株,这也得到国内的研究资料证实[11-13]。还有部分菌株运用现有的诊断血清不能确定血清型,这需要国内研究机构研制生产符合中国国情的新的系列诊断血清,填补诊断血清不足的缺陷。与其他细菌一样,抗生素的应用在小肠结肠炎耶尔森菌的治疗中起到关键的作用。因此,有必要开展小肠结肠炎耶尔森菌对抗菌药物的敏感性研究,为临床指导用药。
在冷冻冷藏食品中检出小肠结肠炎耶尔森菌在安徽省省尚属首次报告,为建立安徽省小肠结肠炎耶尔森菌菌种库,分子分型数据库和小肠结肠炎耶尔森菌病的防治工作提供了科学依据。foxA是小肠结肠炎耶尔森菌的一个保守基因,可用于小肠结肠炎耶尔森菌菌种的鉴定[14]。PCR扩增ail和foxA基因和分离培养的比对试验,结果显示PCR法能准确、快速检测标本中的小肠结肠炎耶尔森菌,为该病患者的早期诊断和治疗,提供一种快速有效的检测方法。分离培养法之所以能获得同样的检测结果,与增菌培养标本在分离培养之前的碱处理有密切关系。小肠结肠炎耶尔森菌的致病性主要是由位于染色体和毒力质粒上的毒力基因决定的,一般通过检测其中的毒力基因来判断该菌的致病性[15]。PFGE被广泛应用于细菌的分子分型研究[16-17],检测发现冷冻冷藏食品中的O:3型菌株与腹泻病人、宿主动物同型菌株[18]带型聚类图高度一致,同为K6GNIIC30021,血清型同为O:3型,说明在冷冻冷藏食品中分离的O:3型菌株与腹泻病人宿主动物标本中分离的同型菌株有密切的同源性关系,也进一步表明污染的冷冻冷藏食品是本地小肠结肠炎耶尔森菌病的传染源之一,应该引起高度重视。
| [1] | Wang X, Li Y, Jing HQ, et al. Complete genome sequence of a Yersinia enterocolitca"old world"(3/O:9) strain and comparison with the "new world" (1B/O:8) strain[J]. J Clin Microbiol, 2011, 49 : 1251–1259. DOI:10.1128/JCM.01921-10 |
| [2] | Wang X, Qiu H, Jin D, et al. O:8 serotype Yersinia enterocolitica strains in China[J]. Int J Food Microbiol, 2008, 125(3) : 259–266. DOI:10.1016/j.ijfoodmicro.2008.04.016 |
| [3] | 景怀琦, 王鑫, 崔志刚, 等. 小肠结肠炎耶尔森菌实验室分离与鉴定手册[M].2版. 北京: 2009: 7-32. |
| [4] | 景怀琦, 王鑫. 小肠结肠炎耶尔森菌实验室分离与鉴定手册[M].3版. 北京: 2013: 14-37. |
| [5] | 刘振, 吴旭东, 刘宗东. 冷冻食品中小肠结肠炎耶尔森菌的检测[J]. 中国公共卫生, 2005, 21(11) : 1322. |
| [6] | 张伦, 刘巧宜, 邓志爱, 等. 广州地区食品中小肠结肠炎耶尔森菌分布特征的初步研究[J]. 中国卫生检验杂志, 2008, 18(5) : 875–876. |
| [7] | 肖玉春, 李可维, 梁俊容, 等. 聚合酶链反应法和分离培养法筛检小肠结肠炎耶尔森菌方法的比较研究[J]. 疾病监测, 2013, 28(6) : 456–458. |
| [8] | Thoerner P, Kingombe CIB, Bogli-Stuber K, et al. PCR detection of virulence genes in Yersinia enterocolitica and Yersinia pseudotuberculosis and investigation of virulence gene distribution[J]. Appl Environ Microbiol, 2003, 69 : 1810–1816. DOI:10.1128/AEM.69.3.1810-1816.2003 |
| [9] | Pelludat C, Rakin A, Jacobi CA, et al. The yersiniabactin biosynthetic gene cluster of Yersinia enterocolitica:organization and siderophore-dependent regulation[J]. J Bacteriol, 1998, 180 : 538–546. |
| [10] | 郝琼, 刘翔, 郭邦成, 等. 1997-2010年宁夏回族自治区小肠结肠炎耶尔森菌致病性的基因特征[J]. 中华预防医学杂志, 2011, 45(10) : 886–889. |
| [11] | 于恩庶. 中国小肠结肠炎耶尔森氏菌研究进展[J]. 中华流行病学杂志, 2000, 21(6) : 453–455. |
| [12] | 景怀琦, 李继耀, 肖玉春. 03型和09型小肠结肠炎耶尔森菌主要毒力基因分布调查[J]. 中国媒介生物学及控制杂志, 2004, 15(4) : 317–319. |
| [13] | 杨晋川, 刘会芳, 许静静, 等. 徐州地区小肠结肠炎耶尔森菌病原学初步研究[J]. 中国人兽共患病学报[J], 2007, 23(5) : 489–492. |
| [14] | 王鑫, 景怀琦, 徐建国. 小肠结肠炎耶尔森菌耐热肠毒素家族及其编码基因研究进展[J]. 中国媒介生物学及控制杂志, 2006, 17(4) : 304–344. |
| [15] | 孟真, 石国祥, 程苏云, 等. 浙江省部分地区小肠结肠炎耶尔森菌 (动物株) 分子生物学特征初探[J]. 中国卫生检验杂志, 2007, 17(1) : 60–63. |
| [16] | Soldati L, Piffaretti JC. Molecular typing of Shigella strains using pulsed field gel electrophoresis and genome hybridization with insertion sequences[J]. Res Microbiol, 1991, 142 : 489–498. DOI:10.1016/0923-2508(91)90182-A |
| [17] | 金东, 崔志刚, 肖玉春, 等. 中国六省致病性小肠结肠炎耶尔森的脉冲场凝胶电泳分析[J]. 中华流行病学杂志, 2006, 27 : 677–680. |
| [18] | 张凤, 丁业荣, 高大维, 等. 腹泻病人标本分离小肠结肠炎耶尔森菌及其病原学研究[J]. 中国卫生检验杂志, 2015, 25(16) : 2693–2696. |
 2017, Vol. 33
2017, Vol. 33


