流行性脑脊髓膜炎 (epidemic cerebrospinal meningitis, ECM),是由脑膜炎奈瑟菌 (Neisseria meningitidis, Nm) 引起的急性呼吸道传染病,具有起病急、病情发展快和病死率高的特点[1]。Nm的主要毒力因子是荚膜多糖,根据其特征,Nm可分为12个血清群 (A、B、C、E、H、I、K、L、X、Y、Z和W135)[2], 大多数感染菌株为A、B、C、Y、W135血清群,并以C群毒力最强[3]。中国大陆目前主要流行的Nm群是C群ST-4821[4-8],是国际上引起ECM流行的第7个具有高致病性的C群菌株亚群[3],此序列群造成安徽省2003-2005年ECM爆发、流行[6、9]。海南省自2010年开始有确诊C群ECM病例,2012年和2013年的ECM病例均由C群Nm引起;2015年首次确诊由B群Nm引起的ECM病例。为了解海南省Nm的分子分型特征,本研究收集2005-2015年海南省健康人群Nm监测分离株、ECM病例及其密切接触者分离株进行多位点序列分型 (multilocus sequence typing, MLST),现将结果报告如下。
1 材料与方法 1.1 菌株来源收集海南省2005-2015年Nm样本共17份,其中ECM病例分离株3株,脑脊液标本1份,密切接触者分离株2株,健康人群Nm监测阳性分离株11株。
1.2 主要试剂及仪器普通巧克力平板、血平板 (广东环凯微生物有限公司);Nm鉴定卡 (法国生物梅里埃公司);Nm诊断血清 (美国REMEL公司);细菌基因组DNA试剂盒 (QIAamp DNA Mini Kit和QIAamp DNA Blood Mini Kit,德国QIAGEN公司);Taq及Ex Taq DNA聚合酶 (5 U/μL)、DL 2 000 Marker (大连TaKaRa宝生物公司);琼脂糖 (西班牙Biowest公司);核酸染料 (北京赛百盛公司);Tpersonal PCR仪 (德国Biometra公司),EPS-300电泳仪 (上海天能科技有限公司);Gel Doc XR+凝胶成像系统 (美国Bio-Rad公司)。Nm普通聚合酶链反应 (polymerase chain reaction,PCR) 引物参照标准[10]合成, MLST分型引物参照PubMLST数据库http://pubmlst.org/neisseria/imformation合成7个管家基因abcZ、adk、aroE、fumC、gdh、pdhC、pdm的PCR扩增引物和测序引物,引物合成和测序均由上海生工生物工程公司完成。
1.3 方法 1.3.1 菌株的复苏鉴定将保存于-80 ℃冰箱的脱脂牛奶管菌株接种巧克力平板,37 ℃ 5% CO2培养24~48 h,挑取单个疑似菌落分离纯培养物供生化鉴定和血清学分群,按WS 295-2008流行性脑膜炎奈瑟菌诊断标准[10]判定结果。
1.3.2 细菌DNA的提取生化反应符合者按细菌DNA提取试剂盒说明书严格操作,脑脊液样本按QIAamp DNA Blood Mini Kit试剂盒说明书提取DNA。提取DNA,-20℃保存用于PCR检测和MLST分型。
1.3.3 细菌菌株PCR复核鉴定PCR扩增Nm属特异性基因crgA和A、B、C、Y、W135不同群的特异性基因片段,确定不同菌株的基因型。反应总体积25 μL,包括10X Buffer2.5 μL,2.5 mmol/L dNTP 2 μL, 10 μmol/L上下游引物各1 μL,TaqDNA聚合酶0.5 μL,灭菌超纯水16 μL,模板DNA 2 μL。反应条件:95 ℃预变性3 min,92 ℃变性30 s,55 ℃退火40 s,72 ℃延伸30 s,共37个循环,72 ℃延伸40 s。扩增产物用2%琼脂糖凝胶电泳,方法同文献[11]。
1.3.4 MLST将提取的DNA进行7个管家基因的PCR扩增,反应总体积50 μL,包括10X Ex Taq Buffer 5 μL,2.5 mmol/L each dNTP Mixture 1μL, 10 μmol/L上下游引物各1μL,Ex Taq DNA聚合酶0.25 μL,灭菌超纯水40.75 μL,混匀后分装每管各24 μL,模板DNA 1μL。反应条件:94 ℃预变性2 min,94 ℃变性1 min,58 ℃退火1 min,72 ℃延伸1 min,共35个循环,72 ℃延伸2 min。扩增产物用1.5%琼脂糖凝胶,方法同文献[11],有单一阳性条带的产物,由上海生工纯化后用相应的测序引物进行双向测序。登陆PubMLST数据库下载Nm的7个管家基因的标准序列,使用DNA Star的SeqMan软件将双向测序结果拼接并加入相应基因的一个标准序列与之比对,截取与标准序列等长的待分析序列提交到PubMLST数据库http://pubmlst.org/neisseria/sequence进行分析,获取该序列的等位基因号,若与PubMLST数据库不能完全比对上的,将序列及测序文件递交至数据库以获得新的命名。每株菌株获得7个管家基因的等位基因号后按顺序排列形成等位基因谱,再次提交PubMLST数据库获取该菌株的序列型 (sequence type,ST) 及所属的ST克隆群。若等位基因谱中有1个新的等位基因号,则提交菌株的等位基因谱和相关的菌株信息到官方数据库以获取新的ST型别号。
1.4 序列分析参考文献[12]和查询PubMLST数据库中相关序列型信息,下载国际上7个高致病性Nm序列群的主要流行株等位基因谱作参照,结合海南省的序列型,采用Splits Tree 4.0软件制作进化树,分析海南省Nm变化趋势。
2 结果 2.1 菌株血清学分群 (表 1)| 表 1 海南省2005-2015年Nm来源分群情况 |
对收集的17份样本进行复苏,结果除了2005年1株、2009年的3株菌株未能复苏,1份脑脊液未能检出Nm外,其他12株分离株经鉴定均为Nm,其中3株为B群、2株为C群、2株为Y群、2株为W135群、3株为不可分群。
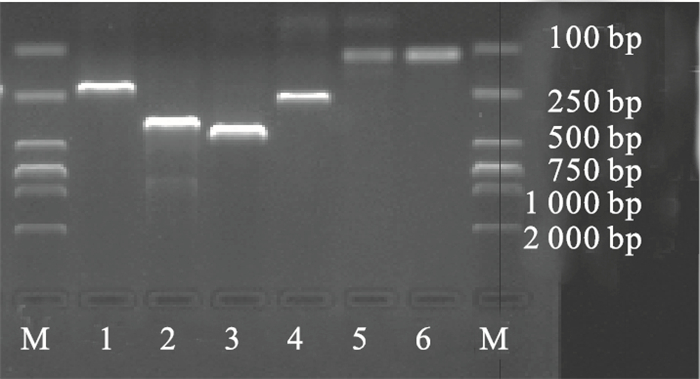
2.2 基因群分布 (表 1、图 1)
|
注:M:Marker;1:crgA;2:A群阳性对照;3:B群 (B165) 分离株;4:C群 (A103) 分离株;5:Y群阳性对照;6:W135群 (B035) 分离株。 图 1 A、B、C、Y、W135群Nm PCR扩增 |
除了2株血清学不可分群株经普通PCR分群为B群和C群各1株,1份脑脊液PCR分群为C群外,其他14株菌株PCR分群与血清学分群结果一致 (其中1株健康人群2005年阳性样本由中国疾病预防控制中心检测)。
2.3 MLST分型 (表 2、图 2)| 表 2 海南省Nm多位点序列分型结果 |
|
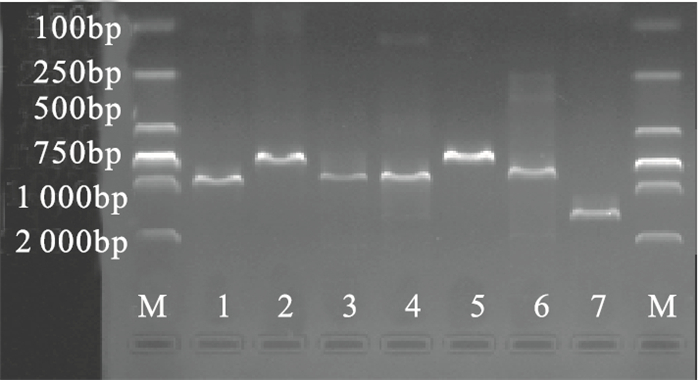
注:M:Marker;1:abcZ;2:adk;3:aroE;4:fumC;5:gdh;6:pdhC;7:pgm。 图 2 7个管家基因扩增结果 |
除了1株B群健康带菌者分离株的aroE基因换用测序引物扩增才成功,其他的样本均能成功扩增出abcZ、adk、aroE、fumC、gdh、pdhC、pgm 7个管家基因,片段大小分别为900、730、780、800、680、770、1 200 bp。17株菌株共分为11种不同ST,B群5株Nm有5种ST,其中ST-11127型和ST-11134型为新发现的ST;C群6株Nm(包括标本) 有3种ST;Y群2株、W135群3株、不可分群1株Nm均为1种ST。除了1株C群、3株B群健康带菌者分离株和1株B群病例分离株为无序列群分类 (unassigned complex STs, UA) 外,其他12株分属于ST-4821、ST-11、ST-5、ST-175、ST-364克隆群,其中前3个克隆群为高致病性克隆群,分别占29.41%(5/17)、17.65%(3/17)、5.88%(1/17)。ST-4821克隆群有ST-4821型和ST-3200型。ST-4821型来自3份C群流脑病人和1株不可分群密切接触者。ST-3200型来自2005年的C群健康带菌者。ST-11、ST-5克隆群分别只有W135群的ST-11型和不可分群的ST-7型,均来自健康带菌者。2株Y群ST-175型属ST-175克隆群,1株B群ST-8209型属ST-364克隆群,均来自健康带菌者。
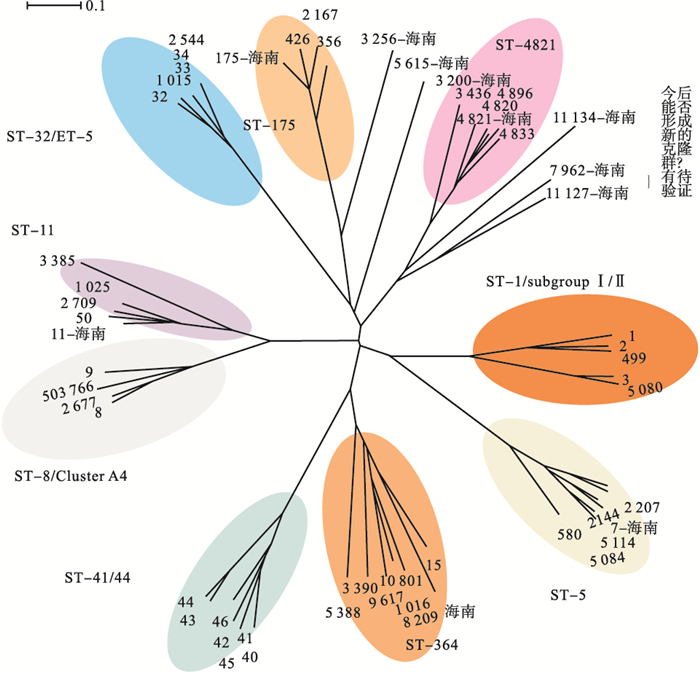
2.4 菌株进化分析 (图 3)
|
注:ST-32、ST-8、ST-41/44是欧美等发达国家的主要B、C血清群流行株[13];ST-1 /subgroupⅠ/Ⅱ是以往发展中国家的主要A群流行株。 图 3 海南省Nm序列型与全球7个高致病性克隆群所属部分序列型的相关性比较分析 |
来自2005年健康者ST-3200型与来自病人C群的ST-4821型比较有2个基因座的改变,并与ST-4821型在同一分支上。2010年来自密切接触者ST-11127型与来自2015年流脑病例的ST-7962型比较有3个基因座的改变,在同一分支上,它们与ST-11134型比较,有2个等位基因相同,均为B群无序列群分类;与C群ST-4821型比较,有3个等位基因相同。其他不同序列型的菌株进化关系较远。
3 讨论Nm是寄居于人鼻咽部的革兰氏阴性双球菌,可引起ECM和菌血症。海南省以往为ECM流行区域,曾在1962年、1967年、1977出现3次全省范围内流行。20世纪80年代开始推广使用A群ECM疫苗后,ECM发病率逐渐下降,病例呈零星、散发状态。2000-2009年,除2003年发生1例ECM病例外,其余年份均未有病例报告。自2010年以来,陆续有C群ECM确诊病例,2015年2月海南省首次报告B群ECM确诊病例。
MLST方法是通过对7个管家基因的测序结果,用核苷酸序列变异来发现细菌型别差异的分型方法[14],自1998年问世以来,已广泛用于各种细菌的分子分型,成为目前分子流行病学研究的新方法。而且MLST方法,可以直接从血清、脑脊液等临床标本中扩增出管家基因,通过测序获得等位基因图谱[3]即序列型。本研究就有1份病例样本未分离出菌株,但通过脑脊液标本核酸扩增,获得了是C群Nm核酸,测序后得到ST-4821序列型的结果,为ECM的临床诊断和流行病学监测提供了科学依据。MLST研究表明,全球Nm的7个高致病性克隆群分别是ST-1 /subgroup Ⅰ/Ⅱ、ST-5 /subgroup Ⅲ、ST-8 /Cluster A4、ST-11 /ET-37 complex、ST-32 /ET-5 complex、ST-41/44 /lineage 3[6]和ST-4821[4]。本研究发现,所有的C群ECM病例分离株或核酸样本,其序列型均是ST-4821型,均来自文昌市,与引起安徽省C群ECM爆发流行的致病株ST-4821型是同一序列型。2012年来自C群ECM病例密切接触者的分离株血清学分群为不可分群株,但PCR分群为C群,其序列型也是ST-4821型,属ST-4821高致病性克隆群。可见C群的致病株ST-4821型是海南省Nm优势流行株序列群,也是文昌市Nm的流行株序列群。而早在2005年海口市的健康人群中就已经存在属于ST-4821高致病克隆群的ST-3200型的C群菌株,其与ST-4821型相比有2个基因座的改变,因此应加强Nm的监测,尤其是疑似ECM病例的监测,及早发现病原。
从健康人群中分离的3株W135群,序列型均为ST-11型, 是高致病性菌株属ST-11高致病性克隆群,分别来自2009、2010年的海口市和2012年的文昌市。截止2015年10月12日ECM数据库里序列型ST-11已有3 546株来自全球的登记株,而W135群的ST-11克隆群是全球广为传播流行的菌株型别之一[13]。中国也于2006年开始先后在福建、广西、广东、湖南、安徽等地发现了感染W135群的ST-11型ECM病例[15],从病例的密切接触者中也分离出ST-11型Nm。海南省虽未有W135群的ECM病例,但存在着爆发流行的风险,应加强流脑菌群的监测,及时了解菌株的序列型,以便制定相应的预防控制措施。
本次研究发现有1株2012年来自文昌市健康带菌者的不可分群菌株ST-7型,属ST-5高致病性克隆群。截止2015年10月05日ST-7型在PubMLST数据库显示已有320菌株登记信息,其中8株为中国登记株,即6株C群、1株A群健康分离株和1株A群病例分离株;3株不可分群株的2株来自尼日尔的携带者,1株为阿尔及利亚病例分离株。其余309株均为世界各地的A群分离株。尽管海南省至今未培养出A群Nm,也未有A群ECM病例,但ST-5克隆群的A群菌株在中国曾引起两次大范围的流脑暴发,并在1987年通过每年的麦加朝圣开始引起世界性的大流行[13]。故应当继续加强A群、A+C群流脑疫苗的接种,提高人群免疫力,密切关注流脑菌群变迁。
本研究的B群Nm序列型较分散,且gdh基因位点718和2个ST型是MLST数据库中以前没有的。海南省2015年首次出现的B群ECM病例,为新生儿,其序列型ST-7962,与2010年来自儋州市病例 (7月龄病例的分离株未能成功复苏,已无法验证及基因分型) 密切接触者的B群Nm ST-11127型有较高的同源性,均为无序列群分类,从进化关系图上看有形成新的克隆群趋势,但这有待今后更进一步以及更多的菌株去研究验证。据文献报道,在针对某种Nm血清群疫苗的选择性压力作用下,没有疫苗预防控制的血清群菌株的发病率会随之增加。海南省已将A群、A+C群ECM疫苗纳入儿童免疫规划,有四价多糖ECM疫苗可预防由A、C、W135、Y群引起的ECM,但尚无B群ECM疫苗。
近年来,B群ECM病例在中国的发病率在逐年增加[5, 16], 如何提高人群尤其是婴幼儿抗B群ECM免疫力已成为预防ECM的关键,加速B群ECM疫苗的研发或评估已刻不容缓,同时加强ECM病原学监测,做到早发现,早处理。
志谢 文中利用splits tree 4.0软件制作的进化树,由安徽医科大学第二附属医院血液内科的晏开力协助完成,在此表示感谢| [1] | 张欣强, 李孝权, 张颖, 等. 2011广州市脑膜炎奈瑟菌分离株的分子特征分析[J]. 医学动物防治, 2012, 28(7) : 758–761. |
| [2] | 徐征, 朱兵清, 高源, 等. 中国不可分群脑膜炎奈瑟菌的分子分型分析[J]. 疾病监测, 2014, 29(9) : 688–692. |
| [3] | 王中强, 邱少富, 王勇, 等. 多位点序列分型技术及其研究进展[J]. 军事医学科学院院刊, 2010, 34(1) : 77–78. |
| [4] | Shao Z, Li W, Ren J, et al. Identification of a new Neisseria meningitides serogroup C clone from Anhui province, China[J]. Lancet, 2006, 367(9508) : 419–423. DOI:10.1016/S0140-6736(06)68141-5 |
| [5] | 邵祝军, 徐丽, 高源, 等. 中国流行性脑脊髓膜炎流行菌群变化趋势分析[J]. 中国计划免疫, 2007, 13(6) : 541–544. |
| [6] | 刘美真, 柯昌文, 管大伟, 等.2003-2011年广东省C群脑膜炎奈瑟菌MLST分子流行病学研究[C].第三界传染病防控基础研究与应用技术论坛, 2012, 267-276. |
| [7] | 杨梦, 袁辉, 徐晓倩, 等. 江西省2005-2008年C群脑膜炎奈瑟菌分子分型分析[J]. 中国流行病学杂志, 2009, 30(10) : 1095–1096. |
| [8] | 吕静, 杨红梅, 江永忠, 等. 2006-2010年湖北省流行性脑脊髓膜炎病原学和血清学分析[J]. 中国病原生物杂志, 2012, 7(4) : 287–290. |
| [9] | 鞠长燕, 刘衡川. 脑膜炎奈瑟菌分子分型方法的进展[J]. 微生物与感染, 2008, 3(2) : 118–120. |
| [10] | 中华人民共和国卫生部.WS 295-2008流行性脑脊髓膜炎诊断标准[S].北京:人民卫生出版社, 2008. |
| [11] | 王少玲, 吴捷, 刁保卫, 等. 霍乱疫情分离株流行菌型及耐药性分析[J]. 中国公共卫生, 2012, 28(1) : 79–81. |
| [12] | 晏开力, 刘丹青, 沈永刚, 等. 安徽省脑膜炎奈瑟菌的分子流行病学研究[J]. 中国疫苗和免疫, 2011, 17(3) : 201–204. |
| [13] | 孙晓芳, 杨郝亮, 周海健, 等. 中国脑膜炎奈瑟菌nadA基因多态性分析[J]. 疾病监测, 2012, 27(11) : 844–848. |
| [14] | 周晓燕, 陈燕芬, 崔步云, 等. 我国羊种3型布鲁氏菌的多位点序列分型研究[J]. 中国人兽共患病学报, 2011, 27(5) : 371–375. |
| [15] | 夏昕, 戴德芳, 湛志飞, 等. 湖南省首例W135群流行性脑脊髓膜炎病例流行病学及病原学分析[J]. 疾病监测, 2013, 28(9) : 714–716. |
| [16] | 林世平, 林一曼, 姜伊祥, 等. 1例罕见的新生儿B群流脑死亡病例的实验室结果分析[J]. 热带医学杂志, 2015, 15(5) : 603–605. |
 2017, Vol. 33
2017, Vol. 33


