近年来,关于氟中毒对机体的损害越来越引起人们的关注,在探讨氟中毒发病机理同时,也在寻求地氟病的有效防治措施。肾脏是氟的主要排泄器官,也是氟中毒靶器官[1-3]。研究发现染氟后,肾脏组织结构发生改变,肾脏细胞凋亡,DNA损伤[4]。硒是机体内一种必需微量元素,一些研究表明适量浓度的硒对氟中毒具有拮抗作用[5-7],大鼠长期饮用不同浓度配比的氟化钠(sodium fluoride,NaF)和亚硒酸钠(sodium selenite,Na2SeO3)水后,发现硒干预组肾脏细胞凋亡率显著小于单独染氟组[8]。腺苷酸激活的蛋白激酶(adenosine monophosphate-activated protein kinase,AMPK)是细胞内能量调节器,在调节能量平衡方面发挥重要作用[9-10]。线粒体作为细胞能量工厂,与AMPK存在着密切关系,而线粒体途径是主要的细胞凋亡途径[11-12]。本研究旨在探讨AMPK是否参与硒拮抗氟诱导NRK-52E细胞凋亡过程,结果报告如下。
1 材料与方法 1.1 主要试剂与仪器NaF分析纯(天津市博迪化工有限责任公司)、Na2SeO3分析纯(天津化学试剂厂)、高糖(Dulbecco′s modified Eagle medium,DMEM)培养基、噻唑蓝、细胞蛋白抽提试剂盒、超敏ECL化学发光即用型底物(武汉博士德生物公司)、胎牛血清(杭州四季青公司)、双染色法凋亡检测试剂盒(annexin v-fluorescein isothiocyanate/propidium iodide,V-FITC/PI) 凋亡检测试剂盒(南京凯基生物科技发展有限公司)、AMPK及线粒体通路蛋白抗体、辣根过氧化物酶标记山羊抗兔IgG(美国Cell Signaling 科技公司)。CO2细胞培养箱(日本 Sanyo 公司),酶标仪(美国 BIORAD 公司),FAS Calibur流式细胞仪(美国 BD 公司),电泳仪(美国 Bio-Rad 公司),凝胶电泳图像分析系统(美国 UVP 公司)。
1.2 细胞培养大鼠肾小管上皮细胞(NRK-52E)购自上海中国科学院细胞库,在37 ℃、5% CO2及一定湿度条件下,用DEME高糖培养基(含10%灭活胎牛血清,1%青链霉素)进行常规培养,2~3 d传代。
1.3 分组与处理取对数期细胞,随机分为对照组,低、高剂量氟组,低、高剂量硒组,4个硒干预组。对照组细胞只加培养基,低、高剂量氟组细胞培养基中分别含有5、20 mg/L NaF,低、高剂量硒组细胞培养基分别含有17.1、34.2 g/L Na2SeO3,4个硒干预组细胞培养基中分别含有5 mg/L NaF+17.1 g/L Na2SeO3、5 mg/L NaF+34.2 g/L Na2SeO3、20 mg/L NaF+17.1 g/L Na2SeO3、20 mg/L NaF+34.2 g/L Na2SeO3。染毒72 h。
1.4 指标与方法 1.4.1 NRK-52E细胞凋亡率检测采用流式细胞仪,每组设6个平行样,细胞以1×106个/mL密度分别接种于25 mL培养瓶中,孵育12 h后,染毒培养72 h,收集细胞,离心,磷酸缓冲盐溶液(phosphate buffer saline,PBS)清洗3次(1 000 r/min,5 min),收集1×105个/mL细胞,加入50 L结合液重悬细胞,加入5 L annexin V-FITC混匀后;加入5 L碘化丙啶,混匀,室温避光孵育10 min,上流式细胞仪检测。Cell Quest 软件获取数据计算细胞凋亡百分率。
1.4.2 NRK-52E细胞中AMPK通路蛋白表达检测采用Western blot法,每组设6个平行样,各组细胞染毒72 h后,收集细胞,细胸裂解缓冲液(radio immunopreciprecipitation assay buffer,RIPA buffer)提取蛋白,内含蛋白磷酸酶抑制剂混合物(phosphatase inhibitor cocktail 100×),二辛可宁酸试剂定量蛋白,调整浓度,煮沸变性,每孔50 L上样,10%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate palyacry lamidegel electrophoresis,SDS-PAGE),进行湿转,5%脱脂奶粉封闭2 h,一抗AMPK、p-AMPK、bax、cytochrome c (Cyt-C)、pro-caspase-9、pro-caspase-3、cleaved-caspase-9、cleaved-caspase-3(1∶1 000)和β-actin(1∶3 000),4 ℃孵育过夜,Tris盐缓冲液(tert-butyldimethylsilyl,TBS)洗膜3次,二抗IgG-羊抗兔(1∶1 000)37 ℃孵育1 h,洗膜3×10 min,超敏化学(electrogenerated chemiluminescence,ECL)显色,凝胶成像采集系统采集图像,Quantity One 4.6.6 软件分析蛋白条带,蛋白表达量用目的条带光密度(integral optical density,IOD)/β-actin IOD 表示。
1.5 统计分析数据以x±s表示,采用SPSS 13.0软件进行统计分析,多样本均数比较采用单因素方差分析,两两比较采用最小显著差法,P<0.05为差异有统计学意义。
2 结 果 2.1 硒对氟诱导NRK-52E细胞凋亡率影响对照组、5、20 mg/L NaF组、17.1、34.2 g/L Na2SeO3组、5 mg/L NaF+17.1、34.2 g/L Na2SeO3、20 mg/L NaF+17.1、34.2 g/L Na2SeO3组NRK-52E细胞凋亡率分别为(5.97±0.09)%、(7.92±0.24)%、(11.06±0.17)%、(6.74±0.49)%、(4.93±0.40)%、(8.84±0.10)%、(6.71±0.18)%、(8.46±0.09)%、(9.88±0.08)%;与对照组比较,5、20 mg/L NaF组、5 mg/L NaF+17.1 g/L Na2SeO3、20 mg/L NaF+17.1、34.2 g/L Na2SeO3硒干预组细胞凋亡率均明显升高,差异有统计学意义(P<0.05);与5 mg/L NaF组比较,5 mg/L NaF+34.2 g/L Na2SeO3硒干预组细胞凋亡率明显降低;与20 mg/L NaF组比较,20 mg/L NaF+17.1、34.2 g/L Na2SeO3 硒干预组细胞凋亡率均明显降低,差异均有统计学意义(P<0.05)。
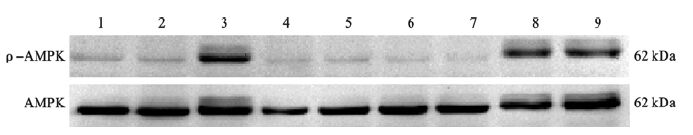
2.2 硒对氟诱导NRK-52E细胞中AMPK磷酸化水平影响(图 1)对照组、5、20 mg/L NaF组、17.1、34.2 g/L Na2SeO3组、5 mg/L NaF+17.1、34.2 g/L Na2SeO3、20 mg/L NaF+17.1、34.2 g/L Na2SeO3组NRK-52E细胞AMPK磷酸化蛋白表达水平分别为(0.16±0.05)、(0.37±0.09)、(0.73±0.16)、(0.13±0.07)、(0.14±0.08)、(0.11±0.03)、(0.12±0.04)、(0.46±0.12)、(0.48±0.15);与对照组比较,20 mg/L NaF组AMPK磷酸化蛋白水平明显升高,差异有统计学意义(P<0.05);与5 mg/L NaF组比较,5 mg/L NaF+17.1、34.2 g/L Na2SeO3 硒干预组NRK-52E细胞AMPK磷酸化蛋白表达水平明显降低;与20 mg/L NaF组比较,20 mg/L NaF+17.1、34.2 g/L Na2SeO3 硒干预组NRK-52E细胞AMPK磷酸化蛋白表达水平均明显降低,差异均有统计学意义(P<0.05)。
|
注:1:对照组;2~3:5、20 mg/L NaF组;4~5:17.1、34.2 g/L Na2SeO3组;6~9:5、20 mg/L NaF+17.1 g/L Na2SeO3组、5、20 mg/L NaF+34.2 Na2SeO3组。 图 1 硒对氟诱导NRK-52E中p-AMPK蛋白表达影响 |
2.3 硒对氟诱导NRK-52E细胞中凋亡相关蛋白表达影响(图 2)
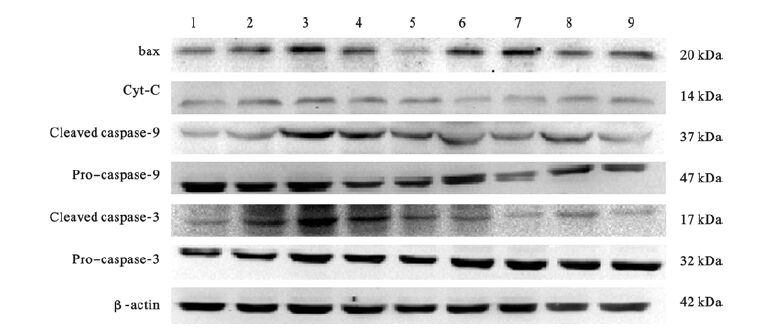
与对照组比较,20 mg/L NaF组细胞中bax蛋白表达升高(P<0.05);与20 mg/L NaF组比较,20 mg/L NaF+17.1、34.2 g/L Na2SeO3 硒干预组细胞中bax蛋白表达明显降低,差异均有统计学意义(P<0.05);与对照组比较,染氟组细胞中Cyt-C蛋白表达明显升高;与染氟组比较,硒干预组细胞中Cyt-C蛋白表达均明显降低,差异有统计学意义(P<0.05);与对照组比较,20 mg/L NaF染氟组细胞中活性caspase-9蛋白表达水平升高,5、20 mg/L NaF组活性caspase-3蛋白表达水平升高;与染氟组比较,硒干预组细胞活性caspase-9、caspase-3蛋白表达水平均明显降低,差异有统计学意义(P<0.05)。
|
注:1:对照组;2~3:5、20 mg/L NaF组;4~5:17.1、34.2 g/L Na2SeO3组;6~9:5、20 mg/L NaF+17.1 g/L Na2SeO3组、5、20 mg/L NaF+34.2 Na2SeO3组。 图 2 硒对氟诱导NRK-52E细胞中凋亡相关蛋白表达影响 |
| 表 1 硒对氟诱导NRK-52E中凋亡相关蛋白表达影响,(x±s,n=6) |
3 讨 论
细胞凋亡是一个主动的信号依赖过程,可由许多因素诱导,如放射线照射、缺血缺氧、病毒感染、药物及毒素等[13]。氟具有细胞毒性,研究证明过量氟可诱导细胞凋亡[2, 4, 14-16]。肾脏作为氟的主要排泄器官,氟对肾脏的毒性作用是多方面的[1-3],近年来有研究报道,肾小管上皮细胞调亡在慢性肾脏病的发病机制中起着重要作用[17]。硒是具有抗氧化作用的微量元素,参与保持细胞膜的稳定性和正常通透性,拮抗氟致机体损伤作用[5-6, 8, 18]。本研究结果显示,染氟组NRK-52E细胞凋亡率明显升高;与染氟组比较,硒干预组NRK-52E细胞凋亡率明显降低。提示,高浓度氟可诱导NRK-52E细胞凋亡,一定浓度的硒对氟诱导细胞凋亡具有拮抗作用。腺苷酸激活的蛋白激酶(AMPK)作为细胞能量调节器,可被许多与能量相关的因子激活,活性氧(reactive oxygen species,ROS)是AMPK的上游激活物之一[10, 19],高浓度川芎嗪(tetramethylpyrazine,TMPZ)诱导产生大量的ROS可激活AMPK[10]。机体正常情况下可产生少量ROS,当细胞受到有害刺激时,则产生大量ROS,许多研究也证实氟中毒引起氧化应激的发生,使体内超氧化物水平升高[20-21]。本研究结果显示,与对照组比较,20 mg/L NaF组NRK-52E细胞中AMPK磷酸化蛋白表达水平明显升高,硒干预组NRK-52E细胞中AMPK磷酸化蛋白表达水平明显降低。表明氟可激活AMPK,上调AMPK磷酸化表达水平,一定浓度的硒可抑制AMPK磷酸化。线粒体作为细胞能量工厂,产生ATP为细胞供能[11-12, 22],AMPK是细胞能量调节器,在维持细胞能量平衡方面起着关键作用[9-10, 19],AMPK对能量代谢的调节与线粒体功能密不可分。线粒体调节凋亡途径又称内源性凋亡,Bcl-2蛋白家族成员在其中起着重要调控作用,而bax是该家族中研究最广泛的促凋亡因子[12, 23]。在某些因素刺激下,bax 迁移至线粒体膜上,导致膜通透性改变,Cyt-C释放,经过caspases级联反应,最终导致细胞凋亡[12-13, 23]。有研究发现给予AMPK特异性阻断剂后,bax迁移活动受到抑制[10],进而阻断凋亡发生。本研究结果表明染氟组NRK-52E细胞bax蛋白表达水平增高,线粒体中Cyt-C表达增强,活性caspase-9、caspase-3表达水平明显增高;与染氟组比较,硒干预组NRK-52E细胞中bax蛋白表达水平明显降低,Cyt-C蛋白表达下降,活性caspase-9和caspase-3表达水平明显降低。综上所述,硒有助于拮抗氟所诱导的NRK-52E细胞凋亡,其机制可能与硒阻碍AMPK磷酸化,降低下游凋亡相关蛋白表达水平有关。
| [1] | Xu H, Hu LS, Chang M, et al. Proteomic analysis of kidney in fluoride treated rat[J]. Toxi Let, 2006, 160(1) : 69–75. |
| [2] | Bai C, Chen T, Cui Y, et al. Effect of high fluorine on the cell cycle and apoptosis of renal cells in chickens[J]. Biol Trace Elem Res, 2010, 138(1-3) : 173–180. DOI:10.1007/s12011-009-8599-z |
| [3] | 张颖, 于燕妮, 范彬. Wnt信号通路在氟中毒肾脏中表达及其意义[J]. 中国公共卫生, 2015, 31(5) : 590–593. |
| [4] | Song GH, Gao JP, Wang CF, et al. Sodium fluoride induces apoptosis in the kidney of rats through caspase-mediated pathways and DNA damage[J]. J Physiol Biochem, 2014, 70(3) : 857–868. DOI:10.1007/s13105-014-0354-z |
| [5] | Reddy KP, Sailaja G, Krishnaiah C, et al. Protective effects of selenium on fluoride induced alterations in certain enzymes in brain of mice[J]. J Environ Biol, 2009, 30(5) : 859–964. |
| [6] | 王裕.氟对大鼠肾小管上皮细胞的毒性作用及硒干预机制的研究[D].太原:山西医科大学硕士学位论文,2015. |
| [7] | 段鹏, 陈晋, 杨波, 等. 硒拮抗氟致大鼠肝细胞氧化应激和DNA损伤作用[J]. 中国公共卫生, 2013, 29(11) : 1626–1629. |
| [8] | Yang SY, Zhang L, Miao KK, et al. Effects of selenium intervention on chronic fluorosis-induced renal cell apoptosis in rats[J]. Biol Trace Elem Res, 2013, 15(1-3) : 237–242. |
| [9] | Yi B, Liu D, He M, et al. Role of the ROS/AMPK signaling pathway in tetramethylpyrazine-induced apoptosis in gastric cancer cells[J]. Oncology Letters, 2013, 6(2) : 583–589. |
| [10] | 易波.ROS/AMPK介导的凋亡通路在川芎嗪抗胃癌作用中的机制研究[D].南昌:南昌大学博士学位论文,2013. |
| [11] | 杨霞.AMPK参与线粒体通路介导的氟致H9c2心肌细胞凋亡机制的研究[D].太原:山西医科大学硕士学位论文,2015, |
| [12] | 唐惠玲. 线粒体介导的细胞凋亡的研究进展[J]. 安徽医药, 2012, 16(11) : 1696–1699. |
| [13] | 张峰, 罗晓星, 赵德化. 细胞凋亡的信号转导与分子调控[J]. 心脏杂志, 2002, 14(6) : 535–537. |
| [14] | Song GH, Huang FB, Gao JP, et al. Effects of fluoride on DNA damage and caspase-mediated apoptosis in the liver of rats[J]. Biol Trace Elem Res, 2015, 166(2) : 173–182. DOI:10.1007/s12011-015-0265-z |
| [15] | Song GH, Wang RL, Chen ZY, et al. Toxic effects of sodium fluoride on cell proliferation and apoptosis of Leydig cells from young mice[J]. J Physiol Biochem, 2014, 70(3) : 761–768. DOI:10.1007/s13105-014-0344-1 |
| [16] | Liu L, Zhang Y, Gu HF, et al. Fluorosis induces endoplasmic reticulum stress and apoptosis in osteoblasts in vivo[J]. Biol Trace Elem Res, 2015, 164(1) : 64–71. DOI:10.1007/s12011-014-0192-4 |
| [17] | Thomas ME, Brunskill NJ, Harris KP, et al. Proteinuria induces tubular cell turnover:a potential mechanism for tubular atrophy[J]. Kidney Int, 1999, 55(3) : 890–898. DOI:10.1046/j.1523-1755.1999.055003890.x |
| [18] | 冯佩.硒对慢性氟中毒致血液抗氧化能力损伤影响机理的研究[D].金华:浙江师范大学硕士学位论文,2012. |
| [19] | Yuan Y, Xue X, Guo RB, et al. Resveratrol enhances the antitumor effects of temozolomide in glioblastoma via ROS-dependent AMPK-TSC-mTOR signaling pathway[J]. CNS Neurosci Ther, 2012, 18(7) : 536–546. DOI:10.1111/j.1755-5949.2012.00319.x |
| [20] | 皇甫冰, 高继萍.杨霞, 等. 氧化应激与肾脏细胞凋亡[J]. 中国比较医学杂志, 2015, 25(2) : 54–60. |
| [21] | 陈杨, 于燕妮. 氧自由基与氟中毒[J]. 中国地方病学杂志, 2009, 28(2) : 234–237. |
| [22] | 刘江涛, 郭雄, 吴翠艳, 等. 线粒体细胞色素c介导的caspase-9激活通路参与大骨节病关节软骨细胞凋亡的发生机制[J]. 西安交通大学学报:医学版, 2011, 32(5) : 580–584. |
| [23] | 李捷萌, 陈彦青, 刘荣国. 线粒体凋亡途径与Bcl-2家族蛋白研究进展[J]. 医学综述, 2008, 14(4) : 489–490. |
 2017, Vol. 33
2017, Vol. 33


