结核病是世界卫生组织(World Health Organization,WHO)唯一宣布进入全球紧急状态的疾病,据2000年流行病学调查结果,中国已有5.5亿感染者,其中免疫功能正常者的10%~20%会在一生中的某个时段发病,而结核病与艾滋病双重感染者则每年的发病风险可高达>10%,故我国的结核病防控形式不容乐观[1-2]。结核分枝杆菌为结核病的病原体,主要经呼吸道传播且感染剂量极低,<10个结核分枝杆菌即可使人患病,最低感染剂量仅为1个活菌,传染性极强[3]。在国务院办公厅印发的全国结核病防治规划(2011—2015)[4]中明确规定>80%的县级结核病实验室开展痰培养、100%的地市级结核病实验室开展药敏试验、100%的省级结核病实验室开展快速菌种鉴定,因此今后从事结核分枝杆菌活菌操作的实验室数量将大大增加,相应的生物安全问题不容忽视,尤其是结核实验室终末消毒效果评价方法,我国尚缺乏相应的国家或行业标准。本研究致力于建立一种新的简易快捷的结核杆菌实验室终末消毒辅助效果评价方法,具体内容如下。
1 材料与方法 1.1 标准菌株结核分枝杆菌标准菌株(H37Rv,ATCC27294)由中国疾病预防控制中心结核病控制中心参比实验室提供。
1.2 主要试剂与仪器DNA基因组提取试剂盒(DNA Microbiome Kit,德国Qiagen公司,Cat No. 151030517);聚酯纤维拭子(美国fisher公司,Cat No.FIS23-400-122);无水乙醇(国药集团化学试剂有限公司,Cat No.10009218);PCR 反应预混液(Go Taq® Colorless Master Mix,美国Promega公司,Cat No.0000128320);琼脂糖(Vetec公司,Cat No.WXBB1741V);甲醛(国药集团化学试剂有限公司,Cat No.10010018),100 bp DNA lader(TransGen Biotech公司,Cat No.I100220)。甲醛熏蒸器(型号F50,北京克力爱尔生物有限公司);大气采样器(型号DFC-3BT,江苏建湖电子仪器仪表厂);NUAIRE生物安全柜(型号NU-430-400E,美国Nuaire公司);组织匀浆器(型号TissueLyser LT,德国Qiagen公司);超声波破碎仪(型号S30,德国 Elma公司);低温冷冻离心机(型号Z36HK,美国Thermal公司);LifeTech基因扩增仪(型号Tc-96,杭州博日科技有限公司);恒温混匀器(型号MS-100,杭州奥盛仪器有限公司),移液器(芬兰Biohit公司);涡旋震荡混合器(型号MX-F,东胜公司);凝胶成像仪(型号Bioimaging,美国UVP公司);隔水式电热恒温培养箱(型号PYX-DHS,上海跃进医疗器械厂)。
1.3 方法 1.3.1 结核分枝杆菌标准株H37Rv的活菌悬液及滤膜的制备取新鲜培养结核分枝杆菌标准株H37Rv的单个生长菌落,滴加生理盐水研磨稀释至1个麦氏比浊,再10倍稀释至10-5,制成系列菌悬液备用。取双份10-4及10-5稀释菌悬液100 μL涂7H10平板以进行菌落计数。同时取10-2稀释菌悬液1 mL经0.45 μm滤膜过滤,制备含H37Rv活菌的滤膜﹙20张﹚备用。
1.3.2 核酸提取方法 1.3.2.1 常规超声破碎法提取核酸将待提取核酸的微量离心管置于超声波破碎仪中,37 kHz 超声15 min,静置15 min后3 000 g离心5 min,取上清置于200 μL微量离心管中,备用。
1.3.2.2 完整细菌全基因组核酸的提取按DNA基因组提取试剂盒提供的方案提取,其中组织裂解部分为采用Tissue Lyser LT在50 Hz裂解10 min,并将其中第4步加入20 μL蛋白酶K,56 ℃、600 r/min孵育30 min优化为加入20 μL蛋白酶K,4 ℃孵育18 h,而后56 ℃、600 r/min孵育30 min,最后核酸洗脱体积为50 μL。
1.3.3 PCR引物设计及扩增反应条件以结核分支杆菌复合群特异性插入序列IS6110为靶标,采用Primer 5软件自主设计特异性核酸扩增引物IS6110P、并经GeneBank特异性比对后合成引物、进行聚合酶链式反应,其中上游引物序列为IS6110P-F:5′-TAC GGT GCC CGC AAA GTG-3′,下游引物序列为IS6110P-R:5′-CGC CAG CCC AGG ATC CTG CGA GCG T-3′。扩增体系组成为:1.3.2.2中提取的模板5 μL、上下游引物各1 μL(10 μmol/L)、Go Taq® Colorless Master 2×Mix 25 μL、ddH2O 18 μL,总体积50 μL。扩增条件为:95 ℃预变性10 min、35个循环,每循环中95 ℃变性30 s、60℃退火30 s、72 ℃延伸30 s,最后产物末端72 ℃延伸10 min。以1%琼脂糖电泳检测鉴定扩增产物,凝胶成像仪下观察记录结果。
1.3.4 实验室终末消毒方法操作过结核杆菌的实验室,试验完成后将实验室内温度调至>25 ℃、相对湿度70%左右时,于实验室四角及中央约1.6 m高度各放置1个含4张H37Rv活菌滤膜的平皿,而后按每立方米实验室空间使用15 mL 36%的甲醛使用量进行熏蒸。将相应体积的甲醛溶液及中和剂氨水分别加入甲醛发生器的A、B槽中,人员退出消毒区域后,关闭消毒区域与外界相通的门、传递窗以及送排风系统等,遥控启动甲醛蒸汽发生器进行熏蒸,熏蒸时间≥8 h。熏蒸后消毒区域继续密闭24 h再充分通风换气[5-6]。
1.3.5 培养法检测消毒灭菌效果 1.3.5.1 标准指示菌检测消毒灭菌效果在实验室消毒前于实验室四角及中央约1.6 m高度各放置含4张H37Rv活菌滤膜的平皿,消毒结束后首先合上平皿盖子,置于无菌密封袋中。在生物安全柜内用无菌剪刀将经甲醛终末消毒后的H37Rv活菌滤膜均分,一份用于核酸检测,一份如下述处理培养:将滤膜置于15 mL无菌离心管中,加入2 mL无菌生理盐水充分涡旋震荡3 min,而后加入等体积4% NaOH涡旋震荡30 s;静置15 min后接种酸性罗氏培养基,37 ℃培养4周观察结核分枝杆菌生长情况。
1.3.5.2 沉降法检测空气总菌落数在实验室中央以及四角约1.6 m高度各放置1个普通营养琼脂平板。琼脂开盖沉降15 min后密闭放入37 ℃培养箱培养48 h[7]。
1.3.5.3 沉降法检测结核分枝杆菌活菌数方法同沉降法检测空气总菌落数,但使用7H10琼脂取代普通营养琼脂,且在沉降结束后用封口膜密封平皿并置于密闭的塑料盒中以防干燥,培养时间为4周[8]。
1.3.6 结核分枝杆菌特异性核酸快速检测 1.3.6.1 样本采集1.3.6.1.1 标准指示菌终末消毒后样本收集 见1.3.5.1。
1.3.6.1.2 拭子擦拭样本采集 同时采用2支聚酯纤维拭子经无菌生理盐水湿润后涂抹待检物品表面,涂抹面积为平面5×5 cm2。其中对于实验室墙面、生物安全柜台面、生物安全柜外表面、实验台面、冰箱表面、实验室门等具有较大表面积的四角及中央进行涂抹采样,而对于实验台面把手、冰箱表面把手、实验室门把手以及离心机、恒温金属浴、超声波破碎仪、漩涡震荡混合器和加样器等则只对操作者经常接触的关键部位进行采样[9]。
1.3.6.1.3 空气抽滤样本采集 空气抽滤样本采集使用0.3 μm滤膜,以5 L/min的流速在1.5 m的高度于实验室的四角及中央采集1 min和5 min的样本各1次[10]。
1.3.6.2 样本预处理1.3.6.2.1 标准指示菌终末消毒后样本的预处理 将1.2.5.1中的一半滤膜置于含2 mL无菌生理盐水的无菌15 mL离心管中,充分润湿后涡旋混匀10 min,静置15 min,取悬液1 mL分置于2只1.5 mL无菌微量离心管中各0.5 mL,备用。
1.3.6.2.2 拭子擦拭样本的预处理 于生物安全柜中将每一部位采集的2支聚酯纤维拭子分别置于含0.5 mL无菌生理盐水的1.5 mL无菌微量离心管中,充分挤压后涡旋混匀5 min,备用。
1.3.6.2.3 空气抽滤样本的预处理 于生物安全柜中将空气滤膜置于含2 mL无菌生理盐水的无菌15 mL离心管中,按1.3.6.2.1的方法处理备用。
1.3.6.3 不同方法提取核酸将1.3.6.2中预处理的样本平均分为2份,分别按上述1.3.2.1和1.3.2.2的方法提取核酸。
1.3.6.4 不同方法提取核酸PCR扩增 PCR扩增反应条件同1.3.3,其中阳性对照为1.3.2.1中超声破碎的100倍稀释菌悬液。
1.3.7 结核分支杆菌分离培养验证PCR结果在生物安全柜内分别取1.3.6.2 中预处理的样本各100 μL,加入等体积4% NaOH涡旋震荡30 s,静置15 min后接种酸性罗氏培养基,37 ℃培养4周观察结核分枝杆菌生长情况。
2 结 果 2.1 H37Rv菌悬液菌落计数结果2个10-4稀释菌悬液涂布7H10平板上分别有6个和8个典型结核分枝杆菌菌落生长,10-5稀释菌悬液涂布7H10平板未见菌落生长。
2.2 不同方法提取结核分枝杆菌核酸PCR反应扩增结果2种提取方法均于10-4稀释菌悬液中扩增出阳性目的片段条带,10-5稀释菌悬液偶有扩增。
2.3 培养法检测甲醛终末消毒效果在观测时限内,标准指示菌检测消毒灭菌效果、沉降法检测空气总菌落数的普通琼脂培养和培养法检测结核分枝杆菌的7H10琼脂培养均未见细菌生长。
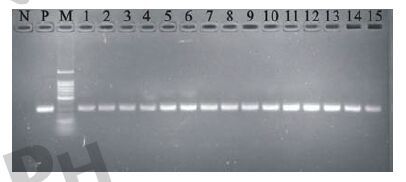
2.4 不同方法提取甲醛终末消毒后标准指示菌核酸PCR扩增结果 2.4.1 常规核酸提取扩增结果(图 1)20个标准指示菌样本及阳性对照均可见强阳性目的片段扩增条带,阴性对照无目的片段扩增条带。
|
注:N:阴性对照;P:阳性对照;M:100 bp ladder分子量标准;1~15:标准指示菌滤膜超声提取物。 图 1 常规核酸提取扩增标准指示菌电泳分析结果 |
2.4.2 完整细菌全基因组核酸提取扩增结果(图 2)
20个标准指示菌样本均未见阳性扩增条带,同时提取的阳性对照可见强阳性目的片段扩增条带。

|
注:N:阴性对照;P:阳性对照;M:100 bp ladder分子量标准;1~15:标准指示菌滤膜完整细菌全基因组提取物。 图 2 完整细菌全基因组核酸提取扩增电泳分析结果 |
2.5 不同方法提取甲醛终末消毒后实验室样本核酸PCR扩增结果 2.5.1 常规核酸提取扩增结果(图 3)
拭子样本中生物安全柜台面、实验台面、冰箱把手和门把手均检出结核分枝杆菌特异性核酸扩增条带(274 bp),其中生物安全柜的10个拭子样本中出现2次。空气抽滤样本中未见阳性扩增条带。阴性结果未列出。

|
注:N:阴性对照;P:阳性对照;M:100 bp ladder分子量标准;1、2:加样器;3、4:实验室墙面;5~8:生物安全柜台面;9:门把手;10:冰箱把手;11~15:实验室台面。 图 3 常规核酸提取扩增电泳分析结果 |
2.5.2 完整细菌全基因组核酸提取扩增结果
拭子样本和空气抽滤样本均未见阳性扩增条带,同时提取的阳性对照可见强阳性目的片段扩增条带。
2.6 结核分枝杆菌培养验证PCR结果全部拭子样品和空气抽滤样品培养均未见菌落生长。
3 讨 论目前,结核实验室消毒效果评价尚缺乏相应国家及行业标准,而随着结核病防控工作的进一步深入,今后中国将有愈来愈多的实验室开展与结核分枝杆菌活菌操作有关的实验,与其相关的生物安全问题不容忽视。而结核分枝杆菌生长缓慢,每16~18 h才分裂1次,故采用常规分离培养方法进行结核分枝杆菌实验室的终末消毒评价耗时较长,需数周至数月,影响了实验室的高效利用,故本文致力于探讨一种可快速对结核分枝杆菌实验室终末消毒效果进行辅助评价的可靠方法。
众所周知,常规核酸检测方法非常容易受到核酸污染而产生假阳性结果,尤其是甲醛熏蒸消毒主要是使消毒对象菌体的蛋白及核酸变性以达到杀灭病原微生物之目的,尽管该病原微生物已无生物活性,但仍可有部分残存游离的核酸片段被扩增而出现假阳性,因而常规核酸提取检测的方法不完全适用于甲醛熏蒸消毒的效果评价。之前有报道指出可以采用普通分子生物学检测方法进行生物安全三级实验室的甲醛熏蒸终末消毒检测[11],但该文在检测前对实验室进行了擦拭,此步骤可能影响了实验结果的客观性。本文数据亦显示,经甲醛熏蒸终末消毒后,在生物安全柜、实验台面、冰箱把手和门把手等易污染的重点部位普通分子生物学检测方法均可出现阳性扩增结果,而沉降法检测空气总菌落数及结核分枝杆菌培养结果均为阴性,证明该检测结果为假阳性,故常规核酸检测方法并不可取。
本研究针对甲醛熏蒸后结核分枝杆菌菌体蛋白变性、抵抗蛋白酶消化能力大大减弱的特点,采用Qiagen公司的DNA Microbiome Kit试剂仅提取具有完整菌体结构细菌的完整基因组核酸,并对提取方法进行了针对性的优化,适当延长消化时间以破坏残存菌体的细胞壁结构,甚至进一步消化基因组核蛋白,从而最大限度地降低死菌及残存核酸片段造成的假阳性干扰,以建立高效、便捷、可靠的辅助检测甲醛终末消毒效果的新方法。
检测结果显示,经甲醛熏蒸终末消毒后的指示菌H37Rv在采用传统方式提取核酸扩增时仍呈现强阳性,而采用本法时检测结果为阴性,与分离培养的阴性结果相一致。
经甲醛熏蒸终末消毒后的实验室现场采样检测亦显示,采用传统核酸检测方式检测时在易污染的重点部位均可出现阳性扩增结果,而本方法无阳性结果出现,与验证试验的阴性分离培养结果一致。
另外,由标准菌悬液培养计数结果可知,10-3稀释的H37Rv菌悬液浓度约为700 cfu/mL,则经过完整细菌全基因组核酸的提取后约在PCR反应体系中加入了相当于3.5 cfu的结核分枝杆菌基因组核酸进行扩增,由此可见本方法的检出限至少为3.5 cfu的活菌数,与Dalovisio等[12]的检测结果较为一致,具有较高的灵敏度。而本文采用的引物是自主设计的IS6110P,其靶基因为结核分枝杆菌复合群特异性的插入序列IS6110,该序列不但已广泛用于结核分枝杆菌的分型和分子流行病学研究,特异性高,且由于相当数量的菌型具有>1个拷贝的IS6110,故检测的灵敏度亦相应增加[13]。例如,结核分枝杆菌的标准株H37Rv即具有16个拷贝。
综上所述,本文方案可灵敏地检测出痕量的具有生物活性的结核分枝杆菌,且可在最大限度上避免由死菌和残存核酸片段造成的假阳性结果,不失为评价结核分枝杆菌实验室经甲醛熏蒸终末消毒后消毒效果的较好方法。
| [1] | 王黎霞. 中国结核病防治工作现状分析[J]. 中国公共卫生, 2012, 28(4) : 413–414. |
| [2] | 徐彩红, 富韵婷, 阮云洲, 等. 中国6省复治肺结核患者耐药情况调查[J]. 中国公共卫生, 2016, 32(1) : 59–61. |
| [3] | 中华医学会呼吸病分会. 社区获得性肺炎诊断和治疗指南[J]. 中华结核和呼吸杂志, 2006, 29(10) : 651–655. |
| [4] | 国务院.全国结核病防治规划(2011-2015年)[EB/OL].[2011-11-17].http://www.gov.cn/zwgk/2011-12/06/content_2012869.htm. |
| [5] | 韩友圻, 刘玉京. 甲醛熏蒸消毒多因素影响作用的研究[J]. 消毒与灭菌, 1989, 6(3) : 132–138. |
| [6] | 中华人民共和国卫生部.消毒技术规范[S].北京:中华人民共和国卫生部,2002. |
| [7] | 中华人民共和国卫生部.WS/T 367-2012医疗机构消毒技术规范[S].北京:中华人民共和国卫生部,2012. |
| [8] | 赵雁林, 王黎霞, 成诗明, 等. 分枝杆菌分离培养标准化操作程序及质量保证手册[M]. 北京: 人民卫生出版社, 2013: 16-35. |
| [9] | 中华人民共和国卫生部.GB/T 18204.4-2013公共场所卫生检验方法第四部分:公共用品用具微生物[S].北京:中华人民共和国卫生部,2013:11-12. |
| [10] | 王钰卓, 王雅玲, 孙力军, 等. 不同生物实验室气载真菌检测分析[J]. 中国公共卫生, 2009, 25(9) : 1149–1150. |
| [11] | 李研, 陈省平, 赖小敏, 等. 生物安全三级实验室甲醛熏蒸消毒灭菌效果评价[J]. 中国医药生物技术, 2012, 7(6) : 463–465. |
| [12] | Dalovisio JR, Montenegro-James S, Kemmerly SA, et al. Comparison of the amplified Mycobacterium tuberculosis(MTB) direct test,Amplicor MTB PCR,and IS6110-PCR for detection of MTB in respiratory specimens[J]. Clin Infect Dis, 1996, 23(5) : 1099–1106. DOI:10.1093/clinids/23.5.1099 |
| [13] | Palomino JC,Leo SC,Ritacco V.Tuberculosis from basic science to patient care (I版)[M].兰州:兰州大学出版社,2009:58-60. |
 2016, Vol. 32
2016, Vol. 32


