2. 贵州毕节医学高等专科学校预防医学教研室
2. Guiyang Medical University, Guiyang, Guizhou Province 550004, China
氟是自然界普遍存在的一种元素,是人和动物必需的元素之一,机体所需的氟量很少。若机体长期处于高氟环境中或摄入过量的氟会影响机体许多生理生化过程,氟累积在机体各组织和器官会导致不同程度的损害,引发氟中毒。氟中毒不仅影响骨骼和牙齿等硬组织,还会对全身软组织造成不同程度损害。肾脏是排泄氟的主要器官,约85%的氟由肾脏排出,肾小球对氟有滤过作用,而肾小管对氟有重吸收作用,肾脏的生理功能使之成为氟中毒容易受损的器官之一[1]。关于慢性氟中毒肾脏损伤的机制主要包括肾脏组织脂质过氧化,诱导细胞凋亡,自由基损害等。自噬(autophagy)和凋亡(apoptosis)是2个受精密调控的生物过程,在各种生物的发展、组织的平衡、疾病的发生发展中起着重要作用。自噬是细胞利用溶酶体降解自身受损的细胞器和大分子物质过程,是真核细胞特有的生命现象。被称为Ⅱ型程序性死亡。Beclin-1基因是酵母自噬基因Atg6的同系物,是哺乳动物参与自噬的特异性基因。凋亡是由基因控制的细胞自主有序死亡,亦称为程序性细胞死亡。细胞凋亡是一个主动过程,它涉及一系列基因的激活、表达与调控。细胞凋亡的激活途径有体外信号刺激和细胞内刺激2条途径。Bcl-2、Bax是细胞内刺激途径中Bcl-2家族成员。Bcl-2具有抑制凋亡作用,Bax具有促进凋亡作用。Beclin-1是一个自噬与凋亡的调节器。Beclin-1可与Bcl-2或Bcl-xl结合形成Beclin-1-Bcl-2复合物,这种复合物的形成阻碍Beclin-1介导的细胞自噬。研究发现[2-4],Beclin-1在许多肾脏疾病的发病中起重要作用。本研究通过免疫组织化学和原位杂交方法观察Beclin-1在慢性氟中毒大鼠肾组织中的表达变化,探讨自噬相关基因Beclin-1与凋亡相关蛋白Bcl-2、Bax在慢性氟中毒肾脏损伤机制中的作用,结果报告如下。
1 材料与方法 1.1 主要仪器与试剂LELCA-RM石蜡切片机(德国莱卡公司);CH20BIMF200显微镜(日本奥林巴斯公司)。兔抗鼠多克隆抗体Beclin-1(美国abcam公司)、兔抗鼠Bcl-2、Bax多克隆抗体(美国Santa Cruz公司);二氨基联苯胺(3, 3 diaminobenzidine,DAB)显色试剂盒、磷酸盐缓冲液(phosphate buffer asline,PBS)、柠檬酸盐缓冲液(pH 6.0)、3%甲醇-H2O2通用型kit(PV-6001)(北京中杉金桥生物技术有限公司);Beclin-1 mRNA原位杂交检测试剂盒、原位杂交用PBS、2×SSC、4%多聚甲醛(武汉博士德生物工程有限公司);针对大鼠Beclin-1靶基因的mRNA序列为:5'-ATGCA GGTGA GCTTC GTGTG CCAGC GCTGT AGCCA-3';5'-CAGTA CCAGC GAGAA TATAG TGAAT TTAAA AGGCA-3';5'-AACCA GATGC GCTAT GCCCA GATGC TGCTG GACAA-3'。
1.2 分组与处理选用4~5周龄,体重80~100 g健康Sprague-Dawley(SD)大鼠24只(贵州医科大学动物实验中心),许可证号:SCXK(黔)2012—0001,随机分为3组,每组8只,雌雄各半;对照组大鼠饮用自来水,含氟量<0.5 mg/L;低、高氟组大鼠分别饮用含氟化钠50、100 mg/L自来水;各组大鼠均饲以常规食料(由贵州医科大学动物实验中心提供,含氟量<1 mg/kg);大鼠自由饮水、摄食,连续9个月,将单只大鼠置于代谢笼中,收集24 h尿液测定尿氟含量;经股动脉放血处死大鼠,取一侧肾脏组织置于10%中性福尔马林中固定,梯度脱水,常规石蜡包埋;另一侧肾和股骨-80℃冰箱保存。
1.3 指标与方法 1.3.1 大鼠一般情况及氟斑牙观察实验期间定期观察大鼠一般生长发育状况;于染氟结束后,观察大鼠氟斑牙[5]发生情况:Ⅰ度:门牙表面黄白相间,白垩条纹清晰;Ⅱ度:牙表面呈无光泽、粉笔样白色斑;Ⅲ度:牙表面出现小沟、裂纹或部分脱落,牙齿呈锯齿状严重缺损。
1.3.2 大鼠尿氟、骨氟含量测定处死大鼠前24 h收集所有大鼠尿液,采用氟离子选择电极法测定尿氟含量(mg/L);处死大鼠后取大鼠股骨干骺端,采用灰化氟离子选择电极法测定骨氟含量(μg/g)。
1.3.3 大鼠肾脏形态病理学观察采用苏木素-伊红(hitalicatoxylin and eosin, HE)染色法,取已经包埋好的大鼠肾组织蜡块切片后常规脱蜡至水,苏木素染色2 min,1%盐酸酒精分化20 s,1%碳酸锂反蓝30 s,伊红染色30 s,梯度酒精脱水,二甲苯透明、中性树胶封片;光镜下观察肾脏组织的形态结构。
1.3.4 大鼠肾组织中Beclin-1、Bcl-2、Bax蛋白表达测定采用链霉素抗生物素蛋白-过氧化物酶联结法(SP法),石蜡切片置60℃恒温烤箱1 h,二甲苯中脱蜡各10 min,酒精梯度脱水,高温修复(柠檬酸盐修复),取出自然冷却至室温;3%H2O2去离子水孵育37℃10 min,BPS冲洗3 min(3次),山羊血清封闭20 min;滴加(Beclin-1、Bcl-2、1∶100,Bax 1∶200)稀释的一抗,置于4℃冰箱过夜,取出复温30 min,BPS冲洗3 min(3次),加二抗(PV6001)37℃水浴20 min,BPS冲洗3 min(3次),DAB染色约4 min,自来水冲洗2 min,擦干后滴苏木素,10 s后冲洗,酒精脱水、二甲苯透明;晾干,中性树胶封片后镜检。每组切片均设立空白对照,用PBS代替一抗作为阴性对照。Beclin-1、Bcl-2、Bax以细胞膜或细胞质内出现棕黄色颗粒为阳性表达;采用计算机图像分析软件Image J进行定量分析。在400倍镜下随机选取5个视野,每个视野选取5个阳性区域进行平均灰度值测量,阳性区表达的强弱与灰度值呈负相关。
1.3.5 大鼠肾组织中Beclin-1 mRNA表达测定采用原位杂交法(in situ hybridization, ISH),切片常规脱蜡至水;3%H2O2室温10 min灭活内源性酶;胃蛋白酶消化20 min;4%多聚甲醛溶液(含焦炭酸二乙酯)室温固定10 min;50℃温度下预杂交2 h;50℃温度下杂交过夜;在50℃温度下用2×SSC漂洗2次,0.5×SSC漂洗1次,0.2×SSC漂洗2次;滴加封闭液,37℃30 min;滴加生物素化鼠抗地高辛,室温3 h;滴加过氧化物酶,常温30 min;滴加生物素化过氧化物酶,常温30 min;DAB显色2 min,苏木素复染,中性树胶封片;以不加探针做对照。Beclin-1mRNA阳性信号定位于胞浆,显示黄色或棕黄色颗粒;采用计算机图像分析软件Image J进行定量分析。
1.4 统计分析数据以x±s表示,应用SPSS 15.0软件进行统计分析,多组间均数比较采用方差分析,方差齐性采用最小显著差法,方差不齐采用Games-Howell法,以P < 0.05表示差异有统计学意义。
2 结果 2.1 大鼠一般状况及氟斑牙检测率对照组大鼠皮毛光滑,食欲良好,活跃,牙齿无明显变化;随染氟时间延长,低氟组大鼠出现精神萎靡,食欲减退,活动度下降;高氟组大鼠精神萎靡、食欲下降比低氟组更明显,毛发无光泽。整个观察期对照组大鼠未见明显牙齿改变;染氟约1个月染氟组大鼠开始出现牙齿改变,至染毒结束时(9个月),染氟大鼠大部分出现氟斑牙,总检出率87.5%(14/16),低氟组大鼠氟斑牙检出率为75%(6/8),高氟组大鼠氟斑牙检出率为100%(8/8)。
2.2 大鼠尿氟骨氟含量变化(表 1)| 表 1 题不同剂量染氟组大鼠尿、骨氟含量变化(x±s,n=8) |
与对照组比较,染氟组大鼠尿氟、骨氟含量明显升高,差异有统计学意义(P > 0.05),呈明显剂量效应关系。
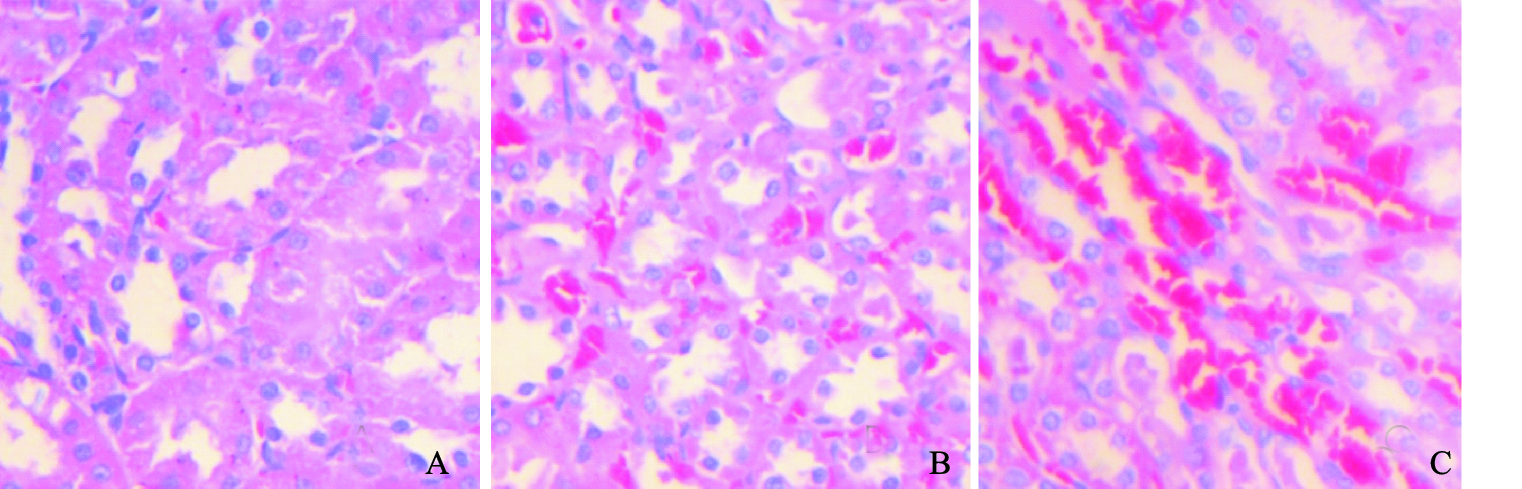
2.3 染氟对大鼠肾组织病理形态学影响(图 1)结果显示,对照组大鼠肾脏组织结构清晰、未见间质血管扩张充血(图 1A);低氟组大鼠肾皮髓质和髓质的肾小管上皮细胞可见水肿,间质血管扩张充血(图 1B);高氟组大鼠肾脏皮髓质交界处及髓质肾小管上皮细胞出现明显肿胀,间质明显充血(图 1C)。
|
注:A:对照组;B:50 mg/L染氟组;C:100 mg/L染氟组。 图 1 染氟对大鼠肾组织病理形态学影响(HE×400) |
2.4 染氟对大鼠肾组织中Beclin-1、Bcl-2、Bax蛋白表达影响(表 2)
| 表 2 染氟对大鼠肾组织中Beclin-1、Bcl-2、Bax蛋白表达影响(x±s,n=8) |
免疫组化结果显示,阳性着色定位于大鼠肾小管上皮细胞的胞质中;对照组Beclin-1阳性着色散在分布,染氟组分布较广泛;对照组Bcl-2阳性着色分布广泛,但以近曲小管上皮细胞胞质表达最强;对照组Bax阳性着色主要在肾皮髓质交接处的近曲小管上皮细胞中,低倍镜下呈一明显条带;与对照组比较,染氟组大鼠肾组织中Beclin-1、Bax表达升高,Bcl-2表达下降,差异均有统计学意义(P < 0.05),呈明显剂量效应关系。
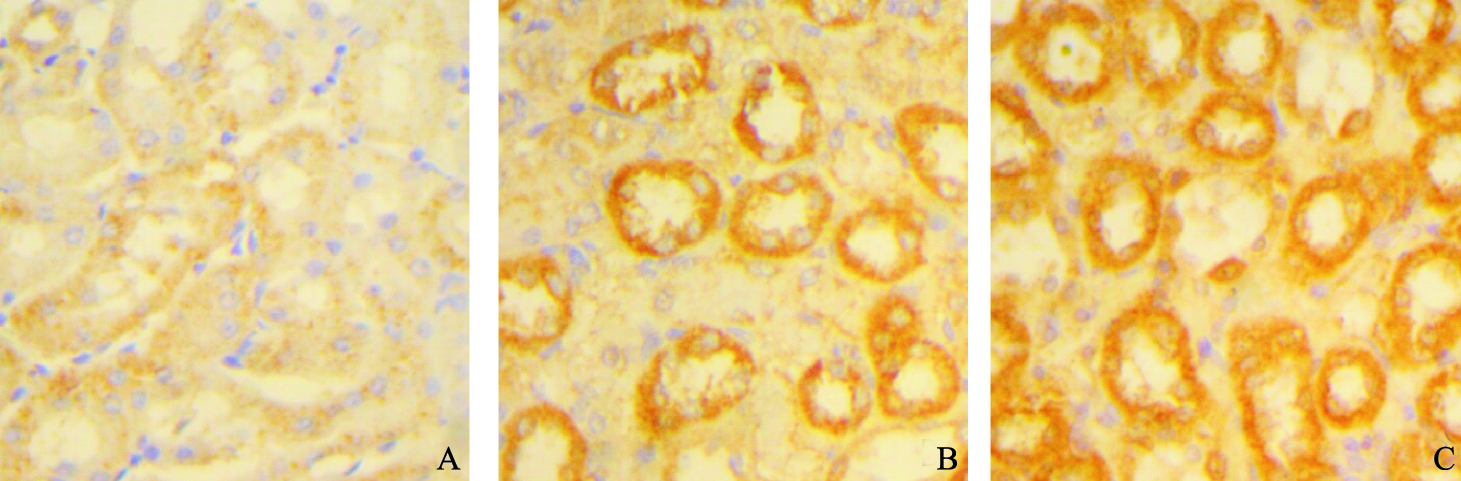
2.5 染氟对大鼠肾组织中Beclin-1 mRNA表达影响(图 2)Beclin-1 mRNA阳性表现为大鼠肾小管上皮细胞胞浆可见棕黄色粗细不等的细颗粒;对照组阳性着色散在分布,染氟组阳性着色从皮髓质交界处向肾乳头呈广泛分布。对照组、低氟组、高氟组Beclin-1 mRNA表达量分别为(179.19±11.51)、(166.94±13.21)、(146.08±17.66),与对照组比较,染氟组大鼠肾组织中Beclin-1 mRNA表达明显下降,差异有统计学意义(P < 0.05)。
|
注:A:对照组;B:50 mg/L染氟组;C:100 mg/L染氟组。 图 2 染氟对大鼠肾组织Beclin-1 mRNA表达影响(ISH,×400) |
3 讨论
本研究结果显示,采用不同浓度含氟自来水喂养大鼠9个月后,染氟组大鼠出现不同程度的氟斑牙,尿氟含量明显高于对照组,肾脏肾小管上皮细胞病理损伤明显。表明氟中毒大鼠模型复制成功。自噬是指从粗面内质网的无核糖体附着区脱落的双层膜包裹部分胞质和细胞内需降解的细胞器、蛋白质等成分形成自噬体,并与溶酶体融合形成自噬溶酶体,降解其所包裹的内容物,以实现细胞本身的代谢需要和某些细胞器的更新。研究表明自噬参与哺乳动物不同器官的生理过程及心血管疾病[6]、神经退行性变[7]、肿瘤[8]、内分泌[9]等一系列病理过程。自噬与肾脏疾病、自噬与中毒后肾损害的关系也逐渐被关注。Berkenstam等[10]在1983年首次从大鼠肾脏皮质中分离出自噬性囊泡。Chien等[11]证实自噬参与了缺血再灌注肾损伤的发生过程。此外,在肾脏缺血再灌注损伤模型中,运用3-甲基腺嘌呤、氯喹抑制自噬作用会使肾脏损伤进一步加重[12]。自噬可在饥饿、缺氧、感染、老化和氧化应激等各种应激条件的刺激下被激活,由一系列自噬相关基因(autophagy-related gene,Atg)所调控, 目前已有40个相关基因被鉴定出来[13]。Beclin-1基因是酵母自噬基因Atg6,位于人染色体17q21, 含有12个外显子。人Beclin-1含450个氨基酸,构成3个重要的结构域,分别是:Bec-2结合部位、螺旋-螺旋结构域和进化保守结构域[14],这些结构域是Beclin-1的主要功能位点。Beclin-1是形成自噬体的一个必需分子,它能够介导其它自噬蛋白定位于吞噬泡,调控哺乳动物自噬体的形成与成熟。郭秀全等[2]研究发现大鼠急性肾损伤后自噬相关蛋白Beclin-1表达上调,表明大鼠肾急性损伤后肾脏组织自噬活性上调。Wu等[15]在大鼠肾脏缺血-再灌注实验中发现在损伤的肾小管中Beclin-1和LC3表达同时增加。研究发现足细胞自噬与IgA肾病关系密切[16],自噬的异常在糖尿病肾病的发病过程中也具有重要作用[17],自噬参与了氟导致的牙损伤过程[18]。Suzuki等[19]认为自噬作为一种重要的保护性反应,有助于防止氟斑牙的形成,自噬通过JNK(c-Jun氨基末端激酶)信号通路保护造釉细胞避免氟导致的氧化损伤[20]。
Beclin-1是一种BH3蛋白,Beclin-1参与形成Ⅲ型PI3K复合物,引导自噬相关蛋白性自噬体膜靶向定位,从而促进自噬体双层膜形成,是自噬体成核的关键分子之一。抗凋亡蛋白Bcl-2具有可容纳BH3结构域的疏水凹槽,可与Bcl-2或Bcl-xl结合形成Beclin-1-Bcl-2-vps34复合物,这种复合物的形成阻碍Beclin-1介导的细胞自噬作用。在营养物质丰富条件下,Beclin-1-Bcl-2-vps34复合物稳定,但在营养物质缺乏或者其它自噬诱导信号刺激时,它们可调节Bcl-2的残基磷酸化,干扰Beclin-1-Bcl-2复合物的结合,使Beclin-1-Bcl-2复合物发生解离,使Beclin-1重新发挥诱导自噬的作用[21]。Bcl-2可与促凋亡基因Bax结合形成二聚体,二者的比例决定细胞是生存还是凋亡。细胞凋亡和自噬均有维持内环境稳定作用,在营养物质不足情况下,自噬可降解其包裹的内容物,以实现细胞代谢的需要和细胞器的更新、保护细胞不因凋亡而过早死亡。自噬可以抑制凋亡,尽可能保护细胞,但如果超过自噬能力极限,自噬可能诱导细胞发生自噬性死亡。自噬和凋亡之间可能存在相互依赖和交叉作用,共同调节细胞的生存和死亡[22]。本研究结果显示,慢性氟中毒大鼠肾小管上皮细胞的胞质中Beclin-1、Bax表达增强,Bcl-2表达降低。提示,自噬相关因子Beclin-1、凋亡相关因子Bax、Bcl-2均参与了大鼠慢性氟中毒时肾损伤的发生发展过程,但其具体机制尚待进一步研究。
| [1] | Ianoa FG, Ferreiraa MC, Quaggiob GB, et al. Effects of chronic fluoride intake on the antioxidant systems of the liver and kidney in rats[J]. Journal of Fluorine Chemistry, 2014, 168 :212–217 . |
| [2] | 郭秀全, 张惠芳, 王养民, 等. 大鼠急性肾损伤后自噬相关蛋白Beclin1的表达[J]. 医学研究杂志,2014,43 (2) :95–96. |
| [3] | 张茂平, 吴蔚桦, 张琼, 等. Beclin1在糖尿病肾病模型大鼠肾组织的表达变化研究[J]. 四川大学学报:医学版,2011,4 :508–510. |
| [4] | 范大为, 刘凯, 袁成刚, 等. Beclin-1在肾癌组织中的表达及其临床意义[J]. 中华腔镜泌尿外科杂志,2015,2 :96–100. |
| [5] | 王连方. 氟斑牙的几种“Dean氏分类法”浅析[J]. 地方病通报,2007,22 (1) :71–73. |
| [6] | Ren SY, Xu XH. Role of autophagy in metabolic syndrome-associated heart disease[J]. Biochimica et Biophysica Acta:Molecular Basis of Disease, 2015, 1852 (2) :225–231 . |
| [7] | Zuo L, Motherwell MS. The impact of reactive oxygen species and genetic mitochondrial mutations in Parkinsons disease[J]. Gene, 2013, 532 (1) :18–23 . |
| [8] | Weckman A, Rotondo F, DiIeva A, et al. Autophagy in endocrine tumors[J]. Endocr Relat Cancer, 2015, 22 (4) :205–218 . |
| [9] | Weckman A, DiIeva A, Rotondo F, et al. Autophagy in the endocrine glands[J]. Journal of Molecular Endocrinology, 2014, 52 (2) :R153–R163 . |
| [10] | Berkenstam A, Ahlberg J, Glaumann H. Isolation and characterization of autophagic vacuoles form rat kidney cortex[J]. Arch B Cell Incl Mol Pathol, 1983, 44 (3) :275–286 . |
| [11] | Chien CT, Shyue SK, Lai MK. BCL-XL augmentation potentially reduces ischemia reperfusion induced proximal and distal tubular apoptosis and autophagy[J]. Transplantation, 2007, 84 (9) :1183–1190 . |
| [12] | Jiang M, Liu K, Luo J, et al. Autophagy is a renoprotective mechanism during in vitro hypoxia and in vivo ischemia reperfusion injury[J]. Am J Pathol, 2010, 176 (3) :1181–1192 . |
| [13] | 冯文之, 陈扬, 俞立. 细胞自噬分子机制的进展[J]. 生命科学,2015,27 (7) :859–864. |
| [14] | Fu LL, Cheng Y, Liu B. Beclin-1:autophagic regulator and therapeutic target in cancer[J]. The International Journal of Biochemistry and CellBiology, 2013, 45 (5) :921–925 . |
| [15] | Wu S, Yuan L, Zhang Y, et al. Probiotic Lactobacillus rhamnosus GG mono-association suppresses human rotavirus induced in the gentobiotic piglet intestine[J]. Gut Pathog, 2013, 5 (1) :22–23 . |
| [16] | Sato S, Yanagihara T, Ghazizadeh M, et al. Correlation of autophagy type in podocytes with histopathological diagnosis of IgA nephropathy[J]. Pathobiology, 2009, 76 (5) :221–226 . |
| [17] | Wu WH, Zhang MP, Zhang F, et al. The role of programmed cell death in streptozotocin-induced early diabetic nephropathy[J]. Journal of Endocrinological Investigation, 2011, 34 (9) :296–301 . |
| [18] | Lei S, Zhang Y, Zhang K, et al. Effects of fluoride on the expression of beclin1 and mTOR in ameloblasts[J]. Cells Tissues Organs, 2015, 200 (6) :405–412 . |
| [19] | Suzuki M, Bandoski C, Bartlett JD. Fluoride induces oxidative damage and SIRT1/autophagy through ROS-mediated JNK signaling[J]. Free Radic Biol Med, 2015, 89 :369–378 . |
| [20] | Suzuki M, Bartlett JD. Sirtuin1 and autophagy protect cells from fluoride-induced cell stress[J]. Biochim Biophys Acta, 2014, 1842 (2) :245–255 . |
| [21] | 蒋炀, 徐晓晗. 细胞凋亡和自噬相互影响的研究进展[J]. 医学前沿,2012,2 (12) :57–58. |
| [22] | 董琳, 童煜, 毛萌. Bcl-2蛋白对自噬和凋亡的调控及其相关机制[J]. 医学研究杂志,2012,8 :174–177. |
 2016, Vol. 32
2016, Vol. 32


