2. 中国医科大学法医学院;
3. 中国医科大学公共卫生学院
亚硝酸盐,俗称“硝盐”,是一种在工业、建筑业和肉类食品业中广泛应用的无机化合物。亚硝酸盐分子在机体内释放出的NO2-,能使血液中正常携氧的低铁血红蛋白氧化成高铁血红蛋白,因失去携氧能力而引起组织缺氧,引起机体中毒,是法医鉴定及预防医学分析中常见的水溶性无机毒物之一[1, 2]。气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)法以其鉴别能力强、分析速度快、灵敏度高等优势,在生物样品分析中占有重要地位。但由于NO2-是水溶性无机离子,必须经过前处理使其转换成挥发性较强的物质后再进行GC-MS检测。本研究通过优化NO2-与2,3-二氨基萘(2,3-diaminonaphthalene,2,3-DAN)衍生化反应条件,旨在建立快速、准确分析尿液中NO2-离子含量的GC-MS方法,结果报告如下。
1 材料与方法 1.1 主要仪器与试剂Shimadzu GC-MS-QP2010(日本岛津公司),pH测定仪(梅特勒-托利多仪器上海有限公司);亚硝酸盐标准溶液(中国药品生物制品检定所),普罗地芬(SKF525A)内标溶液、2,3-DAN(日本和光纯药工业株式会社)。
1.2 样品前处理取0.5 mL尿液,加入pH=3的缓冲溶液1 mL,2,3-DAN 溶液10 μL,涡旋混匀,于60 ℃水浴中加热10 min,冷却后加入内标 5 μL;调pH至8.5,加入乙酸乙酯2 mL,震荡,离心,取上层液体N2气下浓缩至近干,1 μL进样GC-MS分析。
1.3 仪器条件Rtx-5毛细管柱(聚二甲基硅氧烷),10 m×0.18 mm×0.2 μm(膜厚);载气为氦气,柱前压为76.5 kPa,不分流进样;柱初始温度60 ℃,保持1 min,以15 ℃/min上升至270 ℃,保持8 min;EI(70 ev)离子源,离子源温度为200 ℃,接口温度为270 ℃,进样口温度为250 ℃,检测器温度为200 ℃,扫描间隔时间为0.50 s,质量扫描范围为40~900 m/z,扫描时间范围为0~20 min;采用全扫描(Scan)和选择离子检测(SIM)2种方式分析。内标物SKF525A特征离子为:m/z 99和m/z 86;NO2-衍生化产物特征离子为:m/z 169,m/z 141和m/z 114。
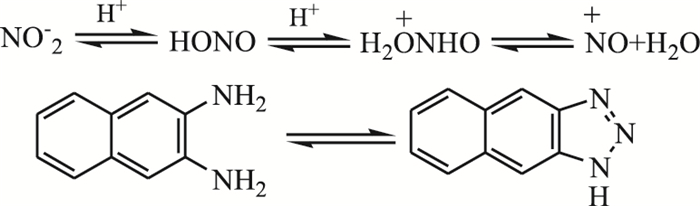
1.4 衍生化反应机制(图 1)
|
图 1 NO2-和2,3-DAN反应机制 |
反应中,2,3-DAN和NO2-发生重氮化反应,进而与另一个氨基分子内缩合成环,生成1H-萘并[2,3-d][1, 2, 3]三唑[3],产物可在National Institute of Standards and Technology(NIST)谱库检索出。
1.5 反应条件优化衍生化反应过程中,反应液pH值、温度和反应时间是影响重氮化反应的重要因素。实验中,分别采用pH=2.0、2.5、3.0、4.0、5.0、6.0、7.0、8.0的缓冲溶液,分别选择20、40、60、80 ℃不同温度下进行衍生化反应,反应时间选择5、10 min,比较不同衍生化反应条件下衍生化产物生成量,以衍生化产物生成量(反应效率)最高的反应条件为最优条件。
1.6 精密度与回收率检测分别取10.0、1.0、0.1 μg/mL 3个浓度的标准溶液进行分析。日内精密度:每个浓度的标准溶液平行分析4次,分别计算每种浓度NO2-的相对标准偏差(RSD)值;日间精密度:每个浓度的标准溶液配成5份,置于冰箱中冷藏,每天取出1份进行分析,分别计算每种浓度NO2-的RSD值。回收率:在尿液中分别加入上述3种浓度的标准溶液,每个样品平行分析4次,计算回收率。
1.7 方法比对与尿样分析分别将本方法最低检出限、线性范围、相对标准偏差等参数与文献[4]方法(以五氟苄基溴作为衍生化试剂,利用相转移催化剂加速2相之间的反应)比对,确定方法实用性。随机取2份患者尿样,均为干化学检测亚硝酸盐阳性(NIT+阳性)尿液样品,采用2,3-DAN衍生化-GC-MS联用法进行测定,验证方法准确性。
2 结 果 2.1 衍生化条件优化衍生化过程中,重氮盐可以迅速进行分子内缩合成环,形成稳定的衍生化产物。结果显示,反应液pH在2~3之间衍生化产物逐渐增加;pH=3时,衍生化产物量最多;pH>3时,衍生化产物量迅速减少;因此,pH=3为衍生化反应介质的最佳酸碱度。衍生化反应效率随着温度升高而升高,当温度大于60 ℃时,衍生化产物的响应值最高,且趋于平缓;故本方法选择60 ℃作为衍生化最佳温度。衍生化反应5 min后,衍生化产物量明显增加,在10 min后,产量增加趋势平缓;因此,选择10 min作为本方法的最佳衍生化时间。
2.2 尿液中NO2-衍生化后色谱图(图 2、3)
|
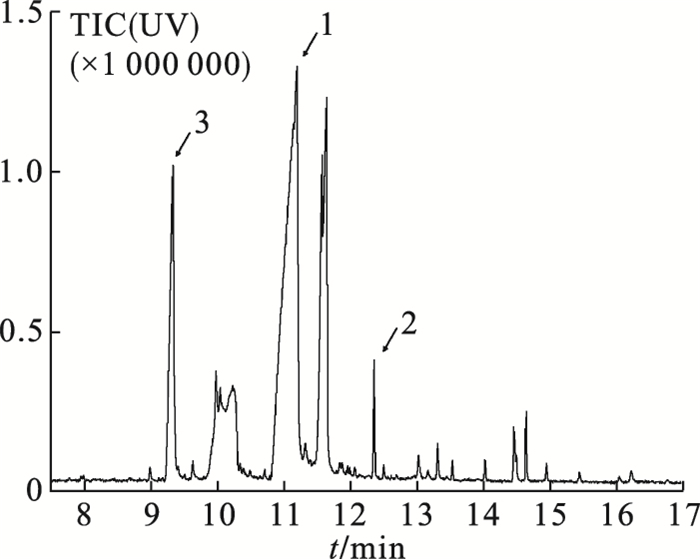
注:1:衍生化产物;2:内标;3:2,3-DAN 图 2 尿液中NO2-经2,3-DAN衍生化的总离子流色谱图 |
|
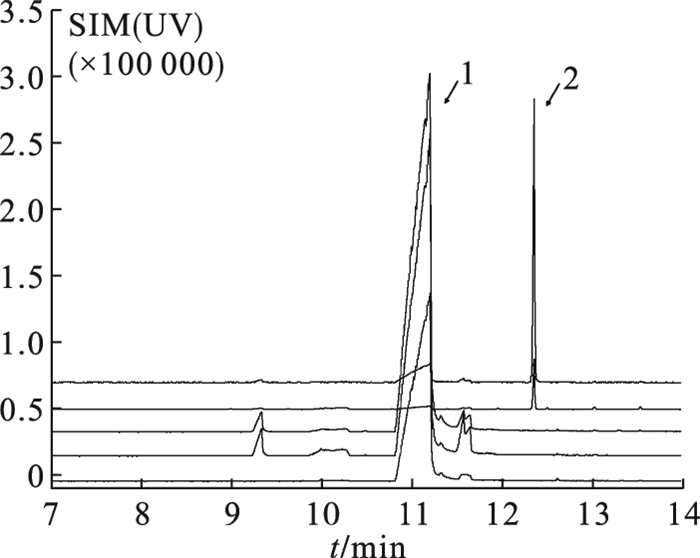
注:1:衍生化产物;2:内标 图 3 尿液中NO2-经2,3-DAN衍生化的选择离子色谱图 |
尿液中NO2-经2,3-DAN衍生化后,色谱图分离度好、灵敏度高、峰形尖锐。内标(SKF525A)保留时间为12.35 min;NO2-衍生物的保留时间为11.15 min;剩余的2,3-DAN保留时间为9.32 min。
2.3 标准曲线及检测限以标准溶液浓度为横坐标,以subscriber identity module(SIM)色谱图中NO2-衍生物m/z 141和内标m/z 86的峰面积之比为纵坐标,绘制标准曲线,线性方程为y=0.207 1x+0.006,相关系数R2=0.999;结果显示,尿溶液中亚硝酸根离子在0.01~20 μg/mL范围内线性关系良好;按照3倍信噪比计算,检测限为0.001 μg/mL。
2.4 精密度与回收率(表 1)|
|
表 1 精密度与回收率检测(%) |
结果显示,该方法日内精密度(n=4)为3.19%~4.06%,日间精密度(n=5)为3.92%~5.16%,NO2-回收率为90.31%~113.50 %。
2.5 方法比对与尿样验证(表 2)|
|
表 2 2,3-DAN衍生化法与五氟苄基溴衍生化法比较 |
结果显示,2,3-DAN衍生化-GC-MS联用法检测尿液中NO2-含量明显优于五氟苄基溴衍生化法,具有检测限低、精密度高、耗时短等特点。采用2,3-DAN衍生化-GC-MS联用法分别检测2份患者尿液(NIT+阳性)样品结果显示,NIT++、NIT+尿液样品中NO2-含量分别为3.629 6、0.691 6 μg/mL。提示,2,3-DAN衍生化-GC-MS联用法与干化学法检测结果具有良好的一致性。
3 讨 论GC-MS具有鉴别能力强、分析速度快和灵敏度高等优势,可完成复杂生物样品中痕量组分的定性和定量分析。但由于GC-MS法不能直接测定NO2-含量,故必须对其进行衍生化,转化成易挥发的化合物再进行分析。文献中亚硝酸盐的衍生化方法主要有2种:在酸催化下与芳香族化合物发生硝化反应,衍生化试剂主要有三甲氧基苯,苯,和甲苯[5, 6];烷基衍生化,衍生化试剂为五氟苄基溴(pentafluorobenzyl bromide,PFB-Br)。使用PFB-Br对NO2-进行衍生化,体系在50 ℃下反应1 h,然后用甲苯萃取进行GC/MS或GC/MS/MS分析,实验中发现硝基精氨酸类化合物对测定产生干扰,这些化合物必须经过固相萃取除去[7, 8, 9, 10, 11]。Chen等[12]通过交换离子进行萃取烷基化,测定人唾液中的NO2-,反应近3 h。使用相转移催化剂(tetradecyl dimethyl benzyl ammonium,TDMBA)来加速2相之间的反应,60 ℃水浴中反应30 min,整个操作耗时近1 h[4]。本研究结果显示,2,3-DAN衍生化法无需相转移催化剂,可直接对尿液中的NO2-进行衍生化,操作简便快捷,具有检测限更低、耗时更短、准确度和精密度高等优点。本方法适用于法医鉴定和预防医学分析领域生物样本中亚硝酸盐(NO2-)痕量检测。
| [1] | 杨光照,韩一明.一起食用亚硝酸盐超标烤肉中毒调查[J].中国公共卫生,2011,27(6):809. |
| [2] | 郭常利.一起误食亚硝酸盐食物中毒调查[J].中国公共卫生,2012,28(3):407. |
| [3] | 胡宏纹.有机化学[M].2版.北京:高等教育出版社,2006:562. |
| [4] | Kage S,Kudo K,Ikeda N.Determination of nitrate in blood by gas chromatography and gas chromatography-mass spectrometry[J].J Chromatogr B,2000,742(2):363-368. |
| [5] | Tsikas D,Fuchs i,Gutzki FM,et al.Measurement of nitrite and nitrate in plasma,serum and urine of humans by high-performance liquid chromatography,the Griess assay,chemiluminescence and gas chromatography-mass spectrometry:interferences by biogenic amines and N(G)-nitro-L-arginine analogs[J].J Chromatogr B,1998,715(2):441-444. |
| [6] | Smythe GA,Matanovic G.Specific analysis of nitrate and nitrite by gas chromatography/mass spectrometry[J].Methods Enzymol,2002,359(1):148-157. |
| [7] | Tsikas D.Measurement of nitric oxide synthase activity in vivo and in vitro by gas chromatography-mass spectrometry[J].Methods Mol Biol,2004,279(3):81-103. |
| [8] | Tsikas D.Simultaneous derivatization and quantification of the nitric oxide metabolites nitrite and nitrate in biological fluids by gas chromatography/mass spectrometry[J].Anal Chem,2000,72(2):4064-4072. |
| [9] | Tsikas D,Trettin A,Zoerner AA,et al.Simultaneous UPLC-MS/MS quantification of the endocannabinoids 2-arachidonoyl glycerol(2AG),1-arachidonoyl glycerol(1AG),and anandamide in human plasma:minimization of matrix-effects,2AG/1AG isomerization and degradation by toluene solvent extraction[J].J Chromatogr B,2011,879(17):167-171. |
| [10] | Tsikas D.Pitfalls with nitric oxide synthase activity assays and their avoidance by gas chromatography-mass spectrometry[J].Kidney Int,2015,87(4):860-861. |
| [11] | Tsikas D,Pham VV,Suchy MT,et al.No effects of atorvastatin on nitric oxide,prostacyclin,thromboxane and oxidative stress in type 2 diabetes mellitus patients of the DALI study[J].Pharmacol Res,2015,94(1):1-8. |
| [12] | Chen SH,Wu SM,Kou HS,et al.Electron-capture gas chromatographic determination of cyanide,iodide,nitrite,sulfide,and thiocyanate anions by phase-transfer-catalyzed derivatization with pentafluorobenzyl bromide[J].J Anal Toxicol,1994,18(2):81-85. |
 2016, Vol. 32
2016, Vol. 32
