手足口病(hand-foot-mouth disease,HFMD)是由人肠道病毒(human enterovirus,HEV)引起的婴幼儿感染为主的流行性传染病,临床上以发热、口腔粘膜和手、足等部位皮疹或疱疹为主要表现,少数患者可出现严重的中枢神经系统症状,个别重症患者甚至可发生死亡[1]。HEV有100多种血清型,Oberste等[2]应用分子定型方法又将其划分为HEV-A~D 4个大组。其中引起HFMD的肠道病毒有20多种血清型,以肠道病毒71型(enterovirus 71,EV71)和柯萨奇病毒A组16型(coxsackievirus A16,CVA16)为主要病原体,兼有其他肠道病毒。本研究应用Oberste的分子定型方法[2],对分离到的HEV地方株进行病毒型别鉴定及亲缘进化分析,旨在更加清晰了解天津市HFMD流行现状和病毒传播特点,为进一步加强HFMD监测提供科学依据。
1 材料与方法 1.1 材料 1.1.1 标本来源采集2013年天津市HFMD哨点医院临床诊断为HFMD的1 728例病例标本1 765份,其中粪便/肛拭子标本1 683份,咽拭子标本82份。所有标本均4 ℃冷链运输,-20 ℃保存备用。
1.1.2 主要试剂与仪器核酸RNA抽提试剂盒(上海之江生物公司,批号H20130401)、CVA16、EV71和肠道病毒通用型核酸检测试剂盒(荧光探针PCR法,江苏默乐生物公司,批号20130927)、柯萨奇A6型核酸检测试剂盒(CVA6荧光探针PCR
法,江苏硕世生物公司,批号20130501)、柯萨奇A10型核酸检测试剂盒(CVA10荧光探针PCR法,江苏硕世生物公司,批号20130501)、MEM培养基(美国GIBCO公司,批号1128853),谷氨酰胺、氨苄青霉素及链霉素(美国SIGMA公司)、PrimeScript RT-PCR Kit(大连TaKaRa公司,批号BK1901)、VP1区测序引物(invitrogen公司)。EX2400型核酸自动提取仪(上海之江生物)、ABI 7500 Fast实时荧光定量PCR仪(美国ABI公司)。
1.2 方法 1.2.1 病毒核酸检测使用上海之江生物的核酸自动提取仪提取病毒RNA,分别用HFMD三通道(EV通用型、EV71和CVA16)荧光RT-PCR检测试剂盒及CVA6、CVA10单通道荧光RT-PCR检测试剂盒在ABI7500型荧光定量PCR仪上进行核酸检测,反应体系、条件及结果判定参照试剂盒说明书。
1.2.2 病毒分离及鉴定将部分核酸检测阳性的标本进行预处理:粪便/肛拭子标本放入含10%氯仿的PBS液中,机械震荡20 min,4 000 r/min离心20 min;咽拭子标本经充分震荡后,4 ℃条件下,10 000 r/min离心20 min,取上清接种到人横纹肌瘤细胞,每日观察细胞有无细胞病变。盲传3代,待75%~100%细胞已被感染时,收集细胞进行核酸鉴定(参照1.2.1方法)。第3代仍不出现细胞病变则判为阴性。
1.2.3 病毒株VP1编码区核苷酸序列扩增提取病毒分离株核酸,使用PrimeScript RT-PCR Kit的随机引物逆转录为cDNA,以cDNA为模板,参照文献[3]合成EV71病毒VP1区扩增引物EV71-S[2372nt]: 5′-GCAGCCCAAAGAACTTCAC-3′和EV71-2A[3429nt]:5′-AAGTCGCGAGAGCTGTCTTC-3′,对 EV71分离株进行基因扩增;合成CVA16病毒VP1区扩增引物[4]CVA16-VP1-S[2335nt]:5′-ATTGGTGCTCCCACTACAGC-3′和CVA16-VP1-A[3426nt]:5′-GCTGTCCTCCCACACAAGAT-3′,对CVA16分离株进行基因扩增。反应体系及反应条件如下:10×PCR缓冲液5 μL,dNTP(10 mmol)2 μL,引物EV71-S和EV71-2A(或CVA16-VP1-S和CVA16-VP1-A)各2 μL(10 μmol),cDNA 8 μL,ExTaq酶0.5 μL,加去离子水至50 μL。在94 ℃预变性5 min后,94 ℃ 30 s,EV71 45 ℃退火40 s,CVA16 50 ℃退火40 s ,72 ℃ 1 min 20 s扩增35个循环,72 ℃延伸10 min。对非EV71和CVA16的其他肠道病毒的VP1区扩增,参照文献[5],合成HEV-A的通用引物486/488、487/489;HEV-B的通用引物490/492、491/493,分段扩增VP1区核苷酸序列。反应体系及反应条件如下:10×PCR缓冲液 5 μL,dNTP(2.5 mmol)4 μL,引物各2 μL(25 μmol),cDNA 5 μL,ExTaq酶0.5 μL,加去离子水至50 μL。在94 ℃预变性5 min后,94 ℃ 30 s,45 ℃ 30 s,72 ℃ 40 s扩增35个循环,72 ℃延伸10 min。
1.2.4 VP1区序列测定与分析所有VP1区序列测定均由上海英骏生物技术有限公司完成。序列拼接结果在RIVM网站上进行HEV型别鉴定(http://www.rivm.nl/mpf/enterovirus/typingtool)。用MEGA 4.0 软件通过Neighbor-Joining法构建基因种系发生树。相关病毒参考株的VP1区基因序列来源于NCBI GenBank。
2 结 果 2.1 HFMD病毒核酸检测结果2013年共检测HFMD疑似病例1 728例,检出阳性1 390例,总阳性率为80.44%。其中EV71 283例,阳性率为16.38%(283/1 728),阳性构成比为20.36%(283/1 390);CVA16 198例,阳性率为11.46%(198/1 728),阳性构成比为14.24%(198/1 390);CVA6 759例,阳性率为43.92%(759/1 728),阳性构成比为54.60%(759/1 390);CVA10 27例,阳性率为1.56%(27/1 728),阳性构成比为1.94%(27/1 390);其他EV 119例,阳性率为6.89%(119/1 728),阳性构成比为8.56%(119/1 390);EV71和CVA16双阳性4例,阳性率0.23%(4/1 728),阳性构成比为0.29%(4/1 390)。2013年HFMD病原谱构成与往年相比发生了较大变化。
2.2 病毒分离情况从1 390份阳性标本中随机选取352份进行病毒分离。共分离到病毒125株,分离率为35.51%(125/352)。其中分离到EV71病毒株40株,CVA16 13株,CVA6 34株,CVA10 11株,其他EV 27株。
2.3 VP1区序列测定及基因型鉴定选取5—10月(HFMD高峰期)的部分毒株进行基因测序,获得HEV-A组病毒株VP1区基因序列62个,在RIVM网站上进行HEV型别鉴定,基因定型结果显示分属于8个基因型,分别为EV71、CVA16、CVA2、CVA4、CVA5、CVA6、CVA8和CVA10;获得HEV-B组病毒株VP1区基因序列8个,基因定型结果显示分属于4个基因型,分别为CVB3、CVB5、Echo21和Echo30。
2.4 种系发生树分析(图 1~2)将HEV-A、HEV-B组天津分离株与GenBank中的各原型株和国内外代表株进行遗传进化分析,HEV-A组选用CVB3原型株Nancy为组外对照,HEV-B组选用EV71原型株BrCr为组外对照,neighbor-joining法构建种系发生树。结果显示,在各基因型中,天津分离株与中国大陆或周边亚洲国家流行株亲缘关系较近,而与原型株遗传距离较远,均处于不同的进化分支。
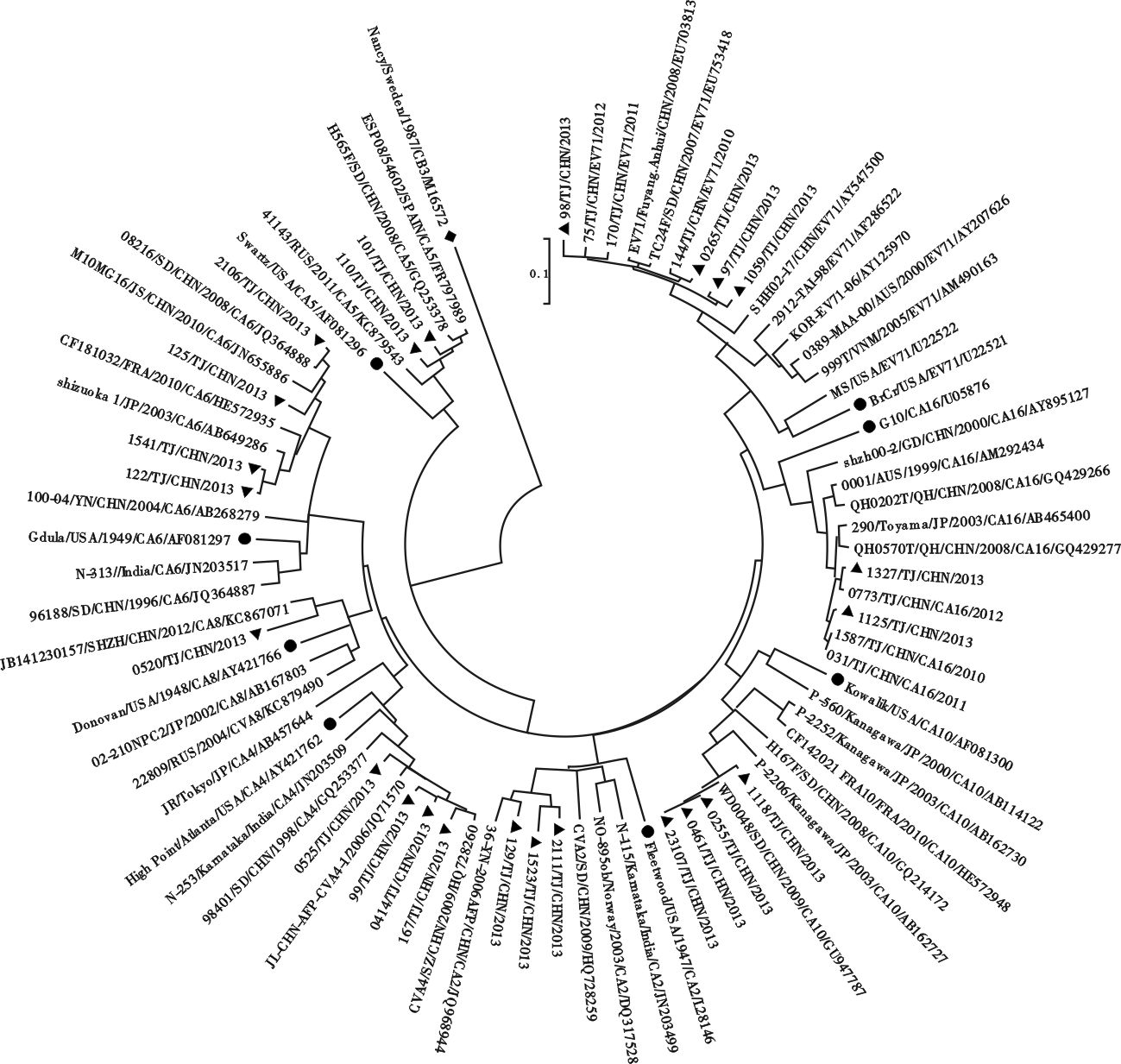
|
图 1 注:▲为2013年天津市HFMD HEV-A分离株;●为各基因型别原型株;◆为组外对照;各参考株按毒株名/分离国家/分离年代/基因型别/序列号排列。 2013年天津市HFMD HEV-A型VP1区种系发生树 |
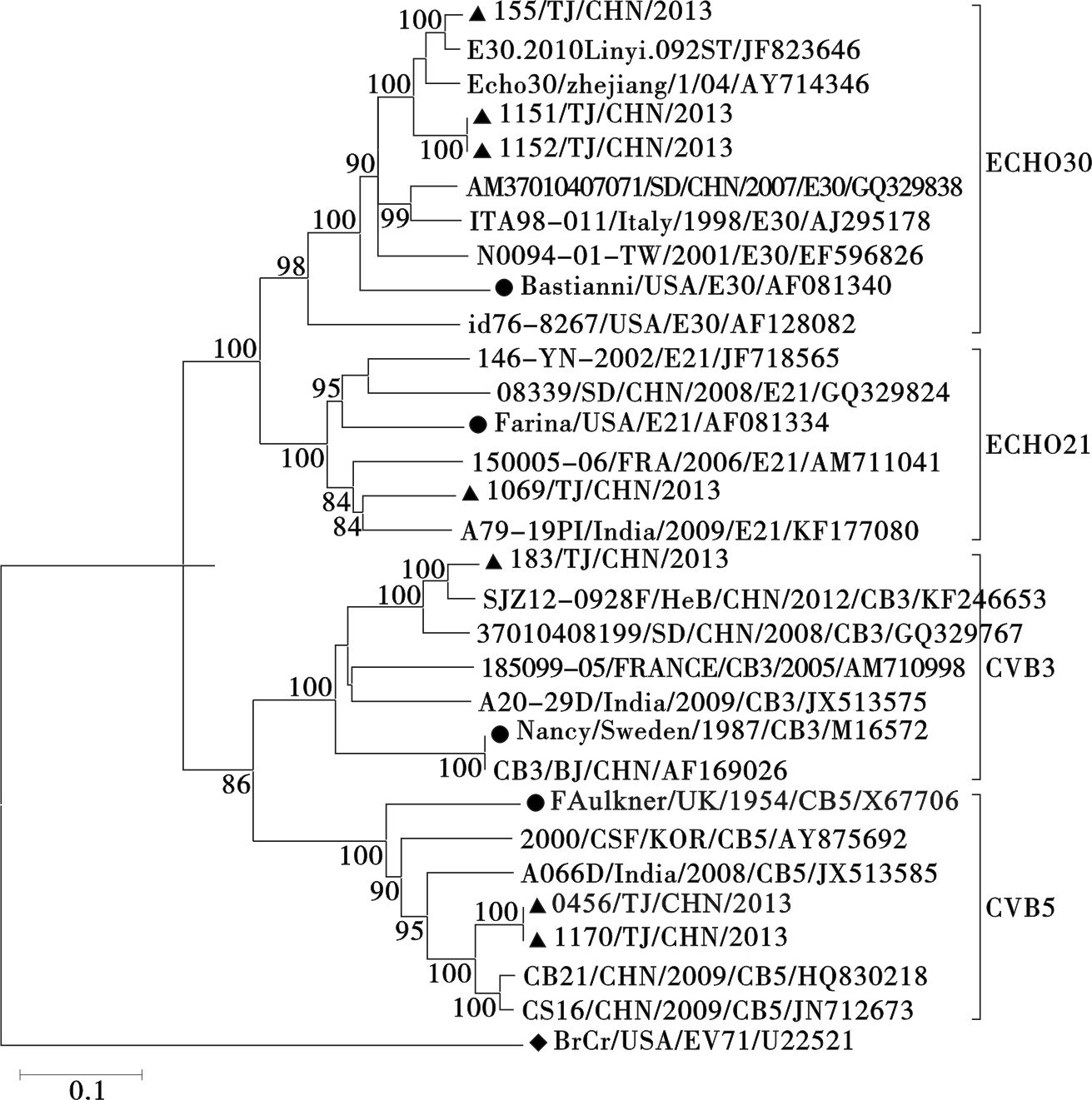
|
图 2 注:▲为2013年天津市HFMD HEV-B分离株;●为各基因型别原型株;◆为组外对照;各参考株按毒株名/分离国家/分离年代/基因型别/序列号排列。 2013年天津市HFMD HEV-B型VP1区种系发生树 |
天津市自2008年开始监测HFMD以来,流行的病原体以EV71和CVA16为主。但近年来统计数据显示,非EV71和CVA16的其他肠道病毒也占据一定比例[6]。为了更加清晰地了解天津HFMD病原谱构成及流行株的基因型和分子进化特征,2013年天津市增加了对CVA6和CVA10的监测。CVA6和CVA10主要流行于芬兰[7]、新加坡[8]、法国[9]、日本[10]等地,中国曾有小规模的暴发流行[11, 12],被认为与EV71和CVA16同样重要[13]。本研究结果表明,2013年引起天津市HFMD的病原谱构成发生了较大变化,病原体以CVA6为主,构成比达54.60%,而往年占主导地位的EV71和CVA16仅为34.89%,这可能与肠道病毒的免疫特点有关,当EV71和CVA16均达到一定的免疫保护水平后,其他肠道病毒可能会成为HFMD的优势病原体[14]。
根据Oberste的分子分型方法,2013年天津市HFMD流行主要由HEV-A 组和HEV-B组的多种肠道病毒引起。遗传进化分析显示,2013年分离到的EV71和CVA16流行株与天津市近几年的流行株在种系发生树中显示出较高的亲缘关系。其中,EV71分离株与C4a基因亚型具有最近的亲缘关系,CVA16分离株与B1b基因亚型具有最近的亲缘关系,提示2013年天津市EV71、CVA16流行株在进化上比较保守,未发生型别转换。而CVA6各分离株之间存在较大的差异,在进化树上处于3个相对独立的小分支,其中2个分支与国内江苏、山东的流行株亲缘关系较近,另一分支与日本流行株亲缘关系较近。提示CVA6基因型内可能存在着多条传播链。CVA10分离株与山东流行株有较高的亲缘关系,同属CVA10 D基因亚型,而与CVA10原型株(A基因亚型)进化距离最远;CVA2、4、5、8型分离株与中国大陆分离到的流行株亲缘关系较近,聚为相对独立的进化分支,与国外各分离株之间亲缘关系较远,提示这些分离株存在一定的地域特点,与近几年国内各基因型流行株流行趋势基本一致。
另外,对HEV-B组VP1区遗传进化分析发现,CVB3、CVB5和Echo30分离株均与国内流行株有最近的亲缘关系,区别于其他国家的流行株,聚为单独的进化分支;而Echo21分离株与印度流行株亲缘关系较近,与国内流行株亲缘关系相对较远。
综上所述,根据2013年天津市HFMD病原检测数据,天津市HFMD的病原谱构成呈多样化和复杂性的特点,应加强对HFMD其他肠道病毒的监测,了解每年的优势病毒,对HFMD的有效预防控制及治疗具有指导意义。
| [1] | 许文波,檀晓娟.手足口病:中国儿童传染病防控面临的新挑战[J].疾病监测,2009, 24(9):649-651. |
| [2] | Oberste MS,Maher K,Klipatrick DR,et al.Molecular evolution of the human enterovirus:correlation of serotype with VP1 sequence and application to picornavirus classification[J].J Virol,1999,73(3):1941-1948. |
| [3] | Zhang Y,Tan XJ,Wang HY,et al.An outbreak of hand,foot,and mouth disease associated with subgenotype C4 of human enterovirus 71 in Shandong,China[J].J Clin Virol,2009,44(4):262-267. |
| [4] | Zhang Y,Wang D,Yan D,et al.Molecular evidence of persist entepidemic and evolution of sub-enotype B1 coxsackievirus A16 associated hand,foot,and mouth disease in China[J].J Clin Microbiol,2010,48(2):619-622. |
| [5] | Oberste MS,Maher K,William AJ,et al.Species-specfic RT-PCR amplification of human enteroviruses:a tool for rapid species identification of uncharacterized enterovirises[J].J Gen Virol,2006,87(Pt1):119-128. |
| [6] | 杨东靖,李力,吕莉琨,等.天津市手足口病分子流行病学分析[J].中国公共卫生,2012,28(7):961-964. |
| [7] | Blomqvist S,Klemola P,Kaijalainen S,et al.Co-circulation of coxsackieviruses A6 and A10 in hand,foot and mouth disease outbreak in Finland[J].J Clin Virol,2010,48(1):49-54. |
| [8] | Wu Y,Yeo A,Phoon MC,et al.The largest outbreak of hand,foot and mouth disease in Singapore in 2008:the role of enterovirus 71 and coxsackievirus A strains[J].Int J Infect Dis,2010,14(12):1076-1081. |
| [9] | Mirand A,Henquell C,Archimbaud C,et al.Outbreak of hand,foot and mouth disease/herpangina associated with coxsackievirus A6 and A10 infections in 2010,France:a large citywide,prospective observational study[J].Clin Microbiol Infect,2012,18(5):110-118. |
| [10] | Fujimoto T,Iizuka S,Enomoto M,et al.Hand,foot and mouth disease caused by coxsackievirus A6,Japan,2011[J].Emerg Infect Dis,2012,18(2):337-339. |
| [11] | Lu QB,Zhang XA,Wo Y,et al.Circulation of coxsackievirus A10 and A6 in hand-foot-mouth disease in China,2009-2011[J].PLoS One,2012,7(12):1-8. |
| [12] | 刘园,李洁,杨扬,等.一起由CVA10引起的手足口暴发疫情的病原分子特征分析[J].中国卫生检验杂志,2013,23(10):2279-2282. |
| [13] | Ang LW,Koh BK,Chan KP,et al.Epidemiology and control of hand,foot and mouth disease in Singapore,2001-2007[J].Ann Acad Med Singapore,2009,38(2):106-112. |
| [14] | 赵蕾,陈敬贤,王明丽.阜阳市手足口病柯萨奇病毒A10型VP4区基因特征分析[J].中华疾病控制杂志,2013,17(6):480-483. |
 2016, Vol. 32
2016, Vol. 32


