2. 吉林医药学院临床医学院
双氢青蒿素(dihydroartemisinin,DHA)是青蒿素在体内主要的活性代谢产物,目前已作为抗疟疾药物在临床上应用。DHA的口服生物利用度高于青蒿素10倍以上,其抗疟疾作用是青蒿素的4~8倍。另外,双氢青蒿素还具有高效低毒、价格低、易天然提取等优点[1]。研究发现,DHA对肿瘤细胞具有选择性杀伤和逆转肿瘤细胞耐药性等优点[2, 3, 4]。因此,DHA有望成为抗肿瘤药物而应用于临床。本研究通过观察DHA对胶质瘤细胞生长的抑制作用,并探讨其可能机制,旨在为双氢青蒿素在临床上作为抗肿瘤药物应用提供依据。结果报告如下。
1 材料与方法 1.1 主要试剂及仪器大鼠脑胶质瘤C6细胞株(吉林医药学院科研实验中心);DHA(成都欧康植化科技有限公司),溶于二甲基亚枫(dimethyl sulfoxide,DMSO)配成50 mmol/L浓度备用;1640培养液(美国Hyclone公司);0.25%胰酶和小牛血清(美国Gibco公司);DMSO和四甲基偶氮唑[3 (4,5 dimethylthiazol 2 yl) 2,5 phenyltetrazolium bromide,MTT](美国Sigma公司);Bcl 2、Bax和caspase 3抗体 (北京中杉公司);β actin抗体(美国Santa Cruz公司)。J 26XP型超低温高速离心机(美国贝克曼公司);PLUS 384型全自动酶标仪(美国MDC公司);DNA蛋白电泳系统(美国Bio-Rad公司);Image Pro Plus 图像分析管理系统(美国Media Cybernetics公司)。
1.2 细胞培养自液氮罐中取出冻存的C6细胞,37 ℃水浴振荡融解,用含10%小牛血清的1640培养液混匀后置于25 cm2培养瓶中,37 ℃、5%CO2及饱和湿度条件下培养,隔日换液。
1.3 指标与方法 1.3.1 C6细胞生长抑制作用观察采用MTT法,将处于对数生长期的C6细胞制成单细胞悬液,按每孔6×103 个细胞密度均匀种于96孔板中,37 ℃、5%CO2及饱和湿度条件下培养过夜。 次日加入DHA 0.00(对照)、0.05、0.50、5.00和50.00 μmol/L,基础培养基用含5%小牛血清的1640培养液,分别作用24、48、72 h,每个浓度设5个复孔,实验重复3次。实验终止前每孔加入MTT 20 μL继续孵育4 h,弃上清,每孔加入DMSO 150 μL,振荡使结晶溶解,在全自动酶标仪上测定各孔490 nm处吸光度(A)值,细胞生长抑制率=DHA组A值/对照组A值×100%。
1.3.2 C6细胞凋亡率检测将生长状态良好的C6细胞按每孔2×105个密度种于6孔板中,实验设50.00 μmol/L DHA组、对照组(加入含5%小牛血清的1640培养液),置于37 ℃、5%CO2培养箱中培养48 h,收集细胞,磷酸盐缓冲液洗涤2 次,按照说明书操作,用1∶ 4 binding buffer 缓冲液190 μL重悬细胞,调整细胞浓度为1×108个/L,然后加入FITC标记的annexin V FITC 5 μL 和20 mg/L PI 10 μL,冰浴10 min,流式细胞术检测每组中10 000个细胞,计算细胞凋亡率。
1.3.3 Cyclin D1、Bax及caspase 3表达检测采用酶联免疫吸附实验,将C6细胞以4×105个密度接种于25 cm2培养瓶中,37 ℃、5%CO2及饱和湿度条件下培养过夜。次日加入DHA 0.00(对照)、 0.05、0.50、5.00、50.00 μmol/L;48 h后1 000 r/min离心5 min,收集细胞培养上清置于4 ℃冰箱中保存备用。在96孔板上以1∶ 1比例加入细胞培养上清和包被液,混匀后放于4 ℃冰箱中过夜,次日封闭后依次加入一抗(cyclin D1、Bax及caspase 3,1∶ 1 000稀释) 和二抗(羊抗兔IgG,1:1 000稀释),洗板后加入显色液避光显色,待颜色呈棕黄色时,加入终止液。振荡后在酶标仪上测定各孔490 nm处吸光度(A)值。每个浓度设5个复孔,实验重复3次。
1.3.4 Bax、Bcl 2蛋白表达检测采用Western blot法,DHA 0.00(对照)、0.05、0.50、5.00、50.00 μmol/L,处理C6细胞48 h,收集各组细胞,裂解液充分裂解细胞,以12 000 g在4 ℃条件下离心15 min,取上清,读取蛋白浓度,跑胶转膜后,封闭1 h,加入一抗(Bax、Bcl-2及-actin,1∶ 1 000稀释)过夜,次日洗涤后加入二抗(羊抗兔IgG,1∶1 000稀释)置于摇床上2 h,采用增强化学发光法发光,胶片曝光拍照。采用Image Pro Plus图像分析管理系统分析,以特异性条带平均吸光度与面积的乘积为有效值,反映蛋白表达水平。
1.4 统计分析数据以 x±s表示,采用SPSS 13.0软件进行统计分析,组间比较采用t检验,以P<0.05为差异有统计学意义。
2 结 果 2.1 DHA对胶质瘤C6细胞的生长抑制作用(表 1)≥0.05 μmol/L DHA作用C6细胞24、48、72 h时,均可抑制胶质瘤细胞生长;0.05和0.50 μmol/L DHA作用48、72 h时,C6细胞生长明显受到抑制,与对照组比较,差异有统计学意义(P<0.01);5.00、50.00 μmol/L DHA作用24、48、72 h时,细胞的生长亦明显受到抑制,与对照组比较,差异有统计学意义(P<0.05)。
|
|
表 1 DHA对C6细胞生长影响(%, x±s,n=5) |
50.00 μmol/L DHA作用于C6细胞48 h 后,细胞凋亡率为[(25.98±3.95)%],明显高于对照组[(2.32±0.78)%],差异有统计学意义(P<0.01)。
2.3 DHA对C6细胞培养上清中cyclin D1、Bax及caspase3表达影响(表 2) 与对照组比较,各浓度DHA组C6细胞培养上清中cyclin D1、Bax蛋白含量无明显变化;与对照组比较,caspase 3蛋白含量升高,差异有统计学意义(P<0.01)。
|
|
表 2 细胞培养上清中cyclin D1、Bax及caspase 3 蛋白表达( x±s,n=5) |
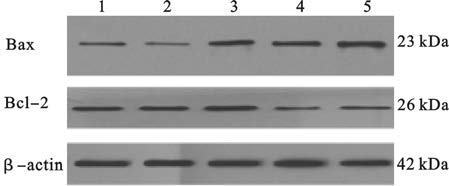
(图 1,表 3) Western blot结果显示,与对照组比较,0.05、5.00、50.00 μmol/L DHA组C6细胞中Bax表达升高、0.50、50.00 μmol/L DHA组C6细胞Bcl 2蛋白表达下降,差异有统计学意义(P<0.05);与对照组比较,0.50、5.00、50.00 μmol/L DHA组C6细胞Bax/ Bcl 2比值增加,差异有统计学意义(P<0.01)。
|
图 1 DHA对C6细胞Bax和Bcl-2蛋白表达影响 |
|
|
表 3 DHA对C6细胞Bax和Bcl 2 蛋白表达影响( x±s,n=5) |
胶质瘤是颅内最常见的原发性恶性肿瘤[5],约占颅内肿瘤的35.26%~60.90%,平均为44.60%[6]。胶质瘤生长时与正常脑组织无明显分界或位于重要的脑功能区,导致手术切除非常困难。研究表明恶性胶质瘤单纯手术的平均生存周期仅为17周,手术结合放疗可延长至37.5周,若手术、 放疗和化疗联合使用,可延长至51周[7]。现在,临床上迫切需要治疗胶质瘤更为有效的化疗方法。DHA可以抑制白血病、结肠癌、前列腺癌和乳腺癌等多种肿瘤细胞的生长[2]。但是DHA对于胶质瘤的作用及机制尚不清楚。细胞生长由细胞的生长周期决定,其中cyclin D1是生长周期的主要调控蛋白之一,其表达增加会促进细胞生长[8, 9]。本研究结果显示,不同浓度DHA对胶质瘤细胞的生长均有明显抑制作用,呈剂量依赖效应;DHA具有减少胶质瘤细胞分泌cyclin D1蛋白趋势。提示,DHA可能通过下调cyclin D1蛋白表达,从而抑制细胞的生长周期而发挥抑制肿瘤细胞生长的作用。
肿瘤细胞发生死亡时也会抑制细胞生长。在细胞的死亡方式中,凋亡是一种主要的死亡方式,其中,线粒体凋亡途径一直在诱导细胞凋亡的各途径中处于重要地位[10, 11]。研究认为DHA可能通过线粒体介导途径使肿瘤细胞凋亡[12]。DHA在体内具有抑制人卵巢癌细胞株HO 8910裸鼠皮下移植瘤的作用,其作用机制与caspase 3诱导细胞凋亡密切相关[13]。本研究结果表明DHA作用后可以明显地促进肿瘤细胞凋亡,细胞中Bax蛋白表达增加,Bcl 2蛋白表达降低,Bax/Bcl 2比值明显增加,caspase 3蛋白表达亦增加。提示,DHA可能通过增加Bax/Bcl 2比值[14],激活线粒体凋亡途径,使caspase 3活化,导致肿瘤细胞发生凋亡。
| [1] | Hou J,Wang D,Zhang R,et al.Experimental therapy of hepatoma with artemisinin and its derivatives:in vitro and in vivo activity,chemosensitization,and mechanisms of action[J].Clin Cancer Res,2008,14:5519-5530. |
| [2] | Chen PQ,Yuan J,Du QY,et al.Effects of dihydroartemisinin on fine structure of srythrocytic stages of plasmodium berghei ANKA strain[J].Acta Pharmacol Sin,2000,21(3):234-238. |
| [3] | Kim SJ,Kim MS,Lee JW,et al.Dihydroartemisinin enhances radiosensitivity of human glioma cells in vitro[J].J Cancer Res Clin Oncol,2006,132:129-135. |
| [4] | 贾立峰,李晓明.双氢青蒿素的抗肿瘤作用及机制[J].临床耳鼻咽喉头颈外科杂志,2013,27(18):1033-1036. |
| [5] | 呼格吉乐,张军力,段美庆,等.新靶点CDK2干扰RNA对人脑胶质瘤增殖影响[J].中国公共卫生,2013,29(6):855-857. |
| [6] | 张纪.深入开展胶质瘤综合治疗及其基础研究[J].中华神经外科杂志,2003,19(1):1-2. |
| [7] | Garside R,Pitt M,Anderson R,et al.The effectiveness and cost-effectiveness of carmustine implants and temozolomide for thetreatment of newly diagnosed high-grade glioma:a systematic review and economic evaluation[J].Health Technol Assess,2007,11(45):221. |
| [8] | Zuryń A,Litwiniec A,Gagat M,et al.The influence of arsenic trioxide on the cell cycle,apoptosis and expression of cyclin D1 in the Jurkat cell line[J].Acta Histochem,2014,116(8):1350-1358. |
| [9] | Gopalakrishnan N,Saravanakumar M,Madankumar P,et al.Colocalization of β-catenin with Notch intracellular domain in colon cancer:a possible role of Notch1 signaling in activation of cyclin D1-mediated cell proliferation[J].Mol Cell Biochem,2014,396(1-2):281-293. |
| [10] | Bellail AC,Qi L,Mulligan P,et al.TRAIL agonists on clinical trials for cancer therapy:the promises and the challenges[J].Reviews on Recent Clinical Trials(Online),2009(4):34-41. |
| [11] | Bi MC,Rosen R,Zha RY,et al.Zeaxanthin induces apoptosis in human uveal melanoma cells through bcl-2 family proteins and intrinsic apoptosis pathway[J].Evid Based Complement Alternat Med,2013,2013:12.205082. |
| [12] | Thomas E,Marco G,Annete M,et al.Artesunate induces ROS-mediated apoptosis in doxorubicin-resistant T leukemia cells[J].PLoS One,2007,2(8):1-8. |
| [13] | 鹿翠平,史小荣.双氢青蒿素对人卵巢癌细胞株HO-8910裸鼠皮下移植瘤的生长及caspase-3活性的影响[J].山西医科大学学报,2012,43(2):95-98. |
| [14] | 齐玲,徐俊杰,赵东海,等.西兰花多肽组分Ⅱ诱导神经胶质瘤细胞凋亡的作用及其机制研究[J].中国病理生理杂志,2014,30(9):1584-1589. |
 2015, Vol. 31
2015, Vol. 31


