2. 吉林医药学院附属医院泌尿外科 吉林 吉林 132013
核桃楸树皮、果皮具有抗肿瘤、抗炎和杀虫作用,在中国许多治疗癌症的验方中均含有核桃楸成分。胡桃醌(juglone)又名5-羟基-1,4-萘醌,是一种天然环状醌类,可从胡桃楸的叶及外壳中提取。研究表明,胡桃醌具有促进肝癌,肺癌、前列腺癌、白血病细胞凋亡等作用[1, 2, 3, 4]。卵巢癌是妇科最常见恶性肿瘤之一,死亡率居妇科肿瘤首位。尽管近年来手术及综合疗法的不断改进,对卵巢癌原发病灶的处理有了明显改善,但卵巢癌患者5年生存率仍无明显提高,可能与70%以上的卵巢癌患者诊断时,病变已发生转移有关[5]。本研究通过观察胡桃醌对人卵巢癌SKOV3细胞的侵袭能力影响,旨在为胡桃醌治疗卵巢癌临床应用提供依据。结果报告如下。
1 材料与方法 1.1 主要试剂人卵巢癌细胞SKOV3株(吉林医药学院实验中心实验室保存),属贴壁生长型细胞;胡桃醌、纤维黏连蛋白(fibronection,Fn)(美国Sigma公司);IMDM (Iscove's modified Dubecco's medium) 培养基及胰酶(美国Gibco公司);胎牛血清(杭州四季青公司);基质金属蛋白酶2(matrix metalloproteinase 2,MMP-2)和MMP-9抗体(美国EPITOMICS公司);matrigel胶(美国BD Biosciences公司);Transwell小室(德国Greiner bio-one公司)。
1.2 细胞分组与处理SKOV3细胞株于37 ℃,5% CO2培养箱中,用IMDM+10%胎牛血清培养,隔日换液,取对数生长期细胞进行实验。实验设对照组、12.5、25.0、50.0、100.0 μmol/L组,每组设3个复孔。
1.3 SKOV3细胞增殖能力检测采用噻唑蓝(MTT )比色法,取对数生长期细胞,调整细胞浓度为1×105个/mL,体积为200 μL,接种于96孔板内,于37 ℃、5%CO2条件下培养。加入不同浓度胡桃醌培养液,体外培养24 h后,加入MTT,测定吸光度(A)值,实验重复3次,增殖抑制率(%)=(1-胡桃醌组A值/对照组A值) × 100%。
1.4 细胞黏附率检测将纤维黏连蛋白用磷酸盐缓冲液(phosphate buffered saline,PBS)稀释为100 mg/L,每孔100 μL包被于96孔板中,37 ℃包被2 h,用PBS洗涤2次,1%牛血清白蛋白封闭2 h;不同剂量胡桃醌处理细胞24 h,收集细胞,以无血清培养基制成单细胞悬液,调节细胞浓度为3×108个/L,加入包被培养板中,每孔200 μL,置37 ℃、5%CO2培养箱中孵育2 h;轻轻洗去未黏附细胞,用10%中性甲醛100 μL固定30 min;每孔加0.5% 结晶紫100 μL,室温染色2 h,蒸馏水洗涤1次,阴干后每孔加入2%十二烷基硫酸钠溶液100 μL,酶标仪570 nm波长测定各孔吸光度(A)值。细胞黏附率=(胡桃醌组A值/对照组A值)×100%。
1.5 细胞体外侵袭能力检测采用Transwell法,取对数生长期SKOV3细胞,用含0.1%小牛血清的IMDM培养液制成3×108个/L细胞悬液,各组分别吸取200 μL接种于上层小室,将其置于灭菌的24孔板,下室加入含10%小牛血清的IMDM培养液600 μL;培养24 h后,弃去上室原有培养液,分别加入不同浓度胡桃醌,继续培养24 h,将上室面的细胞和matrigel胶用湿棉签擦掉,膜用4%多聚甲醛固定30 min,结晶紫染色20 min,PBS冲洗3次,显微镜下观察并拍照;将小室浸没于500 μL 33%醋酸中脱色20 min,测量洗脱液A570值,代表穿过细胞数量。
1.6 细胞中MMP-2、MMP-9表达检测采用Western blot 法,取30 μg蛋白进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳,将凝胶上蛋白移至醋酸纤维素膜,于50 g/L 脱脂奶粉中4 ℃封闭过夜,加兔抗MMP-2和MMP-9抗体(1:1000),小鼠抗β-actin 抗体(1:3000),4 ℃过夜;Tris-HCL-Tween洗膜,分别加辣根过氧化物酶 标记的山羊抗兔抗体(1:3000)室温避光孵育2 h;TBST洗膜后,加底物发光显影。使用Quantity One软件扫描并做灰度分析。
1.7 统计分析数据采用(x±s)表示,采用SPSS 11.0软件进行统计分析,组间比较采用单因素方差分析,两两比较采用t检验,以 P<0.05 为差异有统计学意义。
2 结 果 2.1 胡桃醌对SKOV3细胞生长抑制作用结果显示,以对照组SKOV3细胞增殖率为100%,12.5、25、50、100 μmol/L胡桃醌对SKOV3细胞增殖抑制率分别为(16.8±3.4)%、(39.6±9.7)%、(63.3±13.6)% 和(84.5±17.3)%;与对照组比较,各剂量胡桃醌对SKOV3细胞增殖具有明显抑制作用,且呈剂量效应关系。
2.2 胡桃醌对SKOV3细胞黏附、侵袭力影响(表 1)| 表 1 胡桃醌对SKOV3细胞黏附、侵袭力影响(x±s,n=3) |
与对照组比较,胡桃醌浓度≥25 μmol/L时,SKOV3细胞黏附率逐渐降低,差异有统计学意义(P<0.05),呈剂量效应关系;与对照组比较,25、50、100 μmol/L 胡桃醌组穿过matrigel胶的SKOV3细胞数量明显下降,提示胡桃醌浓度≥25 μmol/L时,SKOV3细胞侵袭力逐渐降低。
2.3 胡桃醌对SKOV3细胞MMP-2和MMP-9表达影响(图 1)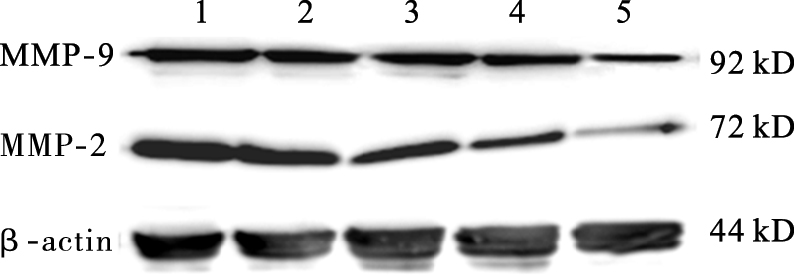 | 注:1:对照组;2~5:胡桃醌12.5、25.0、50.0、100.0 μmol/L组。 图 1 胡桃醌对SKOV3细胞内MMP-2和MMP-9蛋白表达影响 |
结果显示,对照组、胡桃醌12.5、25.0、50.0、100.0 μmol/L组SKOV3细胞MMP-2和MMP-9表达分别为(0.76±0.04)、(0.65±0.03)、(0.58±0.02)、(0.40±0.02)、(0.24±0.01)与(0.76±0.04)、(0.70±0.03)、(0.59±0.02)、(0.45±0.03)、(0.27±0.02);与对照组比较,胡桃醌25.0、50.0、100.0 μmol/L组SKOV3细胞内MMP-2表达下降、胡桃醌50.0、100.0 μmol/L组SKOV3细胞内MMP-9表达下降,差异有统计学意义(P<0.05)。
3 讨 论侵袭、转移是恶性肿瘤的重要生物学特性之一,也是肿瘤复发、治疗失败最终患者死亡的主要原因。研究表明,肿瘤的侵袭和转移是多因素和多步骤过程。首先细胞与细胞外基质(extracellular matrix,ECM) 黏附,其次通过诱导宿主细胞分泌蛋白酶水解细胞外基质,最后细胞运动和迁移[6]。纤维粘连蛋白(fibronectine,FN)是基底膜的一种成分,肿瘤细胞从母体脱离后,侵袭基底膜及细胞外基质,通过膜表面受体可粘附于FN上而产生运动与迁移,使肿瘤扩散与转移。除粘附以外,肿瘤细胞在侵袭过程中分泌多种水解酶降解ECM。基质金属蛋白酶(matrix metalloproteinases,MMPs)能降解细胞外基质中各种蛋白成分和胞外蛋白,是侵袭过程中主要的蛋白水解酶。一般认为与肿瘤侵袭、转移关系最密切的是MMP-2和MMP-9[7]。MMP-2和MMP-9活性表达增高,降解基底膜中的Ⅳ型胶原是癌细胞侵袭与转移的关键步骤。
胡桃醌是从核桃楸中提纯的一种天然成分,在体外具有抗肿瘤细胞活性。SKOV3 是能够同时表达MMP-2 和MMP-9 的高转移人卵巢粘液囊腺上皮癌细胞,其MMP-2、MMP-9 表达水平与细胞的恶性程度、侵袭与转移特性、血管内皮生长因子等癌血管生成因子呈正相关[8]。本研究结果表明,不同浓度胡桃醌可使人卵巢癌SKOV3细胞黏附率下降;Transwell实验证实胡桃醌能够抑制SKOV3细胞穿过matrigel胶的能力,表明胡桃醌能够抑制细胞侵袭;随着胡桃醌剂量增加,SKOV3细胞内MMP-2和MMP-9蛋白表达水平逐渐下降。提示胡桃醌可能通过抑制MMP-2和MMP-9蛋白表达,降低SKOV3细胞黏附与侵袭力。
| [1] | 赵行宇,杨森,周丽霞,等.胡桃醌对肝癌HepG2细胞的增殖抑制及诱导凋亡作用[J].吉林大学学报,2013,2(3):255-258. |
| [2] | 孔陵生,邹翔,季宇彬.青龙衣中胡桃醌对A549细胞周期及凋亡影响[J].哈尔滨商业大学学报:自然科学版,2008,6(12):641-644. |
| [3] | 方芳,王立国,张巍,等.胡桃醌对人前列腺癌PC-3细胞抑制作用[J].中国公共卫生,2013,29(10):1458-1460. |
| [4] | Xu HL,Yu XF,Qu SC,et al.Juglone,from Juglans mandshruica Maxim,inhibits growth and induces apoptosis in human leukemia cell HL-60 through a reactive oxygen species-dependent mechanism[J].Food Chem Toxicol,2012,50(3-4):590-596. |
| [5] | 李慧玲,苏亚娟,邬剑,等.MMP-2、VEGF在卵巢癌组织中的表达及其临床意义[J].中国实验诊断学,2009,13(6):726-729. |
| [6] | Liotta LA.Tumor invasion and metastasis role of the extracellular matrix:Rhoads memorial award lecture[J].Cancer Res,1986,46(1):1-7. |
| [7] | 张明明,徐玉清.MMP-2和MMP-9在恶性肿瘤中的研究进展[J].国际肿瘤学杂志,2012,39(11):820-823. |
| [8] | Lengyel E,Schmalfeldt B,Konik E,et al.Expression of latent matrix metalloproteinase 9(MMP-9) predicts survival in advanced ovarian cancer[ J].Gynecol Oncol,2001,82(2):291-298. |
 2015, Vol. 31
2015, Vol. 31


