2. 皖北矿务局煤电集团总医院普外科;
3. 贵州省疾病预防控制中心
热休克蛋白(heat shock protein,HSP) 是生物体在高温或者其他类型的胁迫诱导细胞合成或表达量改变的一类蛋白,最早是由Ritossa 对果蝇进行热诱导时发现的[1],能起到稳定和保护其他蛋白质“分子伴侣”的作用[2]。HSP根据分子量的大小分为不同的亚型,分子量介于12~43 kDa 的HSP被称为小热休克蛋白(small heat shock protein,sHSP)[3]。其中sHSP20具有松弛血管平滑肌、抑制血小板聚集等多重功能[4]。HSP20是一个极具多样的家族,广泛分布于自然界中,不同的物种含有不同的sHSP,而且不同的组织,其表达量也会不一样。不论机体处于何种状态,sHSP均有相应的表达,参与机体的生物学过程,具有独特的生理作用[5]。家蝇在世界范围内广泛分布,是许多人类和动物疾病的传播媒介。有研究表明,家蝇可以携带并传播多种病原生物[6, 7, 8, 9],而其自身却很少患病,为研究家蝇这种免疫特性,本研究对家蝇HSP20基因及其编码的蛋白质结构和特征进行研究,为进一步研究该基因的功能奠定基础。结果报告如下。 1 材料与方法 1.1 材料 1.1.1 实验材料
家蝇,由贵阳医学院寄生虫教研室常规饲养;载体PEASY-E1购于北京全式金生物公司,大肠杆菌菌株DH5α、OrigmiB/DE3由贵阳医学院寄生虫教研室常规保存。 1.1.2 主要试剂和仪器
限制性内切酶、T4连接酶、rTaq酶、dNTPs、DNA marker、protein marker、PCR产物胶回收试剂盒、DNA产物纯化试剂盒、质粒小量提取试剂盒均购于大连宝生物科技公司;其他试剂均为国产分析纯。隔水式电热恒温培养箱(上海跃进医疗器械厂);数显不锈钢电热培养箱(上海博讯实业); PCR扩增仪(德国Eppendorf公司);稳压稳流电泳仪(美国GE公司);紫外分光光度计(美国GE公司);Millipore 0.22 μm/0.45 μm滤器(美国Merck Millipore公司);Milli-Q超纯水仪(法国Mill-ipore Pharmacia公司)。 1.1.3 引物合成和DNA测序
基因扩增引物和重组质粒DNA测序由上海生物工程有限公司完成。 1.2 方 法 1.2.1 HSP20基因的识别
利用美国国家生物技术信息中心(http://www.ncbi.nlm.nih.gov/)网站的开放阅读框探寻器确定其完整编码序列和编码的氨基酸序列。利用瑞士生物信息学研究所的蛋白分析专家系统(http://ca.expasy.org/)所提供的蛋白质在线分析工具,如protparam (http://au.expasy.org/tools/protparam.html)预测氨基酸序列的分子量、等电点、稳定性指数等理化性质,InterPro Scan(http://www.ebi.ac.uk/InterProScan/)预测氨基酸序列中的功能域。 1.2.2 HSP20基因的扩增
利用prmer5.0软件,根据GenBank(登录号:XM_005190903) 上家蝇HSP20基因序列和PEASY-E1多克隆位点设计特异性引物如下:HSP20F:ATGTCCGTAGTGCCCCTAATGTTCCGTGATTGGTGG;HSP20R:TTA-GGCAGTAGTAGTCTCAACCTTCTTTTCTTTA。以热胁迫后家蝇3龄幼虫提取RNA,逆转录cDNA为模板进行PCR扩增。PCR条件:94 ℃预变性5 min,94 ℃ 30 s、55 ℃ 30 s、72 ℃ 30 s,共30个循环,最后72 ℃延伸10 min。扩增产物用2%琼脂糖凝胶电泳回收。 1.2.3 重组原核表达质粒的构建及鉴定
将PCR产物胶回收,按一定比例与原核表达质粒PEASY-E1连接,转化大肠杆菌OrigmiB/DE3感受态细胞,氨苄青霉素筛选阳性克隆。对阳性克隆提取质粒进行PCR、双酶切和测序鉴定。 1.2.4 PEASY-E1-HSP20在大肠杆菌Origmi/DE3中的诱导表达
取50 μL培养过夜的阳性克隆菌液,加入含氨苄青霉素的 5 mL LB培养基中(菌液/培养基为1/100),37 ℃、250 r/min振摇至A600为0.6时,加入异丙硫代-β-D半乳糖苷(isopropyl-beta-D-thiogalactopyranoside,IPTG)至终浓度0.25 mmol/L诱导表达12 h。离心收集菌体,在沉淀中加入80 μL×SDS-PAGE上样缓冲液,煮沸8~10 min,12 000 r/min离心取上清10 μL进行十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis,SDS-PAGE)分析。 1.2.5 重组蛋白的大量诱导、纯化
按照上述方法对阳性克隆进行大量诱导表达,离心收集菌体,按每克菌体加入3mL细菌细胞壁裂解液重悬菌体,反复冻融后冰上超声裂解(功率150 W,持续1 s,停3 s,共180 s),4 ℃、12 000 r/min,离心20 min后收集上清,分别取上清和沉淀样品处理后行SDS-PAGE判断该重组蛋白的可溶性。并收集上清,用0.45 μL滤膜过滤,参照镍离子金属螯合剂亲和层析柱说明书进行蛋白纯化,收集蛋白洗脱液,再将洗脱的目的蛋白在PBS透析液(pH 7.4)中4 ℃透析24 h。并根据说明书,用Bradford法对经过以上步骤获得的重组蛋白进行蛋白定量,于-80 ℃保存备用。 2 结 果 2.1 HSP20基因序列及蛋白质的理化性质分析(图 1)
HSP20基因序列全长865 bp,包含一个完整的最大开放阅读框(open reading frame,ORF)为567 bp,编码188个氨基酸。ExPASy中ProtParam预测HSP20的理论分子量21 443.2 Da,其等电点为5.96。280 nm处的摩尔消光系数为24 980 M-1 cm-1,0.1%浓度的ABS为1.165。若其成熟肽N-末端为蛋氨酸时,在哺乳动物网状细胞体外表达的半衰期为30 h,在酵母和大肠杆菌中表达的半衰期分别>20和10 h。在溶液中HSP20的不稳定指数为59.81,高于阈值40,其性质不稳定;HSP的疏水指数为72.45,疏水性较高。
 | 图 1 HSP20全长cDNA序列及其ORF编码的氨基酸序列 |
ExPASy中TargetP预测HSP20无信号序列,未发现线粒体、过氧化酶体、溶酶体和细胞核等亚细胞定位序列。 2.3 InterPro Scan分析HSP20蛋白质功能结构域(图 2)
结果显示,该蛋白含有HSP20结构域,证实该蛋白属于小热休克蛋白20基因家族编码产物;无信号肽,与亚细胞定位分析相符。
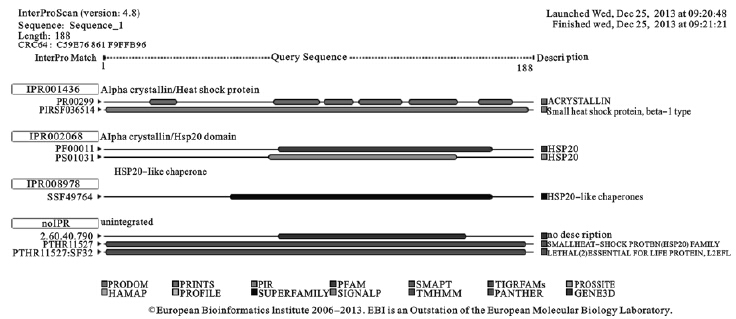 | 图 2 InterPro Scan分析HSP20蛋白质功能结构域 |
Sec预测HSP20蛋白α螺旋(H)和无规卷曲(L)的比例为4.26:67.55,β折叠(E)与无规卷曲(L)的比例为28.19:67.55,二级结构以β折叠(E)为主。 2.5 PEASY-E1-HSP20质粒构建及鉴定(图 3)
特异性引物扩增目的基因,2%琼脂糖凝胶电泳后切胶回收目的基因,将目的基因与质粒载体按一定比例连接后,转化入感受态细胞,氨苄青霉素筛选阳性克隆子。将重组质粒进行PCR和双酶切后,2%琼脂糖凝胶电泳鉴定。重组质粒双酶切后在600~500 bp有一清晰的条带,与目的基因(567 bp)的大小基本相符,测序结果证实重组质粒中插入序列与目的序列一致,表明PEASY-E1-HSP20质粒构建成功。
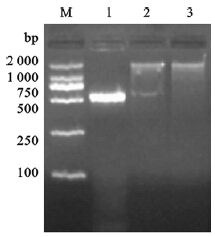 | 注:M:Marker(2 000 bp);1:PCR产物;2:双酶切鉴定结果;3:重组质粒PEASY-E1-HSP20。 图 1 重组质粒PCR及双酶切鉴定图 |
将构建好的重组质粒PEASY-E1-HSP20转化到 E.coli OrigmiB/DE3 中经IPTG诱导表达,15% SDS-PAGE分析结果如图 4第 5、6泳道所示,在 20 kDa左右处出现表达条带,与目的蛋白分子量基本相符。将蛋白进行纯化,结果见图 4第7泳道所示,证明目的蛋白纯化成功。用Bradford 法测的该蛋白浓度为0.32 mg/mL。
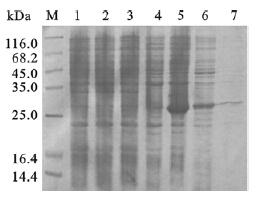 | 注:M:蛋白Marker;1:PEASY-E1未加IPTG诱导;2:PEASY-E1加IPTG诱导;3:PEASY-E1-HSP20未经IPTG诱导的OrigmiB/DE3全菌液;4:PEASY-E1-HSP20加IPTG诱导的OrigmiB/DE3全菌液;5:PEASY-E1-HSP20加IPTG诱导后的沉淀;6:PEASY-E1-HSP20加IPTG诱导后的的上清;7:PEASY-E1-HSP20加IPTG诱导表达后纯化蛋白。 图 4 15%SDS-PAGE分析PEASY-E1-HSP20 在大肠杆菌OrigmiB/DE3中表达纯化效果 |
家蝇孳生于杂乱菌丛的环境中,传播疾病,是重要的媒介传播昆虫,其免疫防御、免疫协助得到很多研究者的关注[10]。sHSP是HSP家族中的一个成员,因其分子量在HSP家族中最小而得名。目前对HSP研究报道较多,但是对家蝇sHSP研究报道较少,sHSP作为分子伴侣在生物体的生命活动中发挥了重要作用。生物体在生命活动的不同时期,sHSP均起到一定的生物学功能,能够协助生物体内变性蛋白质的结构进行重新折叠[11, 12],可以诱导生物体产生耐热性、稳定性细胞骨架等[13],在生物体的生长、发育、进化过程中发挥了重要作用。
本研究根据NCBI上GenBank中家蝇sHSP中HSP20基因设计特异性引物,以家蝇3日龄幼虫提取总RNA后逆转录cDNA为模板,成功扩增出目的基因,测序结果证实与GenBank(登录号:XM_005190903)序列相符,通过生物信息学分析显示该基因包含一个完整的ORF为567 bp,编码188个氨基酸,理论分子量为21 443.2 Da,其等电点为 5.96。重组质粒在大肠杆菌OrigmiB/DE3中经IPTG诱导表达,并成功纯化目的蛋白,15%SDS-PAGE分析显示纯化蛋白与目的蛋白分子量大小相符。
| [1] | Huang LH, Wang HS, Kang L.Different evolutionary lineages of large and small heat shock proteins in eukaryotes[J].Cell Res, 2008, 10:1074-1076. |
| [2] | Rani N,Bharti S,Manchanda M,et al.Regulation of heat shock proteins 27 and 70,p-Akt/p-eNOS and MAPKs by Naringin Dampens myocardial injury and dysfunction in vivo after ischemia/reperfusion[J].PLoS One,2013,8(12):e82577. |
| [3] | Gusev NB,Bukach OV,Marston SB.Structure, properties, and probable physiological role of a small heat shock protein with molecular mass 20 kDa(Hsp20, HspB6)[J].Biochemistry(Moscow), 2005,70(6):762-772. |
| [4] | Carra S,Sivilotti M,Zobel ATC,et al.HspB8,a small heat shock protein mutated in human neuromuscular disorders,has in vivo chaperone activity in cultured cells [J].Human Molecular Genetics,2005,14:1659-1669. |
| [5] | Huang LH,Wang CZ,Kang L.Cloning and expression of five heat shock protein genes in relation to cold hardening and development in the leafminer, Liriomyza sativa[J].Journal of Insect Physiology, 2009(55):279-285. |
| [6] | Ahmad A,Nagaraja TG,Zurek L.Transmission of Escherichia coli O157:H7 to cattle by house flies[J].Prev Vet Med,2007,80(1):74-81. |
| [7] | Boulesteix G,Le Dantec P,Chevalier B,et al.Role of Musca domestica in the transmission of multiresistant bacteriain the centers of intensive care setting in sub-Saharan Africa [J].Ann FrAnesth Reanim,2005,24:361-365. |
| [8] | 国果, 吴建伟, 付萍, 等.家蝇幼虫分泌型抗菌肽对大肠埃希菌抑菌作用[J].中国公共卫生,2012, 28(10):1318-1321. |
| [9] | 刘晖, 王鑫, 蔡辉霞, 等.抗菌肽attacin 重组杆状病毒表达载体的构建[J].中国公共卫生, 2013, 16(11):1871-1872. |
| [10] | 魏洪, 吴建伟, 国果, 等.家蝇幼虫血淋巴提取物抗肿瘤作用[J].中国公共卫生, 2013,29(2):217-219. |
| [11] | Li ZW, Li X, Yu QY, et al. The small heat shock protein(sHSP) genes in the silkworm, Bombyx mori, and comparative analysis with other insect sHSP genes[J]. BMC Evolutionary Biology,2009, 9:215. |
| [12] | Haslbeck M.Recombinant expression and in vitro refolding of the yeast small heat shock protein Hsp4[J].International Journal of Biological Macromolecules,2006,38(2):107-114. |
| [13] | Yang LL,Lü ZY,Hu SM,et al.Schistosoma japonicum proteomics analysis of differentially expressed proteins from ultraviolet-attenuated cercariae compared to normal cercariae[J].Parasitol Res,2009,105(1):237-248. |
 2015, Vol. 31
2015, Vol. 31


