2. 军事医学科学院放射与辐射医学研究所
贫铀(depleted uranium,DU)即天然铀加工浓缩后,U235含量低于0.714%的副产品,其中U238占99.75%以上。在海湾战争中北约军队大规模地使用了贫铀弹,其在穿甲过程中形成高浓度颗粒,吸入颗粒后大部分沉积在肺部或转入机体其他系统引起损伤,长期滞留放射毒性和化学毒性可能导致肺部肿瘤形成[1],引发对贫铀的一系列研究[2,3,4]。研究表明,铀矿尘在诱导大鼠肺组织纤维化过程中铀矿尘浓度与肺组织纤维化程度具有一致性[5]。本研究拟通过观察巨噬细胞吞噬贫铀颗粒后产生的活性氧、一氧化氮及谷胱甘肽变化,及巨噬细胞吞噬贫铀颗粒后上清中可溶性铀含量变化,为从细胞水平上寻找贫铀促排措施提供依据。结果报告如下。
1 材料与方法 1.1 主要试剂1640培养液(美国Thermo公司)、胎牛血清(美国Gibco公司)、2-(2-甲氧基-4-硝基苯基)-3-(4-硝基苯基)-5-(2,4-二磺酸苯)-2H-四唑单钠盐(CCK-8)试剂、谷胱甘肽检测试剂盒(日本同仁公司)、一氧化氮检测试剂盒(中国碧云天公司)、二氯荧光黄双乙酸盐新型荧光探针(美国Sigma公司),将贫铀颗粒(军事医学科学院,取自贫铀弹头的充分燃烧氧化物,经机器研磨,颗粒90%<2 μm)高压灭菌备用,临用前用1640培养液制备成悬浮液。
1.2 细胞培养与处理体外培养的永生化人单核白血病细胞系THP-1(中国医学科学院基础研究所细胞中心)以含有100 U/mL青霉素、100 μg/mL链霉素及10%新生牛血清的1 640培养液于37 ℃、5%CO2孵箱中培养,每隔4~5 d传代1次,取状态好的细胞冻存于液氮中复苏备用。此细胞可受佛波酯诱导向单核系方向分化;本研究采用100 nmol/L的佛波酯将体外培养的THP-1细胞诱导24 h分化为巨噬细胞后进行实验。实验设对照组、贫铀染毒组,每组设3个平行样。
1.3 指标与方法 1.3.1 细胞存活率实验采用CCK-8法,取贴壁生长的巨噬细胞,进行贫铀细胞染毒(0、25、75、100、200、300、400、500 μg/cm2),急性染毒20 h后,加入CCK-8 试剂(100 μL/孔),孵育4 h 后于450 nm处采用酶标仪读取吸光度(A)值。
1.3.2 细胞内活性氧检测将巨噬细胞接种于96孔板中,加二氯荧光黄双乙酸盐新型荧光探针(10 μmol/L)孵育(37 ℃,30 min),贫铀染毒(浓度0、20、40、60、80、100 μg/cm2)作用2 h,D-Hanks洗涤1 次,用化学/荧光发光仪检测各孔的荧光强度,细胞内活性氧水平以平均荧光强度表示。
1.3.3 细胞内一氧化氮、谷胱甘肽含量检测将巨噬细胞接种于6孔板(5×105个/mL),分别进行贫铀染毒(浓度0、20、40、60、80、100 μg/cm2)作用24 h,染毒结束后,D-Hanks 洗涤细胞2~3次,用100 μL细胞裂解液将细胞裂解,高速离心(8 000 r/min,4 ℃,10 min)后收集上清,按试剂盒说明书测定细胞内一氧化氮及谷胱甘肽含量。
1.3.4 巨噬细胞超微结构观察将巨噬细胞接种于6孔板(5×105个/mL),贫铀染毒(浓度0、20、40 μg/cm2)分别作用0.5、1、2 h,染毒结束后弃上清,D-Hanks 洗涤细胞2~3次,用软橡皮将细胞轻轻擦下,离心收集细胞(1 500 r/min,4 ℃,5 min),固定,电镜下拍照观察。
1.3.5 巨噬细胞上清中可溶性铀检测将巨噬细胞接种于6孔板(5×105个/mL),贫铀染毒(浓度0、20、40、60、80、100 μg/cm2)分别作用1、4、24 h,染毒结束后,用0.22 μm过滤收集上清,高速离心(8 000 r/min,4 ℃,10 min)后用湿消化法测定可溶性铀含量。
1.4 统计分析实验数据采用±s表示,采用SPSS 16.0 软件进行统计分析,组间差异比较采用单因素方差分析和t检验,P<0.05 为差异有统计学意义。
2 结 果 2.1 贫铀对巨噬细胞存活率影响对照组、贫铀颗粒25、75、100、200、300、400、500 μg/cm2组巨噬细胞存活率分别为100%、82.58%、52.91%、29.2%、25.05%、22.79%、13.71%、4.71%,随着贫铀作用剂量增加,巨噬细胞存活率明显降低。
2.2 贫铀对巨噬细胞内活性氧、一氧化氮及谷胱甘肽影响(表 1)与对照组比较,贫铀各剂量组巨噬细胞产生的活性氧、一氧化氮含量明显升高,谷胱甘肽含量明显下降。
| 表 1 贫铀对巨噬细胞活性氧、一氧化氮及谷胱甘肽 含量影响(x±s,n=3) |
分别以贫铀0、20、40 μg/cm2处理巨噬细胞0.5、1、2 h后,20 μg/cm2处理1 h时,可见贫铀颗粒被吞入细胞后与溶酶体形成吞噬溶酶体(图 1c),而40 μg/cm2贫铀颗粒组巨噬细胞为空泡化,且胞膜消失(图 1d)。
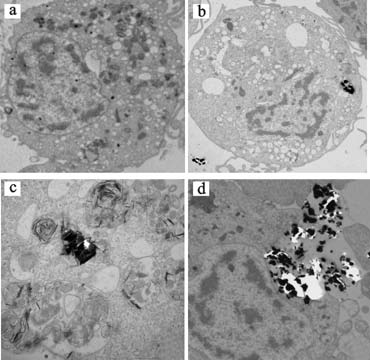 | 注:a:对照组,×8000;b:20 μg/cm2 0.5 h组,×8000;c:20 μg/cm2 1 h组,×15000;d:40 μg/cm2 2 h组,×10000。 图 1 DU颗粒染毒巨噬细胞透射电镜观察 |
巨噬细胞经贫铀颗粒作用1、4、24 h上清中可溶性铀的含量逐渐增加,且随着贫铀颗粒剂量增加,巨噬细胞上清中可溶性铀含量上升。
| 表 2 贫铀对巨噬细胞上清中可溶性铀含量影响(μmol/mL,x±s,n=3) |
研究表明,肺泡巨噬细胞在清除颗粒过程中有着非常重要的作用[6]。虽然颗粒物所致肺组织结构与功能改变其细胞学机制尚未完全阐明,但不同大小的颗粒物进入肺组织后沉积在呼吸道的不同部位,使这些不同部位的细胞产生如活性氧及细胞因子等活性物质[7]。在呼吸道的不同部位,存在着不同类型的细胞,如在支气管及细支气管表面上皮细胞以及肺泡Ⅰ型和Ⅱ型上皮细胞;在远端呼吸道上皮表面有可以游走的且具有较强吞噬功能的肺泡巨噬细胞。这些细胞既不仅作为呼吸道对吸入颗粒的第一道防线,通过颗粒物刺激也可产生和分泌生物活性物质。本研究结果表明,贫铀颗粒通过刺激巨噬细胞产生活性氧、一氧化氮致细胞损伤。
体外研究表明,大鼠吸入贫铀粉尘后难溶性化合物铀主要滞留在肺和支气管淋巴结中被巨噬细胞吞噬[8]。在进入细胞时首先在溶酶体中被各种溶酶体溶解。贫铀颗粒被巨噬细胞吞噬后,会与溶酶体结合继而形成吞噬溶酶体,在溶酶体各种酶作用下被吞噬消化成可溶性铀,当溶酶体中的酶不能满足消化贫铀颗粒时,溶酶体首先破裂将溶酶体酶释放,继而细胞膜也被破坏,将未消化的颗粒释放至外环境中,以此反复吞噬贫铀颗粒。本研究结果显示,电镜下观察到贫铀颗粒并不像其他颗粒那样一点一点的进入细胞,而是呈空泡状大量聚集在细胞中。由于巨噬细胞可吞噬消化贫铀颗粒,表明巨噬细胞在铀的促排过程中起着非常关键作用。提示可通过提高巨噬细胞的吞噬能力或提高巨噬细胞中相关溶酶体酶活性从而促进铀的溶解及排出。
| [1] | Bleise A,Danesi PR,Burkart W.Properties,use and health effect of depleted uranium(DU):a general overview[J].J Environ Radioact,2003,64:93-112. |
| [2] | Briner W,Murray J.Effects of short-term and long-term depleted uranium exposure on open-field behavior and brain lipid oxidation in rats[J].Neurotoxicology and Teratology,2005,27(1):135-144. |
| [3] | Craft ES,Abu-Qare AW,Flaherty MM,et al.Depleted and natural uranium:chemistry and toxicological effects[J].Journal of Toxicology and Environmental Health,Part B,2004,7(4):297-317. |
| [4] | World Health Organization.Depleted uranium:sources,exposure and health effects[M].Geneva:World Health Organization,2001. |
| [5] | 王守凤,胡迎春,袁新健,等.铀矿尘致肺纤维化对PⅢNP、LN 和 TGF-β1影响[J].中国公共卫生,2012,28(6):802-804. |
| [6] | Misson P,van den Brule S,Barbarin V,et al.Markers of macrophage differentiation in experimental silicosis[J]. J Leuk Biol,2004,76:926-932. |
| [7] | Kim KA,Lim Y,Kim EK,et al.Potential biorrmrker of coal workers′ pneumoconiosis[J].Toxicol Left,1999,108:297-302. |
| [8] | 李蓉,艾国平,徐辉,等.吸入贫铀粉尘和/或嵌入贫铀片大鼠体内铀的分布[J].第四军医大学学报,2004,25(6):503-506. |
 2014, Vol. 30
2014, Vol. 30


