2. 吉林医药学院附属医院泌尿外科
白细胞分化抗原147(cluster of differentiation 147,CD147)亦称细胞外基质金属蛋白酶诱导因子(extracellular matrix metalloproteinase inducer,EMMPRIN),是分子量为50~60 kD单次跨膜糖蛋白,属于免疫球蛋白超家族成员。CD147在前列腺癌(prostate cancer,PCa)的组织和细胞中均高表达[1, 2],其表达水平与肿瘤的侵袭和转移[2]、血管生成[3]和能量代谢[4]等密切相关。前期研究利用雄激素依赖性前列腺癌(androgen-dependent prostate cancer,ADPC)细胞系LNCaP,在体外应用激素递减法建立雄激素非依赖性前列腺癌(androgen-independent prostate cancer,AIPC)细胞模型LNCaP-AI[5],成为研究AIPC的发生及其分子机制理想的肿瘤细胞模型。本研究应用RNAi沉默CD147基因表达,观察对体外培养的LNCaP-AI细胞增殖、细胞周期以及细胞凋亡的影响。结果报告如下。 1 材料与方法 1.1 材料
活性炭/葡聚糖处理的胎牛血清(DCC-FBS)(美国Hyclone公司);无酚红1640(美国Sigma公司);LipofectamineTM2000和G418(美国Invitrogen公司);总RNA/mRNA提取试剂盒和reverse transcription(RT)-PCR试剂盒(北京鼎国公司);兔抗CD147和β-actin抗体(美国GeneTex公司)。pSilencer-Scramble和pSilencer-CD147干扰载体(吉林医药学院检验学院实验室)。LNCaP-AI细胞系由吉林医药学院检验学院实验室利用LNCaP细胞系通过雄激素递减法建立[5]。细胞培养在10%DCC-FBS的去酚红1640中。置于37 ℃恒温培养箱中培养,取指数生长期细胞进行实验。 1.2 指标与方法 1.2.1 干扰CD147表达的稳定细胞系建立
根据Lipofectanmine 2000操作手册将pSilencer-Scramble载体(阴性对照)和pSilencer-CD147干扰载体(CD147沉默)分别转染到LNCaP-AI细胞中,挑取在G418压力筛选下存活的克隆,消化并转移细胞继续培养,将细胞分别命名为AI/Scramble(阴性对照组)和AI/shCD147(CD147沉默组)。 1.2.2 CD147基因表达检测
采用RT-PCR法,用总RNA/mRNA提取试剂盒提取总RNA,取细胞总RNA 1 μg,以Oligo(dT)为引物反转录为cDNA,采用RT-PCR方法检测CD147在mRNA水平上的表达,以β-actin作为内参。CD147引物上游:5′-aaggtggactccgacgaccagtgg-3′,下游:5′-cttccggcgcttctcgtagatgaag-3′;β-actin引物上游:5′-atcatgtttgagaccttcaaca-3,下游:5′-catctcttgctcgaagtcca-3,实验采用}反应体系。反应条件94 ℃ 5 min,94 ℃ 30 s,55 ℃ 30 s,72 ℃ 15 s 进行30 个循环扩增反应后72 ℃ 10 min延伸。对扩增基因在1.2%胶浓度并含溴化乙锭的琼脂糖上进行电泳。 1.2.3 CD147蛋白水平表达检测
采用Western blot法,取40 g 蛋白行十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE),将凝胶上蛋白移至醋酸纤维素膜,于50 g/L 脱脂奶粉中4℃封闭过夜,加兔抗CD147抗体(1∶1 000),小鼠抗β-actin抗体(1∶3 000),4 ℃过夜。磷酸缓冲盐溶液吐温(phosphate buffered saline tween,PBST)洗膜,分别加辣根过氧化物酶标记的山羊抗兔抗体(1∶3 000)室温避光孵育2 h。TBST洗膜后,加底物电化学发光显影。使用Quantity One软件扫描并做灰度分析。 1.2.4 细胞增殖检测
取对数生长期细胞,以台盼蓝检测活力大于95%细胞,以1 500个/孔密度接种于96孔细胞培养板,每孔体积200 μL,分组培养2、4、6、8和10 d,各时间点均设3个复孔。培养结束后加入5 mg/mL噻唑蓝20 μL/孔,37 ℃,5%CO2继续孵育4 h,小心吸弃上清,加入二甲基亚砜150 μL/孔,充分混匀,于Bio-Tek 酶标仪490 nm 处测定吸光度(A)值。 1.2.5 细胞周期检测
0.25%胰蛋白酶消化收集细胞,冰冷磷酸缓冲盐溶液(phosphate buffered saline,PBS)清洗2 次,预冷的70%乙醇固定,4 ℃过夜,上机前离心除去乙醇,PBS清洗3 次,100 mg/L RNase A 37 ℃消化40 min;加入1 mL 100 μg/mL碘化丙啶溶液,4 ℃避光染色30 min,流式细胞仪检测细胞DNA含量。 1.2.6 细胞凋亡检测
将细胞消化后接种于6 孔板,培养24 h。细胞经胰酶消化后,取100 μL置于5 mL流式管中,加入5 μL Annexin V-FITC和10 μL 100 μg/mL碘化丙啶溶液,混匀后室温避光孵育20 min,然后加入400 μL PBS缓冲液,流式细胞仪进行凋亡检测。 1.3 统计分析
计量数据以x±s表示,应用SPSS 13.0软件进行统计分析,组间差异比较采用t检验,P<0.05为差异有统计学意义。 2 结 果 2.1 RNAi对CD147表达影响(图 1、2)
通过RT-PCR(图 1)和Western blot(图 2)鉴定CD147在细胞中基因和蛋白水平的表达变化。与AI/Scramble组CD147 mRNA(0.79±0.08)和蛋白表达(0.85±0.11)比较,AI/shCD147组CD147 mRNA(0.39±0.06)和蛋白表达(0.31±0.05)均明显降低,差异有统计学意义(P<0.05)。
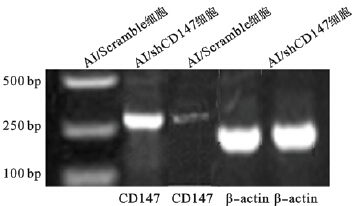 | 图 1 RT-PCR鉴定转染RNAi载体后CD147 mRNA表达 |
 | 图 2 Western blot鉴定转染RNAi载体后CD147蛋白表达 |
与阴性对照比较,CD147干扰组细胞培养至第6 d 时,细胞生长速度减慢,至第8、10 d 细胞生长明显受到抑制(P<0.05)。
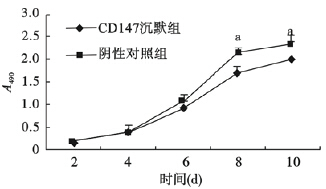 | 注:与对照组比较,a P<0.05。 图 3 CD147沉默对LNCaP-AI细胞生长影响 |
与对照组比较,CD147沉默组细胞周期出现G0/G1期细胞百分率增加;S期和G2/M期细胞百分率减少,表现为G0/G1期阻滞。
| 表 1 CD147沉默对LNCaP-AI细胞周期影响(%,x±s,n=3) |
流式细胞仪检测结果表明,与对照组比较,CD147沉默组LNCaP-AI细胞凋亡无明显变化。
| 表 2 CD147沉默对LNCaP-AI细胞凋亡影响(%,x±s,n=3) |
在美国,PCa占男性恶性肿瘤发病率的第1位,肿瘤致死率的第2位[6]。随着社会老龄化和生活方式的改变,中国PCa发病率逐年增高[7]。早期患者适合前列腺癌根治术,雄激素阻断疗法(androgen deprivation therapy,ADT)有效。然而,绝大多数患者最终由ADPC转化为AIPC,ADT治疗无效,继而引起肿瘤复发和转移[8]。AIPC是PCa病程中的致死性阶段,尚无有效的治疗手段[8]。因此,明确AIPC机制并探索有效的治疗手段具有重要意义。LNCaP细胞系保留人的PCa特征,其生长具有很强的雄激素依赖性,表达前列腺特异抗原(prostate specific antigen,PSA)和雄激素受体,可在雄性裸鼠上成瘤。在此基础上,经过体外实验诱导产生的LNCaP-AI细胞亚系,能够在活性碳处理的血清或去势宿主的环境下生长,同时伴PSA持续升高。该模型可以模拟临床上内分泌治疗过程中PCa由激素依赖发展为激素非依赖的过程,为AIPC机制和治疗研究提供了理想平台[5, 9]。
CD147在PCa中表达增高,参与肿瘤细胞转移和侵袭等生物学行为[1, 2]。本研究利用RNAi技术,将靶向CD147基因的干扰载体转染LNCaP-AI细胞,通过G418筛选后获得稳定低表达CD147的细胞模型,结果显示,CD147沉默后细胞增殖明显受到抑制。细胞在增殖、分化和凋亡方面的异常均与肿瘤的发生和发展有关,其中细胞周期紊乱和抗凋亡的发生是肿瘤发生的机制之一。细胞周期过程为G1-S-G2-M期,G1期为DNA合成前期,标志细胞进入增殖态,增殖旺盛的细胞G1期持续时间短。S期为DNA合成和复制期。G2、M期分别为DNA合成后期及有丝分裂期。细胞周期G1→S、G2→M异常将使细胞周期发生紊乱、细胞增殖失控,最终发生癌变。本研究结果表明,CD147沉默后LNCaP-AI细胞中G1期比例增多、S期比例减少,但细胞凋亡无明显变化。提示CD147通过改变G0/G1和G1/S期细胞转换而影响LNCaP-AI细胞生长和增殖。
| [1] | Zhong WD,Liang YX,Lin SX,et al.Expression of CD147 is associated with prostate cancer progression[J].Int J Cancer,2012,130(2):300-308. |
| [2] | Wang LG,Wu GJ,Yu L,et al.Inhibition of CD147 expression reduces tumor cell invasion in human prostate cancer cell line via RNA interference[J].Cancer Biol Ther,2006,5(6):608-614. |
| [3] | Chen Y,Zhang H,Gou X,et al.Upregulation of HAb18G/CD147 in activated human umbilical vein endothelial cells enhances the angiogenesis[J].Cancer Lett,2009,278(1):113-121. |
| [4] | Le Floch R,Chiche J,Marchiq I,et al.CD147 subunit of lactate/H+ symorters MCT1 and hypoxia-inducible MCT4 is critical of energetic and growth of glycolytic tumors[J].Proc Natl Acad Sci USA,2011,108(40):16663-16668. |
| [5] | 孔德玉,杨冬梅,陈艳媛,等.雄激素非依赖性前列腺癌LNCaP-AI细胞亚系模型的建立[J].吉林医药学院学报,2012,33(6):361-363. |
| [6] | Siegel R,Naishadham D,Jemal A.Cancer statistics,2012[J].CA Cancer J Clin,2012,62(1):10-29. |
| [7] | 杨国平,吴益民,杨洪军,等.前列腺癌标志物与年龄及膳食结构关系[J].中国公共卫生,2008,24(5):551-552. |
| [8] | Scher HI,Fizazi K,Saad F,et al.Increased survival with enzalutamide in prostate cancer after chemotherapy[J].N Engl J Med,2012,367(13):1187-1197. |
| [9] | Shi XB,Ma AH,Tepper CG,et al.Molecular alterations associated with LNCaP cell progression to androgen independence[J].Prostate,2004,60(3):257-271. |
 2014, Vol. 30
2014, Vol. 30


