纳米材料由于具有许多独特性能(如巨大的表面效应、量子效应等),因而在生物医药、环境保护等领域有着极广阔的应用前景[1]。但有研究结果显示,部分人造纳米材料具有毒性,可以引起氧化应激、炎症反应及其他组织器官的损害[2, 3]。目前有越来越多的学者开始关注纳米材料对中枢神经系统的损伤。在正常情况下,只有亲脂性物质易于通过血脑屏障,但是纳米颗粒由于其特殊理化特性,有可能通过不同的途径通过血脑屏障[4, 5],进入脑实质组织中。鉴于目前对纳米铝神经毒性的研究还处于初步阶段,本研究主要通过原代培养星形胶质细胞和脑微血管内皮细胞来建立血脑屏障模型,以探讨纳米氧化铝对血脑屏障通透性的影响。 1 材料与方法 1.1 实验动物
新生1~3dWistar大鼠,雌性,10只,清洁级,由山西医科大学实验动物中心提供〔许可证号:SCXK(晋)2009-0001〕。 1.2 主要试剂与仪器
纳米氧化铝(美国 Sigma公司);达尔伯克改良伊格尔(Dulbecco′s modified eagle medium,DMEM)培养基(美国Gibico公司);胰酶(北京邦定生物医学公司);多聚赖氨酸(Poly-L-Lysine,MW 30000-70000)(美国 Sigma公司);胎牛血清(杭州四季青生物工程材料公司);马血清(中国新锐生物工程有限公司);EC专用培养基(北京赛诺科为生物科技有限公司);羊抗兔[基因科技(上海)有限公司];Ⅷ因子(太原博士德生物工程有限公司);Transwell版(3470),(北京德润丰科技有限责任公司)。二氧化碳培养箱(德国 Heraeus 公司);SW-CJ-2F型超净工作台(苏州安泰空气技术有限公司);80-2B型离心沉淀机(盐城市科学仪器厂);LS-B50L立式压力蒸汽灭菌器(江阴滨江医疗设备厂);AB104-N电子天平(上海电子仪器厂);透射电镜(日本电子公司);Nicomp-380/ZLS动电电位粒径测定仪(美国 PSS公司)。 1.3 纳米氧化铝粒径及电位测定
将纳米铝按照染毒浓度制成不同浓度的悬液,经超声30 min混匀后制成纳米颗粒物染毒悬液。采用Nicomp-380/ZLS动电电位粒径测定仪测定纳米氧化铝颗粒悬液的zeta电位。 1.4 透射电镜观察纳米氧化铝形态及尺寸
称取102 mg 50 nm纳米氧化铝粉末加入10 mL的 DMEM培养液配成0.1 mol/L 纳米氧化铝储备液。临用前,将纳米氧化铝储备液超声混匀10 min 成为均匀的悬浊液,吸取10 mL滴至有碳膜覆盖的电镜铜网上,用吸水纸吸去铜网上多余的DMEM培养液,室温放置待铜网完全干燥后,采用电镜进行观察。 1.5 脑微血管内皮细胞及星形胶质细胞培养
在无菌室内,取大鼠脑皮质制成匀浆,0.1%Ⅱ型胶原酶消化,全细胞培养液终止消化。1 000 r/min离心10 min。弃上清,加入15%葡聚糖吹打成单细胞悬液,4 ℃ 4 000 r/min离心20 min。参照文献[6]进行脑微血管内皮细胞及星形胶质细胞培养。 1.6 血脑屏障模型染毒及通透性测定
血脑屏障体外模型建成后,参考文献[6]有效性鉴定后,以500 μmmoL纳米氧化铝对血脑屏障模型进行染毒,分别在2、4、6、8 h去除染毒,在供体池中加入400 μL浓度为0.02 mg/mL的芦丁,受体池中加入无血清DMEM培养液,加入后2 h从受体池中取400 μL,以无血清DMEM培养液调零,用分光光度计测定吸光值。以不同浓度50 nm纳米氧化铝对血脑屏障进行染毒,分别为溶剂对照组(无血清DMEM)及低(125 μmmoL)、中(250 μmmoL)、高纳米氧化铝染毒组(500 μmmoL),8 h后在供体池中加入400 μL浓度为0.02 mg/mL的芦丁,受体池中加入无血清DMEM培养液,加入后2 h从受体池中取400 μL,以无血清DMEM培养液调零,用分光光度计测定吸光值。 1.7 统计分析
采用SPSS 13.0软件对各项指标的实验数据进行处理,正态结果用(x±s)表示,采用方差分析和LSD-t检验进行组间比较。 2 结 果 2.1 纳米氧化铝颗粒表征
对不同浓度的氧化铝纳米颗粒进行了透射电镜和扫描电镜观察,纳米氧化铝颗粒呈规则圆形,粒径分布均匀。Nicomp-380/ZLS动电电位粒径测定仪测定纳米氧化铝颗粒悬液平均粒径为149.2 nm,电位为47.6 mV。 2.2 血脑屏障有效性鉴定
(1)4 h渗漏实验:在显微镜下观察脑微血管内皮细胞(brain microvascular endothelial cells,BMEC)培养至汇合后,将细胞插入器的液面加高,4 h后,80%的细胞插入器能够维持0.5 cm的液面差,可以将其作为血脑屏障(blood-brain barrier,BBB)体外模型研究药物的通透性。(2)芦丁的通透性曲线(图 1):0.02 mg/mL芦丁溶液的最大吸收波长位于360 nm处,吸光度值为0.503,且与DMEM培养液的吸收峰不重合,将受体池内DMEM的吸光度值调零,每组的3个共培养模型测得的吸光度取平均值,获得受体池芦丁溶液的吸光度与时间曲线。
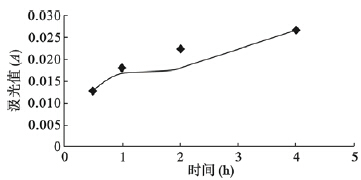 | 图 1 受体池芦丁吸光度与时间变化曲线 |
(1)不同染毒时间血脑屏障通透性变化情况:纳米氧化铝染毒0、2、4、6、8 h 芦丁吸光值分别为(0.441± 0.001)、(0.458±0.008)、(0.534±0.009)、(1.047±0.002)、(1.976±0.012),与纳米氧化铝染毒0h组比较,2、4、6、8 h纳米氧化铝染毒组芦丁吸光值均增加,差异有统计学意义(P<0.05)。(2)不同染毒浓度血脑屏障通透性变化情况:溶剂对照组及125、250、500 μmmoL纳米氧化铝染毒组芦丁吸光值分别为(0.92±0.11)及(1.05±0.04)、(1.44±0.07)、(1.58±0.25),与溶剂对照组比较,250、500 μmmoL染毒组芦丁吸光值均增加,差异有统计学意义(P<0.05)。 3 讨 论
有报道表明,纳米材料可以抑制血管内皮细胞的活性,通过活性氧途径诱导细胞凋亡,产生细胞毒性[7]。蔡文君等[8]发现纳米硫硒化镉能通过血脑屏障,导致小鼠脑细胞和肝细胞DNA损伤。
本实验采取脑微血管内皮细胞和星形胶质细胞共同培养建立体外血脑屏障模型,该方法较为简单实用,且能够较为真实地反映BBB的结构功能特点,自建立以来就一直成为血脑体外研究的首选[9]。模型建立后,采用纳米氧化铝进行染毒,检测芦丁透过供池进入受池的吸光度,来评价血脑屏障通透性的改变。结果显示,与0 h染毒组相比,染毒2、4、6、8 h组芦丁吸光值均增加;与溶剂对照组相比,250、500 μmmoL组芦丁吸光值均增加,均提示血脑屏障通透性发生改变。综上所述,纳米氧化铝可以改变血脑屏障通透性,且随着浓度和时间的增加,其作用更明显。但纳米氧化铝对血脑屏障通透性改变的机制尚不清楚,有待进一步研究。
| [1] | Ju-Nam Y, Lead JR.Manufactured nanoparticles an overview of their chemistry, interactions and potential environmental implications[J].Sci Total Environ, 2008, 400(1-3):396-414. |
| [2] | 张一平.纳米材料安全性与纳米二氧化硅毒性研究进展[J].浙江教育学院学报, 2009, 7(4):85-90. |
| [3] | 李倩, 唐萌, 马明, 等.纳米氧化铁对细胞膜流动性影响及其遗传毒性[J].中国公共卫生, 2006, 22(10):1277-1278. |
| [4] | Zhu MT, Feng WY, Wang Y, et al.Particokinetics and extrapulmonary translocation of intratracheally in stilldeferricoxide nanoparicles in rats and the potential health risk assessment[J].Toxicol Sci, 2009, 107(2):342-351. |
| [5] | Kwon JT, Hwang SK, Jin H, et al.Body distribution of inhaled fluorescent magnetic nanoparticles in the mice[J].J Ocuup Health, 2008, 50(1):1-6. |
| [6] | Shayan G, Choi YS, Shusta EV, et al.Murine in vitro model of the blood-brain barrier for evaluating drug transport[J].European Journal of Pharmaceutical Sciences, 2011, 42(1-2):148-155. |
| [7] | 韩燕, 崔国权, 董淑英, 等.纳米氧化锌诱导血管内皮细胞凋亡及氧化应激[J].中国公共卫生, 2012, 28(4):500-502. |
| [8] | 蔡文君, 田熙科, 李岩, 等.纳米硫酸化镉对小鼠脑和肝DNA的损伤[J].公共卫生与预防医学, 2008, 19(1):12-15. |
| [9] | 李珺, 彭亮, 黄胜和, 等.体外血脑屏障模型的建立及发展[J].广东医学, 2009, 30(4):647-648. |
 2014, Vol. 30
2014, Vol. 30


