2. 中国医科大学免疫学教研室
近年来,乳腺癌已成为严重威胁中国妇女健康的疾病之一,乳腺癌发病率位居大城市女性肿瘤的第一位,而且发病呈年轻化趋势发展[1]。早发现、早诊断、早治疗会显著提高患者生存机会和生存质量[2]。L-精氨酸(L-arginine,L-Arg)作为成人的一种条件必需氨基酸,在某些生理或病理条件下,必须通过食物补充以满足机体的需要[3]。L-Arg可被精氨酸酶1或诱导型一氧化氮合酶分别代谢为尿素和L-鸟氨酸或一氧化氮(nitric oxide,NO)和L-瓜氨酸[4]。据报道,人类乳腺癌细胞系可表达精氨酸酶,乳腺癌的发生与精氨酸的耗竭及机体的免疫抑制状态有关[5],因此,本研究于2012年8月通过乳腺癌4T1荷瘤小鼠模型,采用流式细胞术、ELISA和Griess反应检测T细胞及巨噬细胞的数量及功能,探讨L-Arg对乳腺癌的治疗效果及相关免疫机制,为开发预防或辅助治疗乳腺癌的新药提供实验依据。 1 材料与方法 1.1 材料
6~8周龄的SPF级雌性BALB/c小鼠购自中科院上海实验动物中心。实验动物合格证号:2007000542390。 1.2 主要试剂
4T1小鼠乳腺癌细胞株(中国科学院上海细胞库)。L-Arg(美国Sigma公司);抗-CD3e-FITC(145-2C11)、抗-CD4-PE(H129.19)、抗-CD8α-PerCP(53-6.7)(美国BD Biosciences公司);抗-F4/80-PerCP cy5.5(BM8)(美国Ebiosciences公司);TNF-α和IFN-γ ELISA试剂盒(美国R&D公司)。 1.3 方法 1.3.1 实验分组及小鼠荷瘤模型制备
小鼠随机分为实验组(L-Arg组)和对照组(PBS组),每组10只。4T1小鼠乳腺癌细胞(1×105)皮下注射至小鼠右侧,制备小鼠荷瘤模型。从可以触摸到肿瘤开始,实验组小鼠连续20 d给予灌胃L-Arg(1.5 g/kg),对照组给予等量的PBS。动态监测肿瘤生长:用卡尺测量肿瘤的长度(L)和宽度(W),根据下述式计算肿瘤体积:肿瘤体积(mm3)= 1/2×L×W2。 1.3.2 流式细胞术(FACS)检测
常规制备单细胞悬液,调整细胞浓度至1×107/mL。取0.1 mL细胞悬液用于FACS检测。参照文献[6]进行抗体染色剂FACS检测。 1.3.3 ELISA检测和Griess反应
参照文献[6]进行脾细胞培养并收集上清,根据相应ELISA试剂盒(美国R&D公司)说明书检测IFN-γ和TNF-α的水平。同时采用Griess反应测定上清液中NO水平。 1.4 统计分析
数据以(x±s)表示,采用SPSS 16.0软件进行数据统计分析。采用Kaplan-Meyer方法比较2组小鼠的生存期,通过Student′s t检验比较两组之间差异。P<0.05为差异有统计学意义。 2 结 果 2.1 L-Arg处理对4T1荷瘤小鼠生存期和肿瘤生长的影响
与PBS组相比,L-Arg处理组小鼠肿瘤的生长明显受到抑制(图 1A)。同时,PBS组小鼠接种4T1细胞后32~47 d全部死亡,而经L-Arg灌胃处理后,小鼠的生存期明显延长,在接种4T1细胞51 d后才开始死亡(图 1B)。
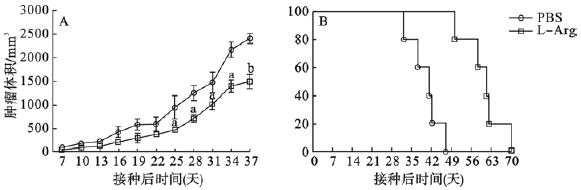 | 注:a P<0.005;b P<0.001。 图 1 L-Arg对4T1荷瘤小鼠肿瘤大小和生存期的影响 |
L-Arg处理后,荷瘤小鼠脾脏的CD3+CD4+T细胞和CD3+CD8+T细胞的比例明显高于PBS对照组小鼠。同时,ELISA结果也显示,L-Arg处理组小鼠脾细胞培养上清中的IFN-γ和TNF-α分泌水平也明显高于PBS对照组。
| 表 1 L-Arg对4T1荷瘤小鼠T细胞和巨噬细胞及培养上清中炎症因子的影响 |
尽管联合治疗手段不断创新,但乳腺癌的发病率仍在不断增加[7]。据报道,人类乳腺癌细胞系可表达精氨酸酶I[5],通过消耗机体的L-Arg,导致T细胞功能下降。而L-Arg作为一种条件必需氨基酸,当消耗大于产生能力时,必须通过食物补充以满足机体的需要。肿瘤的发生与机体的免疫功能低下密切相关。T细胞免疫在抗肿瘤的过程中发挥不可替代的作用,CD4+Th1细胞和CD8+CTL细胞是具有特异性抗肿瘤的关键效应细胞。与正常人相比,肿瘤患者往往表现为T细胞功能低下。L-Arg的消耗能够诱导T细胞的低应答状态,降低T细胞的增殖和CD3ζ链的表达[8, 9]。
CD4+Th1细胞通过分泌IFN-γ促进巨噬细胞的活化。一方面,活化的巨噬细胞可提呈肿瘤抗原给T细胞,进一步促进T细胞活化,杀伤肿瘤细胞[10]。另一方面,巨噬细胞作为效应细胞还可释放出高浓度的NO发挥肿瘤杀伤作用[11]。研究表明,高水平NO可以增强凋亡相关基因和抗致癌基因的表达水平[12]。膳食补充精氨酸可通过增加分泌NO而增强NK细胞活性,从而抑制结肠癌的发展[13]。本实验结果显示,给予L-Arg后,巨噬细胞的比例以及NO的分泌水平均明显升高。此外,NO的产生也可能是L-Arg经iNOS代谢的结果。因此,本研究进一步证实膳食补充L-Arg可作为乳腺癌的有效辅助治疗手段,其通过上调宿主的T细胞免疫应答,促进NO的产生,发挥抗肿瘤效应。
| [1] | 郑艳敏, 沈月平, 刘银梅, 等.中国女性乳腺癌危险因素Meta分析[J].中国公共卫生, 2012, 28(12):1645-1648. |
| [2] | 刘丽媛, 贾存显, 余之刚, 等.女性人群乳腺癌相关知识及影响因素分析[J].中国公共卫生, 2009, 25(10):1275-1276. |
| [3] | Luiking YC, Poeze M, Dejong CH, et al.Sepsis:an arginine deficiency state[J].Crit Care Med, 2004, 32(10):2135-2145. |
| [4] | Bronte V, Zanovello P.Regulation of immune responses by L-arginine metabolism[J].Nat Rev Immunol, 2005, 5:641-654. |
| [5] | Singh R, Pervin S, Karimi A, et al.Arginase activity in human breast cancer cell lines:N(omega)-hydroxy-l-arginine selectively inhibits cell proliferation and induces apoptosis in MDA-MB-468 cells[J].Cancer Res, 2000, 60:3305-3312. |
| [6] | Feng Y, Zhu X, Wang Q, et al.Allicin enhances host pro-inflammatory immune responses and protects against acute murine malaria infection[J].Malar J, 2012, 11:268. |
| [7] | Barron JJ, Quimbo R, Nikam PT, et al.Assessing the economic burden of breast cancer in a US managed care population[J].Breast Cancer Research and Treatment, 2008, 109:367-377. |
| [8] | Rodriguez PC, Zea AH, DeSalvo J, et al.L-arginine consumption by macrophages modulates the expression of CD3 zeta chain in T lymphocytes[J].J Immunol, 2003, 171:1232-1239. |
| [9] | Zea AH, Rodriguez PC, Culotta KS, et al.L-arginine modulates CD3zeta expression and T cell function in activated human T lymphocytes[J].Cell Immunol, 2004, 232:21-31. |
| [10] | Dunn GP, Old LJ, Schreiber RD.The immunobiology of cancer immunosurveillance and immunoediting[J].Immunity, 2004, 21:137-148. |
| [11] | Fukumura D, Kashiwagi S, Jain RK.The role of nitric oxide in tumor progression[J].Nature Reviews Cancer, 2006, 6:521-534. |
| [12] | Yin XY, Jiang JM, Liu JY, et al.Effects of endogenous nitric oxide induced by 5-fluorouracil and L-Arg on liver carcinoma in nude mice[J].World Journal of Gastroenterology, 2007, 13:6249-6253. |
| [13] | Yeh CL, Pai MH, Li CC, et al.Effect of arginine on angiogenesis induced by human colon cancer:in vitro and in vivo studies[J].The Journal of Nutritional Biochemistry, 2010, 21:538-543. |
 2014, Vol. 30
2014, Vol. 30
