良性前列腺增生(benign prostatic hyperplasia,BPH)是老年常见疾病。有研究表明,BPH的发生与年龄密切相关的神经调节因子的变化相关[1, 2]。RhoA/Rock激酶系统参与协调膀胱控尿、排尿的研究较少,为此,本研究对沈阳军区总医院2012年6月—2013年1月住院手术的BPH患者前列腺组织标本进行分析,并对照临床症状评分,以探讨两者之间的关系。现将结果报告如下。 1 对象与方法 1.1 对象
选取沈阳军区总医院2012年6月—2013年1月行经尿道前列腺电切术后病理回报为良性前列腺增生的男性患者前列腺组织石蜡标本20例,除外伴前列腺炎及上皮内瘤变(BPH组),年龄57~78岁,平均(71±7)岁。对照组为同期非病猝死的健康成人男性前列腺标本16例,年龄24~36岁,平均(31±5)岁。此研究经沈阳军区总医院伦理委员会批准。 1.2 试剂
兔抗人RhoA和Rock免疫组化试剂盒(美国加利福尼亚Epitomics公司),二抗羊抗兔试剂盒、磷酸盐缓冲盐水(phosphatic buffered saline,PBS)(上海晶美公司),S-P免疫组化相关试剂盒(福州迈新生物技术有限公司)。 1.3 方法
所有实验样本均通过10%甲醛固定液固定后,常规石蜡包埋,切片厚2 μm,脱蜡,梯度酒精水化,分别作苏木精伊红染色和免疫组化检测。病理结果均经2位病理医师分别阅片,并获得一致意见后得出结论。采用S-P免疫组化染色法[3],检测RhoA 和Rock在正常前列腺、增生前列腺中的表达。操作步骤严格按照S-P试剂盒说明操作执行。用PBS替代一抗作为阴性对照,已知表达阳性的乳腺癌组织为阳性对照。通过光学显微镜观察其着色反应。临床数据记录术前膀胱过度活动症症状评分表(overactive bladder symptom score,OABSS)和国际前列腺增生症状评分(international prostate symptom score,IPSS)。OABSS评分分级[4]:0~5分为轻度,6~11分为中度,≥12分为重度;IPSS评分分级[5]:<10分为轻度,10~20分为中度,>20分为重度。 1.4 结果判定
每张前列腺组织切片于高倍镜下随机选择5个视野,计数500个细胞,(-)和(+)的判定需根据着色细胞占肿瘤细胞数的比例来确定;阳性反应的判定是根据组织细胞核出现棕黄色颗粒。棕色颗粒在组织细胞核中呈现可分为4级[6]。阴性(-):细胞内外无淡黄及棕黄色颗粒,或阳性颗粒<10%;弱阳性(+):细胞内淡黄及棕黄色颗粒占整个切片的10%~30% ;中度阳性(++):细胞内淡黄及棕黄色颗粒占整个切片的31%~70%;强阳性(+++):细胞内淡黄及棕黄色颗粒占整个切片的70%以上。 1.5 统计分析
应用SPSS 11.0软件进行分析,样本率的比较采用χ2检验,相关性分析采用Spearman检验,P<0.05为差异有统计学意义。 2 结 果 2.1 镜下观察结果(图 1、2)
正常前列腺组织中RhoA和Rock蛋白表达阴性或弱阳性表达,而在增 生的前列腺组织中,RhoA和Rock蛋白表达阳性, 阳性着色部位主要在细胞核,呈棕黄色或棕褐色,片状和散在分布。
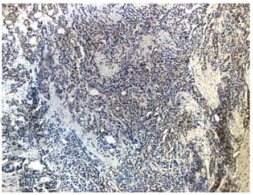 | 图 1 BPH组织中RhoA阳性表达(100×) |
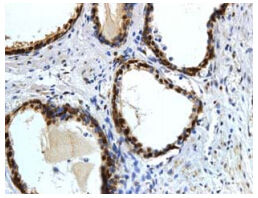 | 图 2 BPH患者前列腺组织中Rock阳性表达(400×) |
BPH组RhoA和Rock蛋白表达率明显高于正常对照组(P<0.05),结合临床数据对比发现,IPSS评分或OABSS评分高者,较IPSS评分或OABSS评分较低者前列腺中2种蛋白表达率差异有统计学意义(均P<0.05)。
| 表 1 不同组别及特征对象前列腺组织中RhoA/Rock蛋白表达情况 |
相关分析结果显示,前列腺组织中RhoA与Rock蛋白的表达水平呈正相关关系(r=0.27,P<0.01)。RhoA和Rock在增生前列腺组织中的表达与IPSS评分呈正相关(r=0.35,P<0.05),与OABSS评分呈正相关(r=0.38,P<0.05)。 3 讨 论
BPH患者主要表现为排尿症状及梗阻症状,分别是膀胱的排尿及储尿问题。出现这些下尿路症状(lower urinary tract symptoms,LUTS)的发生率随年龄增长而增加,40~50岁之间男性LUTS发生率为26%,>70岁男性则达到79%[7]。尽管LUTS/BPH与年龄相关性的确切机制不明,但随着年龄变化可引起神经介质改变[8],如NO和RhoA/Rock激酶通路。本研究显示,RhoA/Rock蛋白在BPH患者前列腺组织中表达增高,提示与BPH的发生有关。但因研究例数有限,对两者的因果关系还有待进一步研究。
副交感神经作用位点位于逼尿肌内的M受体[9]。M受体激活后可引起磷酸脂酶C的活化以及肌醇1、4、5-三磷酸(inositol trisphosphate,IP3)的水解。IP3继而引起细胞内钙的增加,钙与钙调蛋白结合激活肌球蛋白轻链激酶(myosin light-chain kinase,MLCK)。MLCK可使肌球蛋白轻链(myosin light-chain,MLC)磷酸化,继而激活肌球蛋白腺苷三磷酸(adenosine triphosphate,ATP)酶,促进肌肉收缩。MLC由MLCP去磷酸化后引起肌肉松弛[10]。平滑肌细胞收缩也受RhoA/Rock激酶调节,又称替代途径[11, 12]。Rock是一种分子量大约为160 kDa 的丝氨酸/苏氨酸激酶[13],其介导的信号通路不仅直接影响平滑肌细胞的收缩功能,还通过许多血管活性物质的相互作用与细胞粘着和迁移运动,细胞增殖分化和基因表达等细胞功能的调节,与动脉硬化,高血压和缺血性脑损害等血管性疾病的发生和发展关系密切[14]。
本研究结果显示,IPSS评分中的尿频症状评分和OABSS评分越高,RhoA/Rock的表达量越高,提示RhoA/Rock激酶参与临床症状的出现。可能原因是RhoA/Rock通过抑制MLCP的活性而上调血管平滑肌细胞的钙敏化机制,从而增强MLC的磷酸化程度,使MLC持续活化引起肌肉的持续收缩[15],引发LUTS中的储尿期症状。
膀胱的逼尿肌松弛作用主要由交感神经调节[16, 17]。膀胱颈、前列腺内的平滑肌张力同时还受RhoA/Rock激酶系统调整,RhoA/Rock激酶早在2003年就在人的前列腺组织内检测出来[18]。Rock特异性抑制剂Y-27632和fasudil可通过与ATP竞争Rock催化区的ATP 结合位点而阻断Rock的活性[19]。抑制Rock活性,可以减弱在相同钙浓度下由去甲肾上腺素诱导的前列腺尿道、膀胱颈的收缩作用,引起膀胱出口梗阻[20, 21]。McVary等[22]研究表明交感神经系统活性增高导致老年患者BPH发生率增高。本实验结论证实,前列腺增生组织中RhoA/Rock表达量明显高于正常前列腺组织,且与IPSS评分中梗阻症状评分呈正相关。即RhoA/Rock表达越多,排尿期症状即梗阻症状越明显。
神经调节因素在LUTS/BPH的发展中起着重要作用,因此,在治疗方面提出很多治疗方法及靶点,包括α受体阻滞药、M受体阻滞药、5型磷酸二酯酶(phosphodiesterase type 5,PDE5)抑制药、Y-27632。目前尚不清楚这些药物是通过直接作用于前列腺和膀胱,还是间接通过中枢神经系统发挥作用。RhoA/Rock通路的发现帮助解释了由RhoA所调节的多种细胞功能现象,现已知此通路是平滑肌收缩的重要基础,此外,RhoA/Rock通路在许多细胞功能方面均起到了关键作用。近年来,随着RhoA/Rock通路在对其他许多疾病领域的研究进展不断深入,为临床以此为靶点治疗相关疾病提供了大量的基础和临床证据,而Rock抑制剂的应用将会为这些疾病的药物治疗提供更广阔的思路与方向,也将成为今后研究的重点,对于良性前列腺增生患者,除了应用非那雄胺缩小前列腺体积的同时,通过这些药物使神经因素协调工作是治疗良性前列腺增生的治疗方向。
志谢 沈阳军区总医院泌尿外科全体医生在病例收集方面给予的协助,病理科宋福林主任、秦海明等老师给予的帮助指导
| [1] | 史新竹,宁夏,吴作艳.农村老年人高血压与前列腺增生的研究[J].中国公共卫生,2003,19(8):942-943. |
| [2] | 高新,庞俊.老年人良性前列腺增生症与内科疾病[J].中华老年医学杂志,2006,25(06):474-476. |
| [3] | 陈罡,陈峰.免疫组化SP法操作程序的规范和改良[J].医学文选,2004,23(4):419-421. |
| [4] | 杨尚琪,来永庆,陈月英,等.膀胱过度活动症症状评分表评估膀胱过度活动症的临床研究[J].中华临床医师杂志:电子版,2012,06(16):4675-4678.doi:10.3877/cma.j.issn.1674-0785.2012.16.033. |
| [5] | 那彦群,叶章群,孙光,等.中国泌尿外科疾病诊断治疗指南[M].北京:人民卫生出版社,2011:32-33. |
| [6] | Soslow RA,Dannenberg AJ,Rush D,et al.COX-2 is expressed in human pulmonary,colonic,and mammary tumors[J].Cancer,2000,89(12):2637-2645. |
| [7] | Guess HA,Arrighi HM,Metter EJ,et al.Cumulative prevalence of prostatism matches the autopsy prevalence of benign prostatic hyperplasia[J].Prostate,1990,17(3):241-246. |
| [8] | 罗文娟,尹雪艳.代谢综合征与良性前列腺增生的关系[J].医学综述,2013,19(9):1650-1652. |
| [9] | Caulfield MP,Birdsall NJ.International Union of Pharmacology.XVII.Classification of muscarinic acetylcholine receptors[J].Pharmacol Rev,1998,50(2):279-290. |
| [10] | Somlyo AP,Somlyo AV.Signal transduction by G-proteins,rho-kinase and protein phosphatase to smooth muscle and non-muscle myosin II[J].J Physiol,2000,522 Pt 2:177-185. |
| [11] | Kimura K,Ito M,Amano M,et al.Regulation of myosin phosphatase by Rho and Rho-associated kinase(Rho-kinase)[J].Science,1996,273(5272):245-248. |
| [12] | Shimokawa H.,Takeshita A.Rho-kinase is an important therapeutic target in cardiovascular medicine[J].Arterioscler Thromb Vasc Biol,2005,25(9):1767-1775. |
| [13] | Wettschureck N,Offermanns S.Rho/Rho-kinase mediated signaling in physiology and pathophysiology[J].J Mol Med(Berl),2002,80(10):629-638. |
| [14] | Loirand G,Guerin P,Pacaud P.Rho kinases in cardiovascular physiology and pathophysiology[J].Circ Res,2006,98(3):322-334. |
| [15] | Peters SL,Schmidt M,Michel MC.Rho kinase:a target for treating urinary bladder dysfunction?[J].Trends Pharmacol Sci,2006,27(9):492-497. |
| [16] | Christ GJ,Andersson KE.Rho-kinase and effects of Rho-kinase inhibition on the lower urinary tract[J].Neurourol Urodyn,2007,26(6 Suppl):948-954. |
| [17] | Michel MC,Vrydag W.Alpha1-,alpha2- and beta-adrenoceptors in the urinary bladder,urethra and prostate[J].Br J Pharmacol,2006,147 Suppl 2:S88-119. |
| [18] | Rees RW,Foxwell NA,Ralph DJ,et al.Y-27632,a Rho-kinase inhibitor,inhibits proliferation and adrenergic contraction of prostatic smooth muscle cells[J].J Urol,2003,170(6 Pt 1):2517-2522. |
| [19] | Noma K,Oyama N,Liao JK.Physiological role of ROCKs in the cardiovascular system[J].Am J Physiol Cell Physiol,2006,290(3):C661-668. |
| [20] | Takahashi R,Nishimura J,Seki N,et al.RhoA/Rho kinase-mediated Ca2+ sensitization in the contraction of human prostate[J].Neurourol Urodyn,2007,26(4):547-551. |
| [21] | 杨志刚,刘和,常义,等.前列腺增生致膀胱出口梗阻患者逼尿肌神经生长因子表达及超微结构改变[J].现代泌尿外科杂志,2010,15(4):274-276. |
| [22] | McVary KT,Rademaker A,Lloyd GL,et al.Autonomic nervous system overactivity in men with lower urinary tract symptoms secondary to benign prostatic hyperplasia[J].J Urol,2005,174(4 Pt 1):1327-1433. |
 2013, Vol. 29
2013, Vol. 29


