2. 青冈县畜牧兽医局
非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)是一种无过量饮酒史、以肝实质细胞脂肪变性和脂肪贮积为特征的临床病理综合征。NAFLD常伴有肥胖及胰岛素抵抗[1],脂质代谢紊乱也常被认为是脂肪肝发生的关键环节之一,然而其发病机制尚不完全清楚[2]。目前,针对NAFLD的治疗仍以预防为主,并无特效的治疗药物。本研究通过逆转录-聚合酶链反应(reverse transcription-PCR,RT-PCR)技术检测NAFLD模型小鼠肝组织内过氧化物酶增殖活化受体α(peroxisome proliferator-activated receptor-α,PPARα)和解偶联蛋白2(uncoupling protein-2,UCP-2)mRNA表达水平变化,进一步了解NAFLD的发病机制。结果报告如下。 1 材料与方法 1.1 主要试剂与仪器
Trizol试剂(美国invitrogen公司),dNTP、Taq酶及标准分子量DNA-marker(日本TaKaRa Biotech公司),一步法cDNA第一链反转录试剂盒(哈尔滨海基生物科技有限公司)。台式高速冷冻离心机(德国Sigma公司);S1000 Thermal Cyclery型PCR仪(美国Bio-RAD公司);JY3000+型多用途电泳仪(北京君意东方电泳设备有限公司);ChampGelTM 6000全自动凝胶成像分析系统(北京赛智创业科技有限公司);NanoDrop 2000核酸蛋白分光光度计(美国Thermo公司)。 1.2 实验动物与分组
雄性成年ICR小鼠(中国农业科学院哈尔滨兽医研究所)30只,体重18~20 g。许可证号:SCXK(黑)2006-009。将动物随机分成3组,每组10只,对照组以标准饲料喂养8周;NAFLD模型A组以正常饲料喂养4周,再以高脂饲料喂养4周;NAFLD模型B组以高脂饲料喂养8周。 1.3 指标及检测 1.3.1 小鼠体重、肝重及肝指数测定
处死前分别测定各组小鼠的体重(g)和肝脏湿重(g),并计算肝指数(肝指数=肝湿重/体重×100%)。 1.3.2 肝脏病理切片观察
将游离出的小鼠肝脏组织分成2份,一部分固定于4%甲醛溶液中,制作成石蜡切片,苏木素-伊红染色(hematoxylin-eosin staining,HE),观察病理改变。其余肝脏组织于-80 ℃低温冰箱内冻存备用。 1.3.3 RT-PCR
总RNA提取按照试剂盒说明书进行,提取的总RNA经反转录后进行PCR反应。利用美国国立生物技术信息中心(National Center for Biotechnology Information,NCBI)在线资源,参考小鼠PPARα基因和UCP-2基因的mRNA序列,以甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)基因作为内标基因,应用PrimerPremier 5.0软件设计引物,引物序列(上海英骏生物技术有限公司合成)如下:PPARα:上游5′- CACAATGCAATTCGCTTTGG-3′;下游5′- TCTTTCCCGCGAGTATGA-3 ′。UCP-2:上游5′-CGGAGATACCAGAGCACTGTC-3′;下游5′-TGGCATTTCGGGCAACATTGG-3′。GAPDH:上游5′-ACAGTCCATGCCATCACTGCC-3′;下游5′-GCCTGCTTCACCACCTTCTTG -3′。PCR扩增:取上述反转录反应产物于20 μL反应体系中进行PCR反应。反应体系为:0.8 μL cDNA产物、0.2 μLTaq酶、基因上下游引物各0.8 μL、dNTP 1.6 μL、2 μL 10×Buffer,13.8 μL ddH2O。反应程序如下:94 ℃预变性4 min,94 ℃变性30 s,57 ℃退火30 s,72 ℃延伸30 s,30个循环,72 ℃延伸5 min。取8 μL PCR反应产物经2%琼脂糖凝胶电泳,利用ChampGelTM 6000全自动凝胶成像分析系统进行拍照。运用Bandscan软件进行图像分析,计算目的基因mRNA相对表达量。 1.4 统计分析
计量资料用x±s表示,所有数据均采用SPSS 17.0统计软件进行分析,组间均数的比较采用t检验,P<0.05为差异有统计学意义。 2 结 果 2.1 各组小鼠体重、肝脏湿重及肝指数变化(表 1)
与对照组小鼠比较,NAFLD模型组小鼠体重呈下降趋势,肝指数明显升高(P<0.05)。
| 表 1 小鼠体重、肝脏湿重及肝指数比较(x±s,n=10) |
肉眼观察对照组小鼠肝脏无异常变化,色泽鲜红,表面光滑,边缘锐利,富有弹性。NAFLD模型组小鼠肝脏体积增大,呈奶黄色,表面粗糙有油腻感,可见小颗粒状突起,边缘钝而厚。光镜观察对照组未显示明显病变(图 1A),模型A组小鼠可见肝细胞形态大体正常,伴有肝细胞肿胀,出现小泡性肝脂肪变,肝细胞内有脂滴沉积,肝小叶边缘区多量脂肪空泡(图 1B);模型B组小鼠可见肝细胞体积明显变大、脂肪变性明显,胞质内脂滴大小不一,包浆内充满多量脂肪空泡,有淋巴细胞浸润灶(图 1C)。
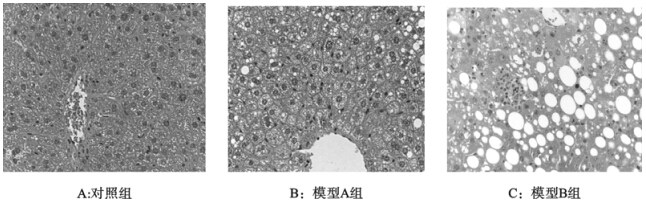 | 图 1 各组小鼠肝脏病理观察(HE,×400) |
对照组、模型A、B组小鼠肝组织中PPARα mRNA相对表达量分别为(1.16±0.27)、(0.63±0.33)和(0.45±0.19),对照组比较,模型B组小鼠肝组织PPARα mRNA相对表达量下降(P<0.01)。对照组、模型A、B组小鼠肝组织中UCP-2 mRNA相对表达量分别为(0.25±0.13)、(0.67±0.76)和(0.89±0.52),与对照组比较,模型组表达量升高,差异有统计学意义(P<0.01)。
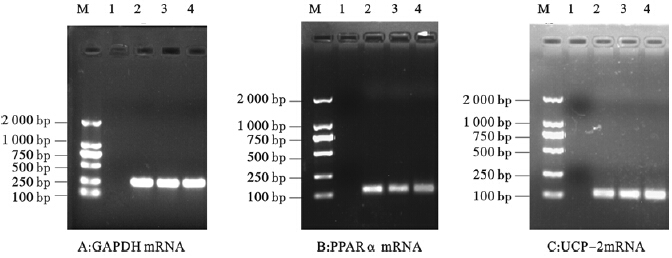 | 注: M:DNA Marker;1:阴性对照;2:对照组;3~4:模型A、B组。 图 2 各组小鼠肝组织GAPDH、PPARα和UCP-2 mRNA表达 |
脂质在肝脏内的蓄积对NAFLD的发生可能会产生直接影响[3],在NAFLD中脂质代谢相关基因表达水平改变会增加脂肪酸的合成[4]。本研究结果显示,NAFLD小鼠肝组织中PPARα和UCP-2 mRNA表达量变化明显,提示这2种基因可能在NAFLD形成的分子机制中发挥重要作用。PPARα在脂质代谢中起调节作用[5],其活化可促进脂肪酸氧化分解,降低高密度脂蛋白水平。本研究结果表明,与对照组比较,模型组小鼠肝组织中 PPARα mRNA相对表达量下降,提示可能引起一系列与脂质代谢相关的蛋白质和酶基因转录水平降低,使肝脏线粒体内脂肪酸的β氧化能力减弱,引发脂质堆积。脂肪沉积的肝细胞可发生脂性改变,诱发和加剧胰岛素抵抗及炎症反应,促进NAFLD发生[6]。
解偶联蛋白是一种与机体能量代谢相关的线粒体载体蛋白[7],UCP-2可调节脂肪酸的β氧化,促进线粒体内脂肪酸分解[8]。肝脏内UCP-2基因可受多因素调节而表达升高,使活性氧产量下降,抑制脂质在肝脏内的沉积,预防脂肪肝。本研究结果表明,与对照组比较,模型组小鼠肝组织中UCP-2 mRNA表达升高,但肝脏却发生明显的脂性变化。提示UCP-2 mRNA表达量可能超过了机体的代偿能力。有研究显示,NAFLD疾病发生时UCP-2基因表达上调可消耗腺嘌呤核苷三磷酸(adenosine triphosphate,ATP)储备,间接抑制脂质合成,促进脂肪酸β氧化,减轻脂质在肝脏细胞内的蓄积。但ATP减少会使机体对外界刺激敏感性增加,抗应激能力减弱,使机体对“二次打击”的防御能力下降,增加了NAFLD发生的可能性[9]。在NAFLD发生过程中,UCP-2的调节作用十分复杂,其作用机制有待进一步研究。
| [1] | Choudhury J,Sanyal AJ.Insulin resistance and the pathogenesis of nonalcoholic fatty liver disease[J].Clin Liver Dis,2004,8(3):575-594. |
| [2] | 管石侠,张宝,马泰,等.脂肪肝合并腹型肥胖患者抵抗素与胰岛素抵抗关系[J].中国公共卫生,2012,28(5):687-688. |
| [3] | Musso G,Gambino R,Cassader M.Recent insights into hepatic lipid metabolism in non-alcoholic fatty liver disease(NAFLD)[J].Progress in Lipid Research,2009,48(1):1-26. |
| [4] | 李莹,顾长好,张玮.非酒精性脂肪肝发病机制的研究进展[J].中国煤炭工业医学杂志,2009,12(10):1648-1650. |
| [5] | Luquet S,Gaudel C,Holst D,et al.Roles of PPAR delta in lipid absorption and metabolism:a new target for the treatment of type 2 diabetes[J].Biochimicaet Biophysica Acta(BBA)-Molecular Basis of Disease,2005,1740(2):313-317. |
| [6] | 施军平,陈芝荟,包剑锋,等.高脂饮食诱导的非酒精性脂肪性肝病大鼠肝组织PPARα和CRT-I mRNA的表达[J].浙江中医药大学学报,2007,31(1):52-55. |
| [7] | 付荣霞,孙长颢,王舒然,等.饲料构成影响大鼠解偶联蛋白-2基因的表达[J].中国公共卫生,2002,18(7):771-773. |
| [8] | 梁坚,王婉梅,揭育丽,等.脂肪肝患者血清瘦素与胰岛素抵抗的关系[J].中国临床康复,2004,8(27):5847-5849. |
| [9] | 张一帆,卿笃信.解偶联蛋白2及其与脂肪肝的关系[J].医学信息,2011(6):2586. |
 2013, Vol. 29
2013, Vol. 29


