鼻咽癌是一种头颈部上皮来源的恶性肿瘤,好发于中国南方地区,起病隐匿,转移早,易复发,严重危害人类生命健康[1]。研究认为鼻咽癌发病与爱波斯坦-巴尔病毒(Epstein Barr Virus,EBV)感染、环境因素以及遗传因素密切相关[2]。微小RNA(microRNA,miRNAs)是一类内源性非编码小RNA,由21~24个核苷酸组成,参与重要的生物学过程,与肿瘤发生密切相关[3, 4]。研究显示,miRNAs与鼻咽癌发生亦存在密切关联[5]。为探讨鼻咽癌病因,本研究采用病例对照方法和分子生物学检测手段,分析了miR499和miR608成熟体的遗传变异与中国南方人群鼻咽癌发病风险关系。结果报告如下。 1 材料与方法 1.1 对象
收集2010年5月—2011年5月广州医学院附属肿瘤医院和广州医学院第一附属医院的原发性鼻咽癌病例,共612例,其中男368例,女244例,年龄16~93岁,平均(54.2±10.2)岁。按性别相同、年龄(±3岁)进行匹配,从参加社区健康体检的人群中选取612名对照。其中男性364人,女性248人,年龄18~85岁,平均(55.1±11.3)岁。纳入和排除标准:病例为经组织病理学检查确诊,尚未进行化疗或放疗的原发性鼻咽癌病例。该研究经广州医学院伦理委员会同意,且调查之前被调查者签署知情同意书。 1.2 问卷调查及标本收集
采用自行编制的流行病学问卷,调查内容包括人口学基本资料、吸烟、饮酒、癌症家族史、EBV病毒感染等项目。由经统一培训的调查员,在鼻咽癌病例确诊后的1周内进行面对面访谈,询问并填写有关项目;亦以相同的调查方式收集对照组资料,并随机抽取5%病例和对照进行复查,以保证问卷质量。抽取调查对象5 mL血液用于DNA提取及基因分型检测。 1.3 基因分型 1.3.1 DNA提取
用TianGen公司的0.1~20 mL血液基因组DNA提取试剂盒(DP319-02),取2 mL抗凝外周血,依其说明书提取研究对象的基因组DNA。 1.3.2 SNP位点选择
以GenBank和miRbase(version 16.0)生物信息学数据库为基础,按照较少等位基因频率(minor allele frequency,MAF)不小于5%原则,发现在中国人群中位于miRNAs成熟体的单核苷酸多态位点只有hsa-miR-499(rs3746444 T→C)和hsa-miR-608(rs4919510 C→G)。因此选取这2个位点进行分析。 1.3.3 TaqMan基因型检测方法
利用Primer Express 3.0软件(Applied Biosystems,USA) 设计所选取多态位点的引物和MGB荧光探针序列,委托ABI公司合成和校验(rs3746444 T→C引物F:GGCTGTTAAGACTTGCAGTGATGT,R:ACGGGAAGCAGCACAGACTT;探针P1:FAM-CACGTGAACTTCACAG-MGB,P2:HEX-CACGTGAACCTCACAG-MGB;rs4919510 C→G引物F:TCCCCAGCCCCATTTTCT,R:AAGATCCACTGGGCCAAGGT;探针P1:FAM-TAAACGGAGCTGTCC-MGB,P2:HEX-TAAACGCAGCTGTCC-MGB)。PCR 反应体积为10 μL,内含约200 ng的DNA 1 μL,Master mix 5 μL,上下游引物与探针各0.1 μL,ddH2O 3.6 μL。在PCR基因扩增仪(Applied Biosystems 2720)上进行PCR扩增,扩增条件为 95℃预热10 min,95 ℃变性15 s,60 ℃退火延伸60 s,共45个循环。用Applied Biosystems 7500 仪器上的基因分型程序判断每个检测样本基因型。 1.4 测序验证
用随机数字表法抽取病例和对照组各30例样本,以测序引物(rs3746444 T→C 引物F:CTTCACTTCCCTGCCAAATCC,R:GCCCACAGAGCGACATTCC;rs4919510 C→G引物F:AGCATCAGCCCTTTCCAG,R:CCAGCAGCATCAACTTC-AC)进行普通PCR扩增,扩增产物送Invitrogen公司测序,以验证TaqMan 检测结果真实性与准确性。 1.5 统计分析 运用SAS 9.13软件进行两独立样本t检验,χ2检验,并对所研究位点基因型在对照组中的分布进行Hardy-Weinberg平衡检验;非条件logistic回归分析多态位点与人群发生鼻咽癌关联。OR值及95%CI表示关联强度;P<0.05为差异有统计学意义。 2 结 果 2.1 研究对象基本特征
鼻咽癌病例按临床分期,Ⅰ期25例(4.0%),Ⅱ期157例(25.7%),Ⅲ期258例(42.2%),Ⅳ期172例(28.1%);EBV病毒感染阳性393例(64.2%),阴性184例(30.1%),不详35例(5.7%)。性别、年龄、吸烟、饮酒和癌症家族史等因素在病例与对照2组之间差异均无统计学意义(P>0.05)。 2.2 基因型判断及验证(图 1)
应用TaqMan技术检测研究对象的多态位点基因型随机抽取的60例样本经测序验证,证实其基因型与TaqMan方法检测结果一致,表明TaqMan检测方法准确可靠。
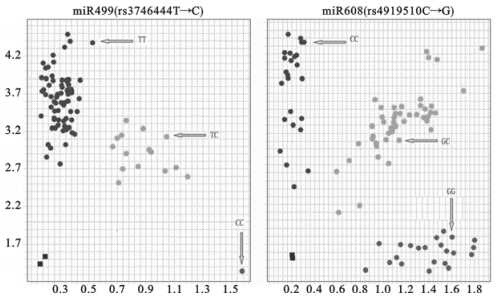 | 图 1 miR499(rs3746444 T→C)和miR608(rs4919510 C→G)多态位点基因分型图 |
miR499(rs3746444 T→C)和miR608(rs4919510 C→G)各基因型频率在病例与对照组之间差异具有统计学意义(P<0.01)。多因素非条件logistic 回归分析显示,以rs3746444 TT基因型为参照,携带rs3746444 C变异基因型(TC+CC)个体发生鼻咽癌的危险增加44%(OR=1.44,95%CI=1.13~1.82);而携带rs4919510(GC+GG)基因型个体发生鼻咽癌的风险是携带CC基因型的1.58倍(OR=1.58,95%CI=1.21~2.07);有明显剂量-效应关系(P<0.01)。
| 表 1 miR499和miR608基因型频率分布与鼻咽癌风险性 |
鼻咽癌是中国南方及东南亚地区常见的一种恶性肿瘤,其发生发展是一个多因素、多阶段、多步骤遗传变异积累的复杂过程。目前鼻咽癌发病的分子遗传机制仍未完全阐明。miRNAs是一类内源性非编码小RNA,通过与靶基因信使RNA 3′非翻译区(3′-untranslated region,3′-UTR)的互补配对,降解靶信使RNA或者抑制其翻译过程,调节靶基因表达水平。大量研究发现miRNAs参与了细胞生长、分化、增殖、凋亡等多种生物学过程,尤其在肿瘤发生发展过程中扮演了重要角色,起着癌基因或抑癌基因的类似功能[3, 4]。miRNAs成熟体的遗传变异,包括单核甘酸多态性可影响其加工过程及对靶基因的结合,引起不同生物学效应[6]。研究表明miRNAs单核苷酸多态与肺癌、乳腺癌等肿瘤的发生及预后密切关联[7, 8, 9]。miRNAs在鼻咽癌发生发展及转移等过程亦起着重要作用[10]。Deng等人报道了miR216通过调节靶基因基尔斯滕大鼠肉瘤病毒癌基因(v-Ki-ras2 Kirsten rat sarcoma viral oncogene homolog,KRAS)的蛋白表达水平而抑制鼻咽癌肿瘤细胞生长及转移[10]。本研究结果显示miR499(rs3746444 T→C)和miR608(rs4919510 C→G)的遗传变异均可增加鼻咽癌发病危险,与凌晓璇等[7]结果一致,推测这2个位点可能是通过影响与鼻咽癌发病相关基因表达,进而促进鼻咽癌发生,但具体肿瘤生物学机制需通过功能学实验进一步验证。
综上所述,miR499(rs3746444 T→C)和miR608(rs4919510 C→G)多态与南方人群鼻咽癌发病风险存在关联,为鼻咽癌易感人群的筛选提供了一个潜在的遗传标志。但本研究是基于医院的病例对照研究,所获关联结果仍需在多种族、大样本人群中去验证。
| [1] | Chin D,Boyle GM,Porceddu S,et al.Head and neck cancer:past,present and future[J].Expert Rev Anticancer Ther,2006,6(7):1111-1118. |
| [2] | Deyrup AT.Epstein-Barr virus-associated epithelial and mesenchymal neoplasms[J].Hum Pathol,2008,39(4):473-483. |
| [3] | Esquela-Kerscher A,Slack FJ.Oncomirs-microRNAs with a role in cancer[J].Nat Rev Cancer,2006,6(4):259-269. |
| [4] | Lu J,Getz G,Miska EA,et al.MicroRNA expression profiles classify human cancers[J].Nature,2005,435(7043):834-838. |
| [5] | Li T,Chen JX,Fu XP,et al.microRNA expression profiling of nasopharyngeal carcinoma[J].Oncol Rep,2011,25(5):1353-1363. |
| [6] | Duan R,Pak C,Jin P.Single nucleotide polymorphism associated with mature miR-125a alters the processing of pri-miRNA[J].Hum Mol Genet,2007,16(9):1124-1131. |
| [7] | 凌晓璇,黎银燕,杨磊,等.肺癌与人微小RNA miR-499-3p种子序列遗传变异关系[J].中国公共卫生,2011,27(9):1105-1107. |
| [8] | Hu Z,Chen J,Tian T,et al.Genetic variants of miRNA sequences and non-small cell lung cancer survival[J].J Clin Invest,2008,118(7):2600-2608. |
| [9] | Hu Z,Liang J,Wang Z,et al.Common genetic variants in pre-microRNAs were associated with increased risk of breast cancer in Chinese women[J].Hum Mutat,2009,30(1):79-84. |
| [10] | Deng M,Tang H,Zhou Y,et al.miR-216b suppresses tumor growth and invasion by targeting KRAS in nasopharyngeal carcinoma[J].J Cell Sci,2011,124(Pt 17):2997-3005. |
 2013, Vol. 29
2013, Vol. 29


