砷是一种特殊的毒物,一方面高浓度砷暴露具有极强的急、慢性毒性,另一方面临床上采用大剂量的砷剂能够有效治疗急性早幼粒细胞白血病[1]。 2010 年12 月美国航空航天局在Science 杂志上提出砷可能是六大基本生命元素碳、氢、氧、氮、磷和硫之外的第7 种元素的假说[2]。NF-E2 相关因子2 ( nuclear factor erythroid 2-related factor 2,Nrf2) 是转录因子中CNC( cap‘n’collar) 家族中重要一员,Nrf2 和它的细胞质接头蛋白Keap1 是细胞抗氧化反应的中枢调节者[3]。在众多Nrf2 调控的下游抗氧化酶和Ⅱ相解毒酶中,NAD( P) H: 醌氧化还原酶 1[NAD( P) H: quinone oxidoreductase 1,NQO1]和血红素单加氧酶-1 ( heme oxygenase-1,HO-1) 受到了广泛关注,两者具有很强的细胞保护功能。肝脏是机体内物质代谢、生物转化重要器官。动物实验和人群流行病学调查也均表明,肝脏是砷的代谢和甲基化场所,也是其毒作用的主要靶器官之一。而目前对于砷暴露后,肝脏系统Nrf2 信号通路的活化情况研究较少。本研究观察了不同时间和浓度亚砷酸钠( NaAsO2 ) 暴露对人类肝细胞的Nrf2 及Nrf2 调控的下游NQO1 和HO-1 蛋白表达的影响。
1 材料与方法 1.1 仪器与试剂SW-CJ-1FD 型超净工作台( 苏净集团安泰公司) ; CO2 恒温培养箱( 荷兰Heraeus 公司) ; 电泳仪、AE-6677 型转膜仪( 日本ATTA 公司) ; 半自动酶标仪( 芬兰labsystems 公司) ; IMAGER 5500 型电泳凝胶成像分析仪( 美国ALPHA 公司) ; 亚砷酸钠( sodium arsenite,NaAsO2 ,纯度≥ 99.0%,美国Fluka 公司) ,磷酸盐缓冲液( phosphate buffered solution,PBS,美国Sigma 公司) ,RPMI 1640 培养基( 美国Gibco 公司) ,胰蛋白酶( 美国 Gibco 公司) ,胎牛血清( fetal bovine serum,FBS,天津市灏洋生物制品科技有限责任公司) ,细胞裂解液( 50 mmol /L 三羟甲基氨基甲烷碱,150 mmol /L NaCl,0.1%十二烷基磺酸钠,0.5%去氧胆酸钠,1 % Nonidet P-40,100 mg /L 苯甲基磺酰氟) ,硝酸纤维素膜 ( 美国Millipore 公司) ,Nrf2 抗体( H-300) 、HO-1 抗体( H-105) 、NQO1 抗体( A180) 和β-actin 抗体( I-19) ( 美国Santa Cruz 公司) ,辣根过氧化物酶标记的羊抗兔/小鼠IgG( ZB-2301,中衫金桥公司) ,显色剂( SuperSignal West Pico Chemiluminescent Substrate,美国Pierce 生物技术公司) ,Bio-Rad 蛋白测定试剂盒( 美国Bio-Rad 公司) ,预染蛋白marker ( pre-stained protein ladder,美国Fermentas 公司) 。
1.2 细胞培养和染毒Chang 肝细胞系购自中科院上海细胞库( 编号为ZN1003) 。于RPMI 1640 培养基( 含10% FBS,1 × 105 U /L 青、链霉素) ,5% CO2、37 ℃条件下培养。待细胞进入对数生长期,0.25%胰蛋白酶消化,吹打均匀,以1∶ 3 传代培养。 待细胞融合率达80% 以上时,进行染毒。NaAsO2 终浓度分别为0( 对照组) 、10、25 和50 μmol /L,染毒时间为2、4、6、12 和24 h。
1.3 蛋白提取染砷终点弃去含砷培养液,PBS 清洗3 次,加入细胞裂解液冰上裂解20 min 后,收集细胞悬液,4 ℃ 12 000 × g 离心2 min 后,取上清液保存于-80 ℃ 备用。样品蛋白浓度采用Bio-Rad 试剂盒法进行测定。
1.4 免疫印迹法( western blot)以10%的十二烷基磺酸钠-聚丙烯酰胺凝胶电泳分离蛋白。特异性一次抗体为抗Nrf2、NQO1、HO-1 和β-actin 抗体; 特异性二次抗体为辣根过氧化物酶标记的羊抗兔/ 小鼠IgG。底物化学发光( enhanced chemiluminescence ,ECL) 检测底物的表达。凝胶成像分析系统分析和计算蛋白的灰度值。最终结果用各实验组的平均灰度值与对照组的平均灰度值的相对比值表示。共进行独立实验3 次。
1.5 统计分析数据以x±s表示,用SPSS 16.0 统计软件进行统计分析,多组间比较采用单因素方差分析( one-way ANOVA) 。P<0.01 为差异有统计学意义。
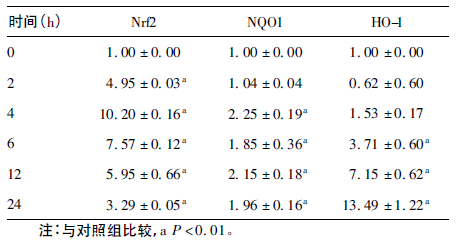
2 结果 2.1 25 μmol /L NaAsO2 对Chang 肝细胞Nrf2、 NQO1 和HO-1 蛋白表达的影响( 表 1、图 1)| 表 1 25 μmol /L NaAsO2 对Chang 肝细胞Nrf2、NQO1 和 HO-1 蛋白表达影响(x±s,n = 3) |
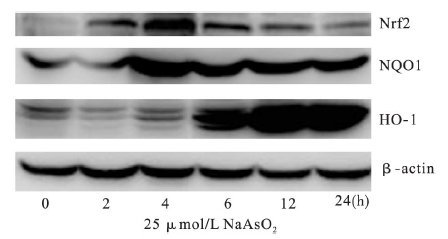 | 图 1 25 μmol /L NaAsO2 对Chang 肝细胞Nrf2、NQO1 和 HO-1 蛋白表达影响(x±s,n = 3) |
除暴露2 h 组的HO-1 和NQO1 蛋白、以及暴露4 h 组的 HO-1 蛋白之外,2 5 μmol /L NaAsO2 暴露2、4、6、12 和24 h,Chang 肝细胞的Nrf2、NQO1 和HO-1 蛋白表达均明显高于对照组(P<0.01) ; Nrf2 蛋白2 h 就开始明显诱导,4 h 表达水平最高,此后随暴露时间的延长虽然表达有所下降,但持续至24 h 仍明显高于对照组; NQO1 的蛋白表达水平从4 h 开始即增加至对照组的2.25 倍,6 、12 和24 h 的蛋白表达水平也持续明显高于对照组(P<0.01) ; 而HO-1 的蛋白表达则从6 h 开始明显诱导,且随暴露时间的继续延长表达持续上升,具有明显的时间-效应关系(P<0.01) 。
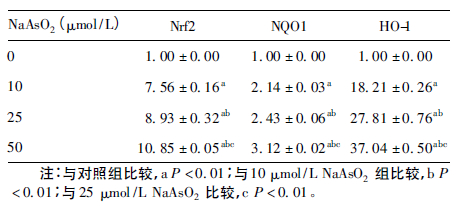
2.2 不同浓度NaAsO2 对Chang 肝细胞Nrf2、NQO1 和HO-1 蛋白表达的影响( 表 2、图 2)| 表 2 不同浓度NaAsO2 对Chang 肝细胞Nrf2、NQO1 和 HO-1 蛋白表达影响(x±s,n = 3) |
 | 图 2 不同浓度NaAsO2 对Chang 肝细胞Nrf2、NQO1 和 HO-1 蛋白表达影响(x±s,n = 3) |
10、25 和50 μmol /L NaAsO2 染毒6 h,Nrf2、NQO1 和HO-1 的蛋白表达均随染毒剂量的增加而大量诱导,具有明显的剂量-效应关系(P<0.01) 。
3 讨论Nrf2-Keap1 /ARE 通路是迄今为止发现的最为重要,也是一种复杂的内源性抗氧化应激通路[4]。 生理情况下,Keap1 与Nrf2 紧密结合,Nrf2 被降解,抑制其诱导靶基因的表达[5]。当机体处于氧化应激状态时,Nrf2 与Keap1 解离[5],由胞质转入胞核中,识别并与抗氧化反应元件( antioxidant response element ,ARE) 结合,启动II 相解毒酶和抗氧化酶基因的转录,提高细胞抗氧化应激能力。本研究发现,NaAsO2 暴露能够诱导Chang 肝细胞Nrf2、NQO1 和HO-1 蛋白表达增强,且具有一定的剂量-效应关系。提示,在Chang 肝细胞中,NaAsO2 暴露能够活化Nrf2 信号通路,启动下游抗氧化酶的基因表达,增强机体对于氧化应激的抵抗力。
NQO1 是一种调节细胞内物质处于氧化还原状态的黄素酶,它以NAD( P) H 为受体,催化醌类及其衍生物,使其失去2 个电子,发生还原反应,其催化特性在于无单电子还原产物半醌及自由基等氧化产物形成,对各种代谢引起的氧化应激反应具有保护作用。HO-1 是血红素降解的限速酶,近年研究发现,HO-1 的抗氧化功能一方面与其阻止游离血红素参与氧化反应有关,另一方面,HO-1 及其酶解产物胆红素,CO 共同发挥着抗氧化、抗炎、抑制细胞凋亡和扩血管、改善组织微循环等作用,广泛参与心、脑、 肺、肝、肾等组织细胞的抗氧化应激损伤,是机体最重要的内源性保护体系之一。研究还发现,HO-1 的蛋白表达情况与Nrf2 的蛋白表达情况并不完全一致: 25 μmol /L 的NaAsO2 暴露Chang 肝细胞后,Nrf2 蛋白表达在2 h 即开始增强,4 h 达到高峰,此后随暴露时间延长表达有所下降; 而HO-1 蛋白表达在6 h 才开始明显诱导,并且随时间的增加而显著增强,具有明显的时间-效应。这些结果提示,可能有其他通路参与HO-1 的调控。研究发现,另一种核转录因子AP-1 也对HO-1 具有重要的调节作用[6],还有研究表明刺激物可通过诱导NF-κB( nuclear factor-kappa B) 上调HO-1 基因表达[7],最新的研究报道HO-1 基因的表达需要另一种核转录抑制因子 Bach1 的失活作为前提[8]。因此,目前认为HO-1 的表达要受到以Nrf2 调控为主的多种信号途径的共同调控。
综上所述,本研究表明,NaAsO2 暴露可以诱导人类肝细胞Nrf2 信号通路的活化,增强细胞对于氧化应激的抵抗力,为进一步了解砷的生物学作用和意义具有重要作用。
| [1] | Powell BL.Arsenic trioxide in acute promyelocytic leukemia:potion not poison[J].Expert Rev Anticancer Ther,2011,11(9):1317-1319. |
| [2] | Wolfe-Simon F,Blum JS,Kulp TR,et al.A bacterium that can grow by using arsenic instead of phosphorus[J].Science,2010,332(6034):1163-1166. |
| [3] | Cho HY,Reddy SP,Kleeberger SR.Nrf2 defends the lung from oxidative stress[J].Antioxid Redox Signal,2006,8 (1-2):76-87. |
| [4] | 钟敏.Nrf2-Keap1 抗氧化系统研究进展[J].中国公共卫生,2006,22(3):360-362. |
| [5] | Li W,Kong AN.Molecular mechanisms of Nrf2-mediated antioxidant response[J].Mol Carcinog,2009,48(2):91-104. |
| [6] | Harada H,Sugimoto R,Watanabe A,et al.Differential roles for Nrf2 and AP-1 in upregulation of HO-1 expressionby arsenit in murine embryonic fibroblasts[J].Free Radical Research,2008,42(4):297-304. |
| [7] | Li Q,Guo Y,Ou Q,et al.Gene transfer of inducible nitric oxide synthase affords cardioprotection by upregulating heme oxygenase-1 via a nuclear factor-{ kappa} B-dependent pathway[J].Circulation,2009,120(13):1222-1230. |
| [8] | Reichard JF,Motz GT,Puga A.Heme oxygenase-1 induction by NRF2 requires inactivation of the transcriptional repressor BACH1[J].Nucleic Acids Res,2007,35(21):7074-7086. |
 2012, Vol. 28
2012, Vol. 28