2. 北镇市疾病预防控制中心;
3. 辽宁省疾病预防控制中心
流感病毒根据病毒颗粒核蛋白和基质蛋白抗原特性及其基因型特征的不同,分为甲(A) 、乙(B) 、丙(C) 3型,每型又可分为不同的亚型。流感病毒主要以 A型和 B型感染人类,A型流感病毒以 H1、H3、H5为常见致病亚型,近年发现的高致病性禽流感病毒,也可跨越种群障碍对人类造成感染[1, 2]。流感病毒具有不同的毒力与传播特性,给感染性疾病的诊断与治疗带来很大困难。因此,快速鉴别病毒型别成为提高治疗效果和控制病毒扩散的关键。本研究采用一种快速、敏感的多重反转录聚合酶链式反应(reverse transcription-PCR,RT-PCR)检测方法,优化混合反应体系,可克服病毒分离培养、血清学诊断及普通 RT-PCR检测的缺点,在 1次反应中同时检测 A型和 B型 2种流感病毒。
1 材料与方法 1.1 材料2009年 9月—2011年 7月,采集辽宁医学院附属第一医院和锦州市中心医院 2家哨点医院疑似流感样患者咽拭子样本,共采 2 871份。采样后保存 Hank’ s采样液中,暂存 4 ℃冷藏冰箱,48 h内送至辽宁省锦州市疾病预防控制中心实验室,冻存于-80 ℃冰箱,48 h内完成检测。
1.2 主要试剂与仪器流感病毒 RNA提取试剂盒 QIAGEN Rneasy Mini Kit、RNA扩增试剂盒 QIAGEN one-step RT-PCR Kit(德国 QIAGEN公司) ; IQ5型实时荧光定量 PCR扩增仪(美国 BIO-RAD公司) ; PeQSTAR型 PCR扩增仪(德国 PEQLAB GmbH公司) ; Biospectrum-AC型自动凝胶成像仪(美国 UVP公司) 。
1.3方法A型与 B型流感病毒引物设计分别选择在流感病毒的高度保守序列 M和 Ns基因上。病毒序列均下载自 NCBI GenBank数据库,特异性高的片段被选作引物设计的区域,由 premier 5.0软件设计完成,上海生工生物工程技术服务有限公司合成。引物序列如下: FluA-M-F30: 5'-TTCTAACCGAGGTCGAAACG-3'; FluA-M-R264: 5'-ACAAAGCGTCTACGCTGCAG-3'; FluB-NS-F485: 5'-GGGACATGAACAACAAAG ATGC-3'; FluB-NS-R988: 5'-TGTCAGCTATTATGGAGCTG-3'。A型 M基因产物长度为 234 bp,B型 Ns基因产物长度为503 bp。用 QIAGEN公司试剂盒,按说明书提取和扩增病毒样本 RNA。通过实时荧光定量 PCR(real-time PCR)法,检测已知 A型和 B型 2个确诊流感病例咽拭子样本 CT值,并在多重 RT-PCR检测中使用。共设 5个反应体系,对应的试剂类型分别为 A型、B型、AB混合型、AB混合型、AB混合型,各体系中对应加入的样本类型分别为 A型、B型、A型、B型、AB混合型。再扩增病毒 RNA及用 1.5%琼脂糖进行凝胶电泳,观察电泳结果。随机抽取的 40份疑似流感样病例的临床咽拭子标本进行多重 RT-PCR检测,并将其检测结果与实时荧光定量 PCR的检测结果相比较。
2 结果 2.1 Real-time PCR结果(图 1)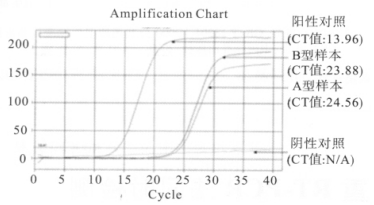 | 图 1 real-time PCR 检测结果 |
已知 A型和 B型2个流感样本,检测 CT值分别为 A型 24.56,B型 23.88,此次检测阳性对照 CT值是 13.96,阴性对照 CT值是 N /A。
2.2 多重 RT-PCR电泳结果(图 2)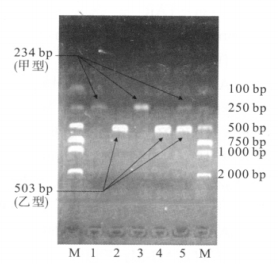 | 注: M: marker; 1: A 型试剂、 A 型样本; 2: B 型试剂、 B 型样本; 3: AB 型试剂、 A 型样本; 4: AB 型试剂、 B 型样本; 5: AB 型试剂、 AB 型样本。 图 2 多重 RT-PCR 电泳结果 |
通过琼脂糖凝胶电泳图片可见,分别在第 1、3、5孔的 234 bp处出现 A型(甲型)流感病毒 M基因目的条带,同时分别在第 2、4、5孔的 503 bp处出现 B型(乙型) Ns基因目的条带。
2.3 验证结果用多重 RT-PCR方法检测40份临床疑似流感患者咽拭子中,检测出流感病毒 A型阳性 8份,阳性率为 20% ,检出流感病毒 B型阳性标本 3份,阳性率为 7.5% ,而用 real-time PCR检测此 40份样本结果同样为流感病毒 A型阳性 8份,B型阳性 3份。
3 讨论目前,已建立的用于流感病毒分型检测的多重 PCR方法已获得美国 FDA认证[3],其关键的实验设计仍是主要针对动物流感病毒分型的检测[4]。之后出现的如微型芯片[5]、流式细胞术[6]和序列检测[7]等方法大多程序复杂,成本昂贵。病毒性呼吸道感染的实验室诊断迫切需要灵敏、特异并能同时检测多种可疑病毒的方法,如多重 RT-PCR,realtime PCR[8],nested-PCR[9]等,这些技术已经越来越多地用于对该类疾病的快速诊断。
本研究采用的多重 PCR方法可通过凝胶电泳直观验证检测结果,无需昂贵的设备,操作简单,快速经济。多重 PCR有较多影响因素,实验中优化混合反应体系中引物浓度[10]、改变退火温度、延伸时间的长短[11, 12]、体系中提供足量的 dNTP[13]等反应条件,可以获得更高敏感性。本研究结果表明,多重 RT-PCR方法与 real-time PCR法的检测结果完全符合,多重 RT-PCR法可以替代普通 RT-PCR检测流感病毒,且可以检测混合感染流感病毒样本。锦州市疾病预防控制中心在检测每份疑似流感病例咽拭子均需要同时用 A型和 B型 2个反应体系检测,优化反应体系后,检测一份样本只用 1份 AB型混合反应体系即可,每年可节省约 50%试剂盒购买经费,同时也大大减少了工作量和工作时间,提高了工作效率。
| [1] | Chan PK.Outbreak of avian influenza A(H5N1)virus infection in Hong Kong in 1997[J].Clin Infect Dis,2002,34(2):S58-S64. |
| [2] | Tran TH,Nguyen TL,Nguyen TD,et al.Avian influenza A(H5N1)in 10 patients in Vietnam[J].N Engl J Med,2004,350(12):1179-1188. |
| [3] | Lee CS,Kang BK,Lee DH,et al.One-step multiplex RT-PCR for detection and subtyping of swine influenza H1,H3,N1,N2 viruses in clinical samples using a dual priming oligonucleotide(DPO)system[J].Virol Methods,2008,151(1):30-34. |
| [4] | Jang JH,Kang KJ,Kim YH,et al.Reevaluation of experimental model of hepatic fibrosis induced by hepatotoxic drugs:an easy,applicable,and reproducible model[J].Transplant Proc,2008,40(8):2700-2703. |
| [5] | Wu XL,Zeng WZ,Jiang MD,et al.Effect of oxymatrine on the TGF beta/smad signaling pathway in rats with CCl42 induced hepatic fibrosis[J].World J Gastroentero,2008,14(13):2100-2105. |
| [6] | 杨颖,蔡玟,黄志彪,等.环磷酰胺致小鼠免疫功能低下模型建立与评价[J].中国公共卫生,2008,24(5):581-583. |
| [7] | Kim HY,Kim JK,Choi JH,et al.Hepatoprotective effect of pinoresinol on carbon tetrachloride-induced hepatic damage in mice[J].J Pharmacol Sc,2010,112(1):105-112. |
| [8] | 罗予,卞广林.脆弱类杆菌荧光定量PCR法检测[J].中国公共卫生,2007,23(1):100-101. |
| [9] | 张杰,王嵬,张玲,等.血痕中乙型肝炎病毒DNA检测[J].中国公共卫生,2010,26(8):983-985. |
| [10] | 许美燕,唐传红,张劲松,等.利用SRAP和ISSR建立快速鉴定灵芝属菌株的SCAR标记[J].菌物学报,2008,27(5):707-717. |
| [11] | 胡毅玲,王声勇,池桂波,等.多重PCR在肿瘤遗传标志分子流行病学研究中的应用[J].中国公共卫生,2001,17(5):412-413. |
| [12] | 黄银花,胡晓湘,徐慰倬,等.影响多重PCR扩增效果的因素[J].遗传,2003,25(1):65-68. |
| [13] | 杨学文,王礼文,缪界平,等.多重PCR在幽门螺杆菌检测及分型中的应用[J].临床检验杂志,2000,18(3):148-150. |
 2012, Vol. 28
2012, Vol. 28
