2. 西安交通大学医学院环境与疾病相关基因教育部重点实验室
高原肺水肿是由高原低压缺氧所诱发的一种严重危及生命的急性高原病,表现为肺动脉高压及毛细血管通透性改变[1, 2, 3]。低氧习服是指人或动物的组织器官经过1 次或多次短暂、非致死性低氧刺激后,组织器官获得对更严重甚至致死性缺血或缺氧较为长久的耐受性[4]。目前认为这是在细胞水平产生的一种对抗缺氧或缺血的内源性保护机制,普遍存在于动物心、肝、肾和脑等多种组织、器官和细胞中。但目前关于肺组织低氧习服产生的机制研究较少[5]。低氧诱导因子1α(hypoxia inducible factor-1α,HIF-1α) 是近年来发现介导哺乳动物细胞适应低氧环境的核转录因子。本研究观察了低氧习服对大鼠肺组织细胞超微结构改变和HIF-1α 表达影响,以探讨低氧习服产生的机制,结果报告如下。
1 材料与方法 1.1 实验动物健康12 周龄雄性SD 大鼠(西安交通大学动物中心) 50 只,体重348 ~ 385 g ,许可证号: SYXK(陕) 2007-003。自由摄食,喂以大鼠标准饲料(西安交通大学动物中心) ,饮用蒸馏水。
1.2 试剂与仪器兔抗大鼠HIF-1α 多克隆抗(美国Santa Cruz 公司体) ,生物素标记羊抗兔IgG(北京中山生物技术有限公司) ,逆转录-聚合酶链反应(RT-PCR) 试剂盒(北京鼎国生物技术责任有限公司) ,透射电镜(荷兰飞利浦公司) ,光学显微镜 (日本Nikon 公司) ,AlphaImager2200 凝胶成像系统(美国Alpha Innoteeh 公司) 。
1.3 实验方法 1.3.1 动物分组及高原低氧大鼠模型建立将大鼠50 只随机分为5 组,每组10 只,分别为高原低氧 1、2、3、30 d 组和对照组(西安地区,海拔5 m) 。高原低氧1 d 组由西安地区途中耗时1 d 带到海拔2 700 m青海格尔木地区,高原低氧2 d 组途中耗时 2 d 带到海拔5 000 m 唐古拉地区,高原低氧3、30 d 组途中耗时3 带到海拔4 500 m 西藏那曲地区,30 d 组在那曲饲养30 d。以动物出现明显呼吸、心跳加快及多动、嘴唇紫绀为高原低氧模型建立成功。腹腔麻醉处死动物,摘取肺脏,将组织迅速放入液氮中保存。
1.3.2 大鼠高原低氧致肺组织细胞结构改变取肺组织用体积分数4%戊二醛固定,按常规制取电镜标本(取材-清洗-固定-脱水-干燥-镀膜) 后,透射电镜观察。余下肺组织用10% 甲醛固定作光镜标本,苏木精-伊红(HE) 染色,光学显微镜观察[6]。
1.3.3 低氧习服大鼠肺组织HIF-1α 蛋白表达采用Western blot 法,取液氮保存肺组织样本,加入含有蛋白酶抑制剂鸡尾酒片的蛋白提取缓冲液(pH = 7.4) ,剪碎、重悬,内切式匀浆机以13 000 r /min 高速匀浆,4 ℃,1 000 g 离心30 min,上清-70 ℃保存。考马斯亮蓝R-250 进行蛋白定量,取200 μg 蛋白进行常规十二烷基硫酸钠-聚丙烯酰胺凝胶电泳,转膜。5%脱脂奶粉(脱脂奶粉1.0g 溶于20 mL 的0.01 mmol /L 磷酸盐缓冲液中) 室温封闭1 h,加羊抗大鼠HIF-1α 多克隆抗体(1∶ 500) 室温孵育过夜; 加辣根过氧化酶标记马抗羊抗体(1∶ 2 000) 室温孵育2 h; 二氨基联苯胺显色5 min。凝胶成像系统分析处理[7, 8]。
1.3.4 高原低氧大鼠肺组织HIF-1α mRNA 表达采用RT-PCR 法,取液氮保存肺组织,Trizol 试剂盒提取组织总RNA,利用依赖于RNA 的DNA 聚合酶(M-MLV) 反转录酶反转录合成cDNA,以cDNA 产物为模板分别进行目的片断PCR 扩增[9]。引物 HIF-1α 上游: AAG TCT AGG GAT GCA GCA C,下游: CAA GAT CAC CAG CAT CTA G,长度175 bp; β-actin 上游: CAT CTC TTG CTC GAA GTC CA,下游: ATC ATG TTT GAG ACC TTC AAC A,长度300 bp。扩增产物经5%琼脂糖凝胶电泳后成像,用凝胶成像系统进行图像分析,以HIF-1α 和β-actin mRNA 产物条带积分吸光度值之比(HIF-1α / β-actin) 反映HIF-1α mRNA 表达量。
1.4 统计分析数据用x±s 表示,采用SPSS15.5 统计软件对数据进行处理,组间均数差异比较采用单因素方差分析,组间两两比较采用两样本t 检验,P < 0.05 为差异有统计学意义。
2 结果 2.1 高原低氧环境对大鼠肺组织结构影响(图 1)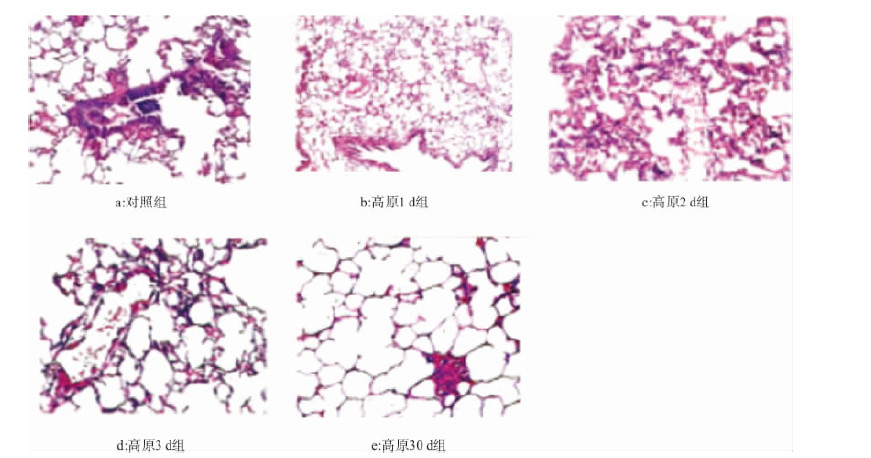 | 图 1 高原低氧环境对大鼠肺组织结构影响( HE 染色,× 100) |
对照组肺结构正常。高原低氧1 d 组大鼠肺脏毛细血管扩张充血; 高原低氧2、3 d 组大鼠肺泡隔增宽,肺间质疏松,毛细血管扩张充血明显,某些区域内可见肺泡腔内有粉红色渗出物; 高原低氧30 d 组大鼠肺泡腔清晰,肺泡隔结构基本正常,部分区域可见肺间质增生及轻度肺气肿改变。
2.2 高原低氧环境对大鼠肺组织超微结构影响 (图 2)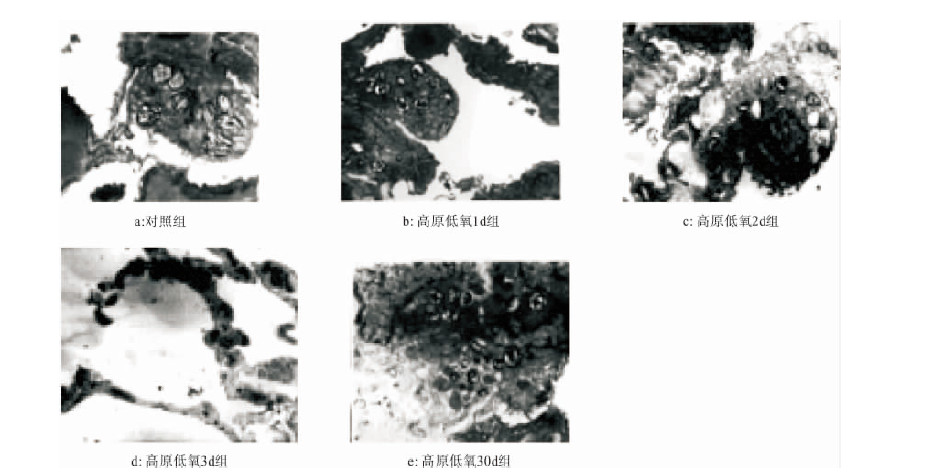 | 图 2 高原低氧环境对大鼠肺组织超微结构影响( 醋酸铀-枸榭酸铅双染色,× 2 500) |
对照组肺组织超微结构正常。高原低氧1 d 组大鼠Ⅱ型肺泡细胞变薄,细胞数量基本正常,嗜锇性板层颗粒略增多; 高原低氧2、3 d 组大鼠Ⅱ型肺泡细胞变薄,有时可见细胞膜损伤、断裂,并形成髓鞘样结构,细胞数量明显减少,细胞内嗜锇性板层颗粒明显减少,排空现象增加; 高原低氧30 d 组大鼠肺脏Ⅱ型肺泡细胞数量明显增多,嗜锇性板层颗粒明显增多,肺间质水肿明显减轻。
2.3 高原缺氧对大鼠肺组织HIF-1α 蛋白及mRNA 表达影响(图 3)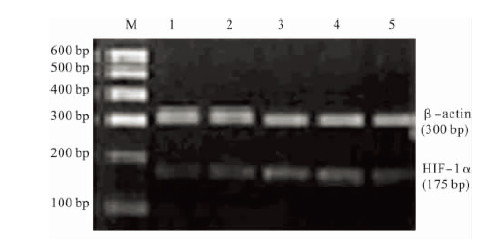 | 注: M: Marker; 1: 对照组; 2 ~ 5 分别为高原低氧1、2、3、30 d 组。 图 3 高原低氧环境对大鼠肺组织HIF-1α mRNA 表达影响 |
Western blot 检测结果显示,各高原缺氧组大鼠肺组织均未见HIF-1α 蛋白表达。 RT-PCR 检测结果显示,高原低氧30 d 组HIF-1α mRNA 积分吸光度值(0.874 ± 0.075) 明显高于对照组(0.225 ± 0.026) (F = 0.028,P < 0.01) 。
3 讨 论本研究结果显示,光镜下急性低氧组出现肺间质充血、肺泡隔增宽等间质性肺水肿表现,亦可见肺泡性肺水肿,透射电镜发现大鼠在海拔5 000 m 高原低氧环境2 d,肺组织超微结构出现肺泡隔明显增宽、毛细血管充血等间质性肺水肿表现,Ⅱ型肺泡细胞数量明显减少,细胞内嗜锇性板层颗粒明显减少,而典型的肺泡性肺水肿则少见。与以往报道的急性缺氧在高原5 000 m 多典型的肺泡性肺水肿不一致[9],高原低氧3 d 组也是间质性肺水肿为主。高原低氧30 d 组大鼠低氧习服后,获得了对抗高原肺水肿能力,主要表现为间质性肺水肿得到改善,肺间质充血减轻,肺泡隔增宽不明显,肺泡Ⅱ型上皮细胞及其细胞内嗜锇性板层颗粒数量增加。本研究结果显示,大鼠肺组织在常氧和缺氧环境下低表达HIF-1α mRNA,但应用Western blot 方法未检测到低氧习服肺组织表达HIF-1α 蛋白。因此,低氧习服后肺组织HIF-1α mRNA 表达提高,有利于减轻大鼠高原低氧性肺水肿。
低氧习服可以提高机体组织器官对低氧耐受性。属于细胞水平产生的内源性保护机制。本研究结果显示,大鼠肺组织随着低氧习服时间延长,HIF-1α mRNA 表达水平逐渐升高,表明HIF-1α 参与低氧习服调控过程,对暴露于急性低压缺氧环境大鼠的肺组织起到保护作用。HIF-1 是引发缺氧耐受的重要蛋白质分子,是哺乳动物不同组织、细胞形成缺氧耐受的共同分子生物学机制。体内与高原低氧习服有关的合成诱导型一氧化氮关键酶的表达也受 HIF-1 调控[10],参与低氧习服过程受HIF-1 调控的下游基因达12 种,在低氧习服中起关键作用的基因目前尚不清楚,需要进一步研究。
| [1] | 李素芝,高钰琪.高原疾病学[M].北京:人民卫生出版社, 2006. |
| [2] | 李福祥,夏前明,李鸿雁,等.低氧习服对模拟高原低氧大鼠肺组织的影响[J].中国呼吸与危重监护杂志,2008,7(3):199-203. |
| [3] | Yi X,Liang Y,Huerta-Sanchez E,et al.Sequencing of 50 human exomes reveals adaptation to high altitude[J].Science,2010,329 (5987):75-78. |
| [4] | 李文华,袁东亚.西藏藏族青年血浆AVP含量的测定与分析[J].中国公共卫生,2008,24(1):84-85. |
| [5] | Engebretsen BJ,Irwin D,Valdez ME,et al.Acute hypobaric hypoxia(5486 m)induces greater pulmonary hif-1 activation in hilltop compared to madison rats[J].High Alt Med Biol,2007,8 (4):312-321. |
| [6] | 李文华,刘晓丽,蔡平.心肌桥壁冠状动脉内皮细胞超微结构观察及其临床意义[J].中国组织工程研究与临床康复, 2010,14(20):3722-3725. |
| [7] | Ostrowski RP,Colohan AR,Zhang JH.Mechanisms of hyperbaric oxygen-induced neuroprotection in a rat model of subarachnoid hemorrhage[J].J Cereb Blood Flow Metabol,2005,25(5):554-571. |
| [8] | Nguyen MV,Pouvreau S,El Hajjaji FZ,et al.Desferrioxamine enhances hypoxic ventilatory response and induces tyrosine hydroxylase gene expression in the rat brainstem in vivo[J].J Neurosci Res,2007,85(5):1119-1125. |
| [9] | 刘忠,李文华.高原低氧环境下大鼠RAAS水平与右心室 ACE2表达变化[J].中国公共卫生,2011,27(3):299-301. |
| [10] | 李文华,刘忠.西藏红景天对高原肺水肿大鼠非组织的影响[J].中国公共卫生,2011,27(8);1004-1006. |
 2012, Vol. 28
2012, Vol. 28
