2. 广东省食品行业协会;
3. 暨南大学医学院;
4. 广东出入境检验检疫局检验检疫技术中心
毒物兴奋效应(hormesis)是指机体低浓度接触某一化学物时产生刺激效应,而高浓度接触时却产生抑制效应的现象〔1〕。亚硝酸钠(NaNO2 )是一种常用的食品添加剂,广泛存在于熏制和腌制食品中。国内外学者对NaNO2 的毒性作用进行了大量研究,但对于低剂量长期接触是否具有致癌危险性尚存很大分歧〔2, 3〕。人们在日常生活中多是长时间、低剂量接触环境化学物,这种接触方式可能会产生与安全性评价所设计的毒物剂量范围完全不同的生物学效应〔4〕,也很可能存在hormesis。本研究采用小鼠结缔组织成纤维细胞(L929 细胞)作为受试生物体,观察不同浓度NaNO2 对L929细胞增殖影响,探讨低剂量NaNO2 能否诱导L929细胞增殖的 Hormesis及其毒理学意义。
1 材料与方法 1.1 主要试剂小鼠结缔组织成纤维细胞(L929,中山大学药学院动物中心细胞库);RPMI 1640培养基(美国Gibco公司);新生牛血清(上海依科赛生物制品有限公司);胰蛋白酶 (美国Difco公司);蛋白酶K (德国Merck公司);溴化四氮唑蓝(MTT,美国Sigma公司);二甲基亚砜(dimethyl sulfoxide,DMSO,天津大茂公司);荧光染料Hoechst No.33258(美国 Sigma公司);亚硝酸钠(天津福晨化学试剂厂)。
1.2 方法 1.2.1 实验方案实验分2个阶段进行:(1)不同剂量 NaNO2 处理L929细胞,采用MTT还原法检测不同染毒时间 (24、48、72 h) L929细胞的增殖情况,确定hormesis表现最明显的处理时间及剂量范围(hormetic zone)。(2)不同剂量 NaNO2 处理L929细胞的遗传损伤效应观察,参照MTT试验结果设置染毒剂量,选取位于hormetic zone下限、中限及以上的5个剂量作为处理组,以完全培养液作为阴性对照,进行 48 h贴壁染毒,隔24 h更换新鲜配制的含不同剂量NaNO2 的培养液,并采用单细胞凝胶电泳技术(single cell gel electrophoresis,SCGE)及KCl-十二烷基磺酸钠沉淀法(K-SDS)法检测DNA的损伤及DNA-蛋白质交联作用(DNA-protein crosslink,DPC),探讨NaNO2 诱导L929细胞增殖的hormesis 与DNA损伤作用关系。
1.2.2 细胞培养将L929细胞置于37℃,5% CO2 饱和湿度的CO2 细胞培养箱中培养,培养液按10%新生牛血清和 90% RPMI1640母液比例混合,按体积比1‰加入双抗液(含青霉素和链霉素各10万单位/mL)。
1.2.3 MTT法检测细胞存活率取对数生长期L929细胞,用0.25%胰蛋白酶消化后制成细胞悬液,接种于96孔培养板,细胞密度为6 × 104个/mL。于37℃培养24 h后,用 NaNO2 染毒,使终浓度达到3.07 × 10-4、1.54 × 10-3、7.68 ×10-3、0.0384、0.19、0.96、4.8、24、120、600、3000 mg/L,以完全培养液作为阴性对照,每个剂量设6个平行样,分别染毒24、48 和72 h (每隔24 h更换培养液)。染毒结束前4 h每孔加入浓度为5 mg/mL的MTT液10 μL,培养4 h,倾去培养液后每孔加入150 μL DMSO,充分振荡,在酶标仪570 nm波长处测定吸光度(A)值,并计算细胞相对存活率。实验重复3次。
1.2.4 SCGE法检测DNA损伤分别用0.02、0.5、2、20、 1500 mg/L浓度的NaNO2 染毒L929细胞48 h,以完全培养液作为阴性对照。实验按Kaya等〔5〕的方法稍加改进。先用 0.8%普通琼脂糖均匀涂布于磨砂玻片上,待干燥后制作底胶,再铺上细胞悬液与0.8%低熔点琼脂糖混合液,平行制备 2份。裂解,电泳20 min (25 V,300 mA),中和,染色。脱色后采用G激发光观察细胞,并采用SCGE图像分析系统处理图片。每次实验分析200个细胞,计算尾长(μm)、尾DNA% 及Olive尾矩等指标。实验重复3次。
1.2.5 K-SDS法检测DNA-蛋白质交联作用按照彭光银等〔6〕的试验方法,回归方程为y=8.821x+2942.036,R2= 0.99。根据标准曲线定量计算交联DNA和自由DNA,计算 DPC系数。
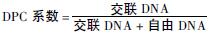
数据均采用x±s 表示,应用SPSS 13.0软件对实验数据进行单因素方差分析及两两比较SNK检验,检验水准α=0.05。
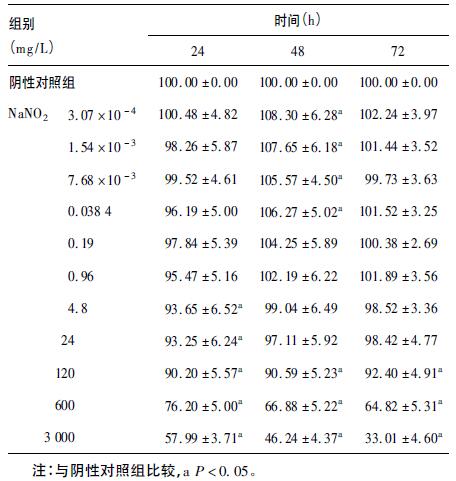
2 结 果 2.1 NaNO2 对L929细胞相对存活率影响(表 1)| 表 1 不同NaNO2 染毒剂量和时间对L929 细胞 相对存活率影响( %,x±s,n = 24) |
染毒24 h,> 4.8 mg/L染毒组细胞相对存活率随染毒剂量增加逐渐下降(F=95.779,P < 0.05)。染毒48 h,< 0.0384 mg/L剂量范围内,各染毒组与对照组比较,细胞相对存活率均有所增加 (F=110.739,P < 0.05)。NaNO2 染毒48 h可诱导L929细胞增殖的hormesis,其hormetic zone约为0~0.0384 mg/L。 染毒72 h后,> 120mg/L剂量组细胞存活率急剧下降(F= 445.438,P < 0.05)。
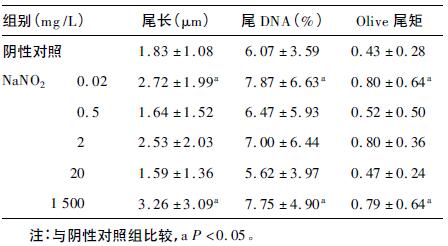
2.2 NaNO2 诱导L929细胞遗传损伤 2.2.1 NaNO2 对L929细胞DNA损伤(表 2)| 表 2 不同剂量NaNO2 对L929 细胞DNA 损伤( x±s,n = 200) |
与阴性对照组比较,0.02、1500 mg/L剂量组的拖尾细胞较多,尾长 (μm)、尾DNA%、Olive尾矩等指标明显改变,差异均有统计学意义(F=19.54、30.00、13.66,P < 0.05)。其他剂量组的细胞拖尾程度相对较轻,无剂量-效应关系。
2.2.2 NaNO2 诱导L929细胞内DNA-蛋白质交联2、20、 1500 mg/L剂量组DPC系数分别为(5.57 ± 0.40)、(7.20 ± 0.38)及(7.93 ± 0.37),与对照组(3.60 ± 0.21)比较,差异均有统计学意义(F=62.286,P < 0.05),表明细胞发生DNA-蛋白质交联作用,并呈现剂量-效应关系。0.02 mg/L及 0.5 mg/L剂量组的DPC系数分别为(4.83 ± 0.18)、(5.03 ± 0.15),与阴性对照组比较,差异无统计学意义(P > 0.05)。
3 讨 论本研究中,以NaNO2 处理L929细胞48h,在0~ 0.0384mg/L范围内细胞相对存活率增大,而在高剂量时细胞增殖活性受到抑制,剂量-反应关系表现出典型的hormesis双相曲线。但有关细胞增殖的hormesis是否属于有利反应,目前尚无定论〔7〕。本研究结果提示,NaNO2 诱导L929细胞增殖的hormesis并不是完全有益的效应。SCGE试验及K-SDS试验分别反映DNA受到的断裂性损伤和交联性损伤。 0.02 mg/L剂量组的各SCGE指标值均大于对照组(P < 0.05),表明DNA发生了断裂损伤。该剂量恰好位于细胞增殖的hormetic zone剂量范围内,提示能诱导L929细胞产生 hormesis的NaNO2 剂量会损伤遗传物质。而较高剂量(2、20、 1500 mg/L)可诱发L929细胞的DNA-蛋白质交联作用,使DNA 受到交联性损伤,并呈剂量-效应关系。低剂量诱发断裂损伤、高剂量诱发交联损伤的现象,在其他文献中也有报道〔8, 9〕。
正常细胞中总会存在微量的DNA-蛋白质交联产物,但是DPC过度增加则是一种病理现象。而且DPC是DNA分子的一种严重遗传损伤,较难修复〔10〕。而DNA断裂是常见的DNA损伤形式之一,相对来说更易于被修复。细胞受到低剂量刺激时,产生较易修复的断裂损伤,保证细胞得以存活并产生更多后代,对抗不良环境。当高剂量刺激超出细胞对毒性的耐受范围,增殖活性便受到抑制。这符合过度补偿理论(hormesis机制假设之一)的观点〔11〕,其具体机制还有待进一步研究。
| 〔1〕 | Calabrese EJ,Baldwin LA.Toxicology rethinks its central belief [J].Nature,2003,421:691-692. |
| 〔2〕 | NIH.Toxicology and carcinogenesis studies of sodium nitrite(CASNO.7632-00-0)in F344/N rats and B6C3F1 mice(drinking water studies)[R].NC:National Toxicology Program,Research Triangle Park,2001. |
| 〔3〕 | 王廷兆.警惕食品添加剂为癌“搭桥”[J].抗癌,2004,3:25-26. |
| 〔4〕 | 王东红,彭安,王子健.有毒物质低剂量刺激作用的研究进展[J].安全与环境学报,2004,4(1):18-21. |
| 〔5〕 | Kaya E,NurdanÖ,Semra S.Monitoring of buccal epithelial cells by alkaline comet assay(single cell gel electrophoresis technique) in cytogenetic evaluation of chlorhexdine[J].Clin Ora1 Invest, 2002,6(3):150-154. |
| 〔6〕 | 彭光银,杨旭,赵玮.液态甲醛致小鼠肝和睾丸DPC研究[J]. 医学研究杂志,2006,35(11):9-12. |
| 〔7〕 | 陶功学.低剂量兴奋效应作用机制的研究进展[N].中山大学研究生学刊:自然科学、医学版,2007,28(1):16-21. |
| 〔8〕 | 贺庆芝,许雪梅,孙杰.甲醛对小鼠源性巨噬细胞DNA损伤作用[J].中国公共卫生,2009,25(12):1517-1518. |
| 〔9〕 | 刘延君,林哲绚,李慧.彗星电泳法和K-SDS法检测甲醛和H2O2对人脐静脉内皮细胞DNA的损伤[J].癌变畸变突变, 2005,17(1):8-11. |
| 〔10〕 | 颜进,张本延.DNA-蛋白质交联在甲醛遗传毒性研究中的进展 [J].武汉科技大学学报:自然科学版,2005,28(4):415-419. |
| 〔11〕 | Calabrese EJ,Baldwin LA.Defining hormesis[J].Human and Experimental Toxicology,2002,21:91-97. |
 2012, Vol. 28
2012, Vol. 28