2. 辽宁省疾病预防控制中心;
3. 中国医科大学口腔医学院中心实验室
慢性牙周炎是牙周支持组织的慢性破坏性炎症,是世界范围内常见病和多发病之一,是中国成年人失牙的主要原因〔1〕。菌斑细菌是牙周炎的始动因子,在牙周微生物中,目前认为10余种微生物与牙周炎的发生发展密切相关,其中牙龈卟啉单胞菌(Porphyromonas gingivalis,P.gingivalis)被认为是最重要的牙周可疑致病菌之一,是各型牙周炎的重要病原因子〔2〕。P.gingivalis具有一系列逃避宿主防御机制及破坏宿主组织的毒性因子,如菌毛、牙龈素、红细胞凝集素、多糖荚膜,脂多糖、外膜膜泡和多种蛋白酶等。研究表明毒力调节基因A (virulence modulating gene A,vim A)在P.gingivalis牙龈素的成熟,菌毛形成,脂多糖合成中起重要调控作用〔3〕。本研究通过建立实验性大鼠牙周炎模型,检测不同时段大鼠龈下菌斑中P.gingivalis、vim A基因相对含量,探讨在牙周炎发展过程中P.gingivalis致病基因vim A作用。
1 材料与方法 1.1 主要试剂与仪器P.gingivalis W 83(美国佛罗里达大学牙科学院口腔微生物研究所Dr.Lamont RJ教授惠赠)。 9700型PCR扩增仪(美国ABI公司)。GDS 8000型自动凝胶成像分析仪(美国UVP公司)。所有引物均由大连宝生物工程有限公司合成。
1.2 实验动物SPF级雄性SD大鼠(中国医科大学实验动物部)23只,6 周龄,体重250~300 g,许可证号:SCXK (辽) 2008-0005。所有大鼠在SPF级屏障系统内饲养,喂饲标准鼠粮,自由饮水。
1.3 指标与方法 1.3.1 实验性大鼠牙周炎模型建立剥离大鼠双上颌第一磨牙颊、腭侧牙龈1 mm,使用直径0.2 mm正畸结扎钢丝结扎于牙颈部,以管饲法接种P.gingivalis W 83细菌(浓度为 1.0 × 109 CFΜ/mL)1.0~1.5 mL混悬菌液,隔天接种1次,连续接种5次,同时饮10%葡萄糖水,建立稳定大鼠4周、8 周实验性牙周炎模型。
1.3.2 龈下菌斑样本采集从第1次接种细菌开始计算时间,分别于接种后4周和8周,使用无菌牙签取大鼠双侧上颌第一磨牙龈下菌斑,置于0.5 mL磷酸盐缓冲液(phosphate balanced solution,PBS)中,-80℃保存。对照组大鼠:同时合笼饲养,不结扎,不剥离牙龈,接种不含细菌的细菌培养液,饮普通自来水。P.gingivalis W 83标准株作为阳性对照。
1.3.3 PCR扩增(1)龈下菌斑DNA提取:采用常规酚- 氯仿法提取龈下菌斑细菌DNA。(2)引物序列:细菌通用引物:上游5'-AACTGGAGGAAGGTGGGGA-3',下游5'-AGGAGGTGATCCAACCGCA- 3',扩增片段长度371 bp〔4〕; P.gingivalis 16 S rRNA:上游5'-AGGCAGCTTGCCATACTGCG- 3',下游5'-ACTGTTAGCAACTACCGATGT-3',长度 197 bp〔5〕;vim A:上游5'-CACCATCGTCAGAGAGCGTA-3',下游5'-GTACGTCTCACTTCGGCACC-3',长度927 bp〔6〕。 (3) PCR反应体系:Premix Taq 12.5 μL,上下游引物(0.01mmol/L)各1 μL,DNA模板2 μL,三蒸水补足至总积25 μL。(4) PCR反应条件:94℃预变性5 min,94℃变性45 s,55℃(细菌通用引物50℃、P.gingivalis 16S rRNA 58℃)退火45 s,72℃延伸60 s,35个循环,最后72℃延伸5 min。以标准株P.gingivalis W 83 DNA作为阳性对照,等体积三蒸水作为空白对照。
1.3.4 PCR扩增产物检测取扩增PCR产物5 μL,2%琼脂糖凝胶电泳,自动凝胶成像分析仪拍照。应用电泳凝胶成像分析软件(Fluorchem V 2.0)分析各电泳条带平均灰度值 (AVG)。P.gingivalis 16 S rRNA与细菌通用引物PCR产物的AVG比值为P.gingivalis相对含量,vim A与P.gingivalis 16S rRNA引物PCR产物的AVG比值为该vim A相对含量。
1.4 统计分析计量数据用x±s表示,采用SPSS 11.0软件进行分析,P < 0.05为差异有统计学意义。
2 结 果 2.1 大鼠实验性牙周炎模型建立肉眼观察模型组大鼠牙龈炎症情况,结果显示双侧上颌第一磨牙牙颈部牙龈无法与牙面贴合,局部食物残屑堆积。4周和8周组大鼠均出现牙龈炎症表现,表现为牙龈红、肿,牙龈探诊易出血,可探及较深的牙周袋,骨破坏明确。
2.2 PCR产物电泳结果(图 1)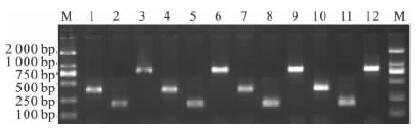
|
注:M:DL2000 DNA Marker;1~3、4~6、7~9、10~12泳道分别为对照 组、大鼠牙周炎4周组、8周组、P.gingivalis W 83阳性对照组;各组电泳 条带依次为细菌通用引物、P.gingivalis特异引物、vim A基因扩增产物。 图 1 PCR 产物电泳图谱 |
PCR扩增电泳结果显示大鼠龈下菌斑中细菌通用引物扩增产物无明显变化;P.gingivalis 特异引物扩增产物随时间延长增加;与对照组比较,牙周炎4、8周组大鼠牙周炎模型中vim A引物扩增产物明显升高。
2.3 各组大鼠龈下菌斑P.gingivalis和vim A相对含量比较 (表 1)| 表 1 各组大鼠龈下菌斑P.gingivalis 和vim A 相对含量(x±s) |
牙周炎4周和8周组P.gingivalis相对含量明显高于对照组(F=106.57,P < 0.01)。牙周炎8周大鼠龈下菌斑 P.gingivalis相对含量明显高于4周组,结果提示P.gingivalis 相对含量随牙周炎病程延长明显升高。牙周炎4周和8周组 vim A相对含量明显高于对照组(F=19.12,P < 0.05),vim A相对含量在牙周炎4周与8周时无明显差异。
3 讨 论本研究结果显示牙周炎组大鼠在接种细菌后4周,牙龈组织炎症明显,有真性牙周袋形成,明显牙槽骨吸收,获得比较稳定的大鼠牙周炎模型。P.gingivalis是慢性牙周炎患者牙周袋中最常分离出的细菌之一,与牙龈出血指数和牙周袋深度密切相关。研究表明慢性牙周炎患者牙周袋中存在较高浓度的P.gingivalis,其致病性与P.gingivalis的定植数量有关〔7〕。本研究结果表明,大鼠病变部位P.gingivalis相对含量明显高于对照组,同时在牙周炎8周和4周大鼠病变部位P. gingivalis比例也存在差异,提示P.gingivalis在大鼠牙周炎发生过程中具有重要作用。
近年来许多学者对P.gingivalis毒力基因结构、作用和调控机制进行了深入探讨。研究表明牙龈卟啉单胞菌vim A基因可以调节牙龈素分泌、加工、活化和成熟〔8, 9〕;vim A在P. gingivalis囊泡和菌毛的形成发挥调控作用,提示可能参与细菌的排序、运输功能〔10〕。本研究结果显示牙周炎组vim A相对含量高于对照组,表明vim A基因参与对牙周组织的破坏作用,但8周组和4周组大鼠牙周炎模型中vim A相对含量未见明显差异,提示随着牙周炎病情加重,局部微环境的改变或自身免疫系统作用,抑制vim A基因表达,从而使其处于一个相对稳定状态。Vim A基因在动物牙周炎模型中的变化机制值得进一步研究。
| 〔1〕 | 姜红,姜广水.大学生口腔健康认知及行为影响因素分析.[J] 中国公共卫生,2011,27(9):1181-1183. |
| 〔2〕 | 张玉杰,郭杨,张瑾,等.多重PCR技术用于检测牙龈卟啉单胞菌致病岛rag基因的研究[J].中国实用口腔科杂志,2011,4 (9):546-549. |
| 〔3〕 | Lamont RJ.Controlling Porphyromonas gingivalis requires Vim [J].Microbiology,2010,156(7):1907-1908. |
| 〔4〕 | 方怡,黄文杰,刘志红,等.反相杂交技术在常见社区获得性肺炎致病菌基因诊断研究中的应用[J].广东医学,2003,24(6): 591-592. |
| 〔5〕 | 赵蕾,吴亚菲,杨禾,等.不同Vim A基因型牙龈卟啉单胞菌在牙周健康人群中的分布[J].口腔医学,2007,27(11):565-568. |
| 〔6〕 | Vanterpool E,Roy F,Zhan W,et al.Vim A is part of the maturation pathway for the major gingipains of Porphyromonas gingivalis W 83[J].Microbiology,2006,152(11):3383-3389. |
| 〔7〕 | 王者玲,岗本公彰,杨圣辉,等.PCR直接检测龈下菌斑主要可疑牙周致病菌[J].中国微生态学杂志,2003,15(2):115-116. |
| 〔8〕 | Abaibou H,Chen Z,Olango GJ,et al.vim A gene downstream of recA is involved in virulence modulation in Porphyromonas gingivalis W 83[J].Infect Immun,2001,69(1):325-335. |
| 〔9〕 | Vanterpool E,Roy F,Fletcher HM.The vim E gene downstream of vim A is independently expressed and is involved in modulating proteolytic activity in Porphyromonas gingivalis W 83[J]. Infect Immun,2004,72(10):5555-5564. |
| 〔10〕 | Osbourne DO,Aruni W,Roy F,et al.Role of vim A in cell surface biogenesis in Porphyromonas gingivalis[J].Microbiology, 2010,156(7):2180-2193. |
 2012, Vol. 28
2012, Vol. 28



