2. 山东省公安厅刑侦局
副溶血弧菌(Vibrio parahaemolyticus,VP)是沿海地区常见的革兰氏阴性杆菌。食用未煮熟或者生食海鲜产品容易感染副溶血弧菌而引起发烧、呕吐、腹泻、恶心等食物中毒症状〔1〕。国家食源性疾病监测网数据表明,近年来中国副溶血性弧菌中毒呈逐年上升趋势,抽样检测发现中国沿海地区海、水产品副溶血弧菌检出率高达30.29%〔2〕,且全球副溶血弧菌感染事件屡见不鲜。为了解副溶血弧菌的血清型别和分子型别特征,本研究对沈阳地区24株副溶血弧菌进行毒力基因检测和脉冲场凝胶电泳技术(pulsed-field gel electrophoresis,PFGE)分析。结果报告如下。
1 材料与方法 1.1 菌株来源军事医学科学院疾病预防控制所传染病控制中心实验室对2010年腹泻菌进行监测,选择7-8月从沈阳某医院就诊的腹泻病人便标本中分离出副溶血弧菌共24株。分子量参考标准菌株为PulseNet中使用的沙门菌H9812〔3〕。
1.2 主要试剂与仪器Api 20E生化板条(法国生物梅里埃公司),血清(日本生研公司),营养琼脂、克氏双糖铁琼脂(北京陆桥公司),20 mg/mL蛋白酶K (德国Merck公司),限制性内切酶Xba I、Not I和Marker DL2000(大连宝生物公司),PFGE琼脂糖(美国SeaKem Gold公司)、细胞基因组提取试剂盒(北京天根公司)。脉冲场电泳仪为CHEF MAPPERTM system及其配套设备、Bio-rad Quantity One凝胶成像系统(美国Biorad公司),台式高速离心机(德国Eppdoff公司),浊度仪(意大利BioMerieux公司),BioNumerics 6.0软件(比利时Applied Maths公司)。
1.3 方法 1.3.1 菌株生化鉴定应用Api 20E生化板条对24株副溶血弧菌进行鉴定,应用Apiweb软件读取结果。挑取单个菌落涂抹于氧化酶试纸上,观测结果。
1.3.2 血清分型副溶血弧菌血清型分O抗原和K抗原。O抗原血清使用方法:用3%氯化钠溶液制成10 mg/mL菌悬液,121℃ 1 h灭活。离心去上清,用同体积含有5%甘油和3%氯化钠溶液重悬菌体。在洁净玻片上滴1滴菌悬液并滴加同体积血清,混匀,1 min内呈明显凝集者为阳性,否则为阴性。K型血清使用方法:挑取单个菌落混匀于1滴血清中,1 min内呈明显凝集者为阳性,否则为阴性。同时做盐水对照。
1.3.3 菌株毒力基因检测参照基因组提取试剂盒说明提取基因组作模板,应用PCR技术检测毒力基因:耐热溶血素基因(thermostable direct hemolysin,tdh)、耐热溶血素相关溶血素基因(thermostable direct hemolysin-related hemolysin,trh)和不耐热溶血素基因(thermolabile hemolysin,tl)。其中tdh基因正向引物序列5'-GTAAAGGTCTCTGACTTTTGGAC-3',反向引物序列5'-TGGAATAGAACCTTCATCTTCACC-3'产物长度为269 bp;trh基因正向引物序列5'-TTGGCTTCGATATTTTCAGTATCT-3',反向引物序列5'-CATAACAAACATATGCCCATTTCCG-3',产物长度为450 bp;tl基因正向引物序列5'-AAAGCGGATTATGCAGAAGCACTG-3',反向引物序列5'-GCTACTTTCTAGCATTTTCTCTGC-3',产物长度为500 bp。50 μL反应体系,反应条件为94℃ 5 min预变性,30个循环94℃ 30 s、56℃ 45 s、72℃ 45 s,最后72℃延伸5 min。
1.3.4 PFGE分析参考文献〔4〕操作如下:(1)制备胶块:刮取适量细菌均匀悬浮于细胞悬浊液(100 mmol/L Tris-HCl:100 mmol/L乙二胺四乙酸二钠盐,pH 8.0)中,用浊度仪检测并调整OD值至3.7;取400 μL细菌悬浊液于37℃水浴中孵育5 min后加入20 μL蛋白酶K (储存液浓度为20 mg/mL)混匀;每管加入400 μL的1%脉冲场凝胶电泳琼脂糖:1%十二烷基硫酸钠,混匀,加入模具室温下凝固10~15 min。(2)裂解细胞:将胶块置于细胞裂解液中裂解。(3)洗胶块:倒掉细胞裂解液,加入纯水洗2遍。(4) DNA酶切:用刀片切下2 mm宽胶块放入1.5 mL离心管中,在缓冲体系中缓冲15 min;副溶血弧菌用Not I酶、H9812用Xba I酶酶切,酶用量均为20 U,酶切温度为37℃,3 h。(5)加样及电泳:将酶切胶块贴在梳子齿上,用l%脉冲场凝胶电泳琼脂糖溶胶,用脉冲场电泳仪进行电泳,电泳程序:电压6.0 V/cm,脉冲转换时间10~35 s,线性条件,转换角度120°,电泳时间20 h。(6)图像分析:电泳结束后,将胶块放入万分之一浓度的溴化乙锭溶液染色30 min,纯水洗涤,在凝胶成像系统紫外灯下摄影得到电泳图谱。
2 结果 2.1 菌株生化鉴定及血清分型经Api 20E板条鉴定24株菌均为副溶血弧菌,均分解葡萄糖不分解乳糖,氧化酶实验为阳性。血清鉴定结果:其中O3:K6型17株,O4:K8型2株,O3:K29型2株,O3:K5型、O3:K9型、O4:K9型各1株。
2.2 毒力基因分析(图 1、2)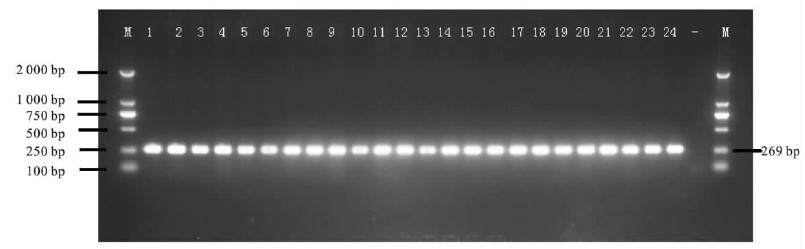 | 注:M:Marker DL2000;1-24:24株副溶血弧菌PCR扩增结果;-:为阴性对照。 图 1 24 株副溶血弧菌tdh 毒力基因PCR 电泳图 |
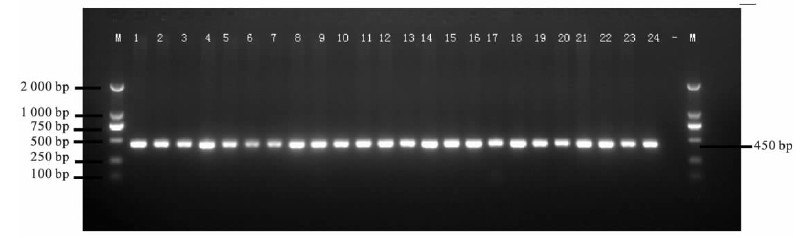 | 注:M:Marker DL2000;1-24:24株副溶血弧菌PCR扩增结果;-:为阴性对照。 图 2 24 株副溶血弧菌tl 毒力基因PCR 电泳图 |
PCR检测结果显示,24株副溶血弧菌均携带tdh和tl毒力基因,但均未检出trh基因。
2.3 PFGE分析(图 3)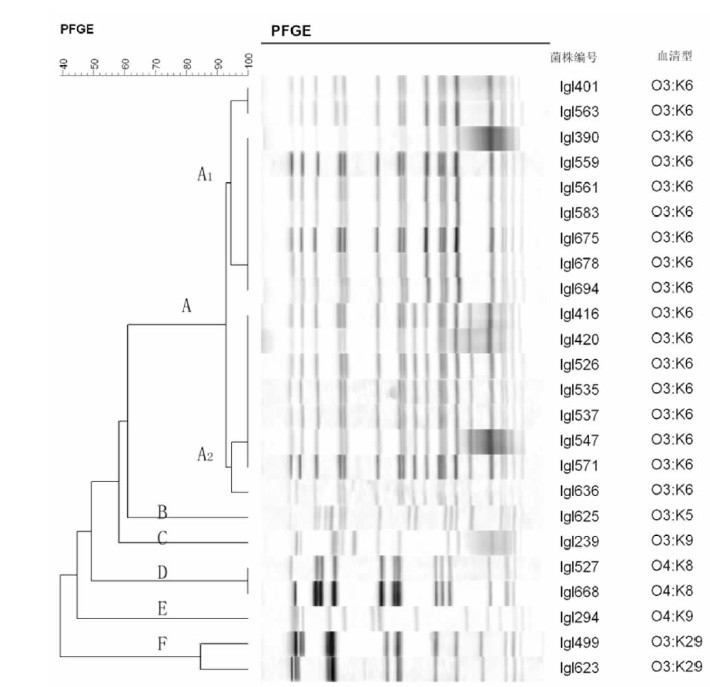 | 图 3 24 株副溶血弧菌PFGE 聚类分析图 |
经限制性内切酶Not I对副溶血弧菌染色体DNA进行酶切后,产生17~25条DNA片断,范围为20.5~1 135 kb。经酶切后24株副溶血弧菌按相似度80%分为A~F六大聚类,共10种PFGE图谱。由图 3可知聚类A共17株菌,占70.8%,为主要PFGE聚类。聚类A中所有菌株血清型均为O3:K6型,按相似度94%可分A1和A2 2个分支。聚类A1分2种PFGE图谱,401和563图谱相同,其余7株图谱相同。2种图谱仅有1条带差异,表明菌株在同源性上密切相关。聚类D 2株菌带型相同,均为O4:K8血清型。聚类F 2株菌均为血清型O3:K29,分为2种图谱型,相似度高于85%。聚类B、C和F含有不同血清型菌株,其带型彼此差异较大。
3 讨论副溶血弧菌自1950年在日本发现之后,陆续在各国食物中毒案例中出现并被认为是海产品中导致人腹泻的主要致病菌,成为中国沿海地区食物中毒和感染性腹泻的重要病原体。副溶血弧菌种类具有多样性,但是只有相对较少的血清型能使人感染,其中O3:K6是主要流行型别,且具有较强的传播能力和致病性〔5〕。中国副溶血弧菌存在多个血清型菌株的流行,其中O3:K6型为引起中国副溶血弧菌食源性疾病的优势流行血清型〔6, 7〕。沈阳地区24株副溶血弧菌被分为6个血清型,其中O3:K6型占70.8%,为主要血清型。副溶血弧菌对人和动物均有较强的毒力,其中tdh和trh基因可作为有毒株和无毒株的分子标识。本研究结果显示,沈阳地区副溶血弧菌均含有tdh和tl基因,提示均为有毒株。基于标准化PFGE技术,本研究对沈阳地区24株副溶血弧菌进行分子分型,结果显示这些菌株可分为10种图谱型,17株O3:K6被分为4种型别,显示了较之血清分型更高的分辨力。此外,结果还显示相同血清型菌株具有相同图谱型或聚集在一起,提示它们之间具有遗传相关性。17株O3:K6虽然被分为4种型别,但具有优势型别,且型别之间仅相差1~3条带,表明17株O3:K6在流行病学上密切相关,提示可能在沈阳地区存在副溶血弧菌腹泻病的局部暴发或流行。
本研究通过对副溶血弧菌的血清型、毒力和基因型别进行监测分析,为建立副溶血弧菌分子分型监测数据库奠定了良好基础,可为副溶血弧菌主动监测、暴发调查和传染源追踪提供技术和数据支持。
| 〔1〕 | Yang ZQ,Jiao XA,Zhou XH,et al.Isolation and molecular characterization of Vibrio parahaemolyticus from fresh,low-temperature preserved,dried,and salted seafood products in two coastal areas of eastern China[J].International Journal of Food Microbiology,2008,125:279-285. |
| 〔2〕 | 赖晓华,肖新才,王鸣.珠江河口水体及海、水产品致病性弧菌检测.[J].中国公共卫生,2010,26(4):448-449. |
| 〔3〕 | Hunter SB,Vauterin P,Lambert-Fair MA,et al.Establishment of auniversal size standard strain for use with the PulseNet standardizedpulsed-field gel electrophoresis protocols:converting the national databases to the newsize standard[J].Journal of Microbiology,2005,43:1045-1050. |
| 〔4〕 | Parsons MB,Cooper KL,Kubota KA,et al.PulseNet USA standardized pulsed-field gel electrophoresis protocol for subtyping of Vibrioparahaemolyticus[J].Foodborne Pathogens and Disease,2007,4(3):285-292. |
| 〔5〕 | Ansaruzzaman M,Chowdhury A,Bhuiyan NA,et al.Characteristicsof a pandemic clone of O3:K6 and O4:K68 Vibrio parahaemolyticusisolated in Beira,Mozambique[J].Journal of Medical Microbiology,2008,10(57):1502-1507. |
| 〔6〕 | Chao GX,Wang F,Zhou X,et al.Origin of Vibrio parahaemolyticusO3:K6 pandemic clone[J].International Journal of Food Microbiol-ogy,2011,2(145):459-463. |
| 〔7〕 | Yu Y,Hu WZ,Wu BB,et al.Vibrio parahaemolyticus isolates fromsoutheastern Chinese coast are genetically diverse with circulation ofclonal complex 3 strains since 2002[J].Foodborne Pathogens andDisease,2011,8(11):1169-1176. |
 2012, Vol. 28
2012, Vol. 28


