2. 广西医科大学公共卫生学院;
3. 南宁市第四人民医院
反向点杂交膜芯片,其原理是将特异性探针先固定在固相载体膜上,在液体环境中与单链 PCR产物的靶序列特异结合,再经过酶显色而完成检测。在前期研究中本课题组曾采用商品化的结核杆菌耐药基因膜片检测试剂盒检测结核杆菌耐药性,但杂交结果与药敏结果比较后,发现试剂盒在检测耐药种类方面与药敏结果有较大差异〔1, 2〕。因此,本研究根据结核杆菌标准株 H37Rv全基因组序列中的 katG、inhA、ahpCpromoter,rpoB、rpsL、rrs、embB、pncA、gyrA等 9个耐药基因序列,应用 Oligo 6. 0软件重新设计 12对下游引物 5'端标记生物的特异性引物、54条寡核苷酸探针,重新构建结核耐药基因检测的反向斑点杂交膜芯片,以进一步提高结核杆菌多耐药基因膜芯片检测的灵敏度和特异度。
1 材料与方法 1.1 材料52株结核杆菌临床分离株样本来自南宁市第四人民医院。主要试剂有 PCR试剂 ( Tap酶、10 × Buffer,三磷脱氧核苷 dNTP,日本 TaKaRa公司 ) ;尼龙膜 (带正电荷,15×20 cm,0. 45 μm,美国 PALL公司 ) ;四甲基联苯胺 ( TMB)、POD母液 (深圳亚能生物技术有限公司 )。主要仪器有 PCR 仪(美国 ABI公司 ) ;凝胶成像分析系统 (美国 BIO-RAD公司) ;杂交炉 (美国 Thermo公司 )。
1.2 培养分离菌株标本处理及DNA提取参见文献〔2〕。
1.3 引物设计与合成根据结核杆菌标准株 H37Rv的katG、inhA、ahpC promoter,rpoB、rpsL、rrs、embB、pncA、gyrA基因序列,应用 Oligo 6. 0软件分别设计 12对特异性寡核苷酸引物,以上引物均由上海生工生物工程公司合成并纯化,条下游引物 5'端生物素标记。引物序列已申请专利200910114023. 4。
1.4 单基因 PCR的优化单基因PCR反应体系 :模板 DNA 1 μL,上、下游引物各 0. 5 μL( 10 pmol /μL),2.5 mmol/L dNTP1 μL,Taq酶 0. 2 μL( 5 U/μL),10 × Buffer 2. 5 μL,其余用去离子水补足,总体积 25 μL。程序 : 95 ℃变性 5 min,94 ℃变性 50 s、58 ℃退火 40 s、72 ℃延伸 50 s,共进行 35个循环,最后 72 ℃延伸 10 min。对影响 PCR反应的条件如退火温度、引物浓度等进一步优化,将退火温度梯度设置为 45. 8、50. 5、54、61. 4、66 ℃,其他反应条件同上,确定最佳退火温度;引物以 10 pmol /μL,在反应体系中分别加入 0. 3、0. 5、0. 8、1. 0、P2 μL,退火温度以上述确定的为准,其他反应条件不变、确定最佳引物浓度。
1.5 多重 PCR优化 1.5.1 多重 PCR扩增12对引物分为 4个反应管,每管有3对引物,多重 CPR反应体系 :模板 DNA 4 μL,2. 5mmol/LdNTP 1 μL,Taq酶 0. 5 μL( 5 U/μL),10 × Buffer 6 μL,上、下游引物 ( 10 pmol /μL)加入量以单基因 PCR最佳引物浓度为准,其余用去离子水补足,总体积 50 μL。程序同上。PCR产物在 2%琼脂糖凝胶上电泳。
1.5.2 多重 PCR优化设置退火温度为 50、56、58、60、62 ℃,其他反应条件同 1. 5. 1,确定最佳退火温度。每对引物先以单基因 PCR确定的最佳引物浓度为准加入,再根据产物量大小来平衡引物的加入量,产物量较多的引物,降低该引物的终浓度 ;反之,产物量较少的引物则增大其终浓度。
1.6 电泳各种实验条件优化过程中,获得 PCR产物时均进行琼脂糖凝胶电泳。取 PCR产物 5 μL,点样于溴化乙锭染色的 2. 0%琼脂糖凝胶上,120 V电压,电泳 35 min。
1.7 DNA序列测定多重 PCR扩增结核杆菌敏感株 DNA,取 5 μL产物进行琼脂糖凝胶电泳,并切胶纯化进行 DNA序列测定,将测定结果与美国国立生物技术信息中心 ( National Center for Biotechology Information,NCBI) Genbank数据库存进行同源序列比对 ( basic local alignment search tool,BLAST),判断测序结果与目的序列是否具有高度同源性。
1.8 膜芯片探针设计与合成针对结核杆菌常见的耐药突变位点,用 Oligo 6. 0设计 36条野生型检测探针、16条突变型检测探针,设计阴性对照探针,取 katG基因下游引物 P2作为阳性对照探针。探针由上海生工生物工程公司合成并纯化。探针序列已申请专利 200910114023. 4。
1.9 膜芯片制备尼龙膜裁剪为 6.5 cm ×2 cm,取 0. 8 μL探针点于同一张尼龙膜上,室温晾干后 80 ℃烘烤 1~2 h后备用。
1.10 膜芯片杂交与结果判读室温下用 A液( 2 × SSC,0. 1% SDS,pH 7. 4)清洗膜片 30 s。55 ℃杂交炉预杂交15~ 30 min。将保持单链状态的变性产物加入预热的 A液中,55 ℃杂交 4h。同时预热 B液( 0. 5 × SSC,0. 1% SDS,pH 7.4),每张芯片需要 25 mL B液。取出膜片,放入 B液中,55 ℃洗膜 10 min。取出膜片,放入 10 mL POD溶液 ( 5 μL POD母液 +10 mL A液)中,置于摇床上,室温下轻摇 45 min。A液 25 μL室温下轻摇洗膜 5 min;重复洗一次 ; C液( 0. 1 mol/L柠檬酸钠,7. 4),25 mL室温下轻摇 3 min。新鲜配制并按顺序加入以下试剂: 19 mL C液 +1 mL TMB +10 μL 3%双氧水,室温下避光显色15~30 min。芯片置于清水中3~5 min,终止显色。结果判读 :当质控点阳性对照探针下处呈现蓝紫色斑点而阴性对照探针处无显色时,即可判定杂交显色结果。若野生型探针有杂交信号而突变型探针无杂交信号或者野生型探针的杂交信号远远强于突变型探针,则说明该位点无突变发生 ;反之,则说明该位点发生了相应的突变。
1.11 膜芯片检测应用多重PCR-膜芯片技术检测 52例结核杆菌临床分离株 DNA,结果与传统药敏试验相比较。
2 结果 2.1 单基因 PCR条件优化 (表 1,图 1、2)| 表 1 多重PCR反应体系 |
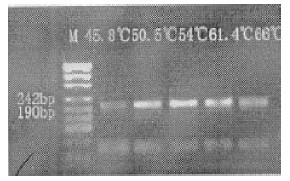 | 图 1 gyrA基因 PCR退火温度梯度 |
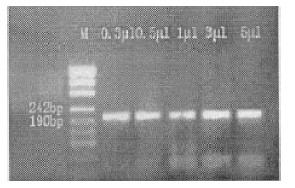 | 图 2 gyrA基因引物浓度梯度 |
对影响 PCR反应的条件如退火温度、引物浓度等进行优化,以 gyrA基因为例,扩增产物为 199 bp,如图 1所示,不同退火温度 45.8~ 66 ℃均出现 199 bp的条带,均无非特异性扩增,但 45. 8、 66 ℃时产物量少。因此,gyrA基因退火温度可选择在 54~ 61.4 ℃。如图 2所示,不同引物浓度0.3~ 5 μL均出现 199 bp的条带,产物量相当,但1~ 5 μL时可见引物二聚体。因此,将 gyrA基因最佳引物浓度确定为 10 μM,加入量可在 0.3~ 0. 5 μL。同样的,其余 11对引物,分别扩增 katG、inhA、ahpC启动子,rpoB、rpsL、rrs、embB、pncA耐药相关基因可变区,经过优化后,各单基因 PCR最终共同选择 58~60 ℃作为退火温度,引物终浓度为 200 pmol/L,镁离子终浓度为 1.5 mmol/L, Tap酶浓度为 1 U /25 μL作为单基因 PCR的最优条件。
2.2 多重 PCR(图 3)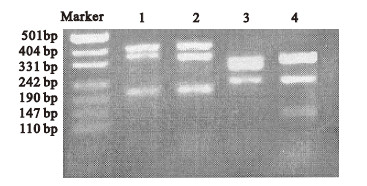 | 注: 1、2、3、4分别代表表 1中 rke,iag,rrp,pri。 图 3 多重 PCR电泳结果 |
按照单基因 PCR反应条件优化的方法,12对引物分 4管在同一条件下进行 PCR反应,对多重 PCR退火温度、引物浓度进行优化,获得最佳的多重 PCR反应体系;所有引物的浓度均为 10 μmoL /L,dNTP各2. 5 mmol/L,Taq酶为 5 U/μL。反应程度 : 95 ℃预变性 5 min,94 ℃ 50 s,60℃ 45s,72℃ 50s,共计 35个循环,72℃ 10min。
2.3 DNA序列测定结果12对引物的 PCR产物的 DNA序列测定所得的序列片段与 NCBI Genbank数据库进行在线 BLAST比对,结果与数据库中结核杆菌 H37Rv标准序列的符合率均> 96%,表明产物与目的的序列具有高度同源性。
2.4 膜芯片检测结果与传统药敏试验比较药敏试验显示耐药的 43株临床分离菌株,膜芯片检测有 42株判为耐药,灵敏度为 95. 35%,药敏试验显示敏感的 9株临床分离菌株,膜 芯片检测均判为敏感,特异度为 100%。其中膜芯片检测的耐药种类与药敏试验耐药种类完全一致率为 53% ( 23 /43),18株检测结果部分相同。
3 讨论痰培养 +药敏试验是临床上广泛采用的判断结核杆菌耐药性的金标准。由于结核杆菌生长缓慢,尤其是耐药菌株的生长更为缓慢,致使药敏获是结果需 6~8周,不能在患者治疗的初期及时地指导临床合理用药。现已确定耐药的抗结核药物主要是异烟肼、利福平、乙胺丁醇、链霉素、吡嗪酰胺、喹诺酮类等〔3〕,并已证明了结核杆菌的耐药性分别与 katG、 inhA、ahpC,rpoB、embABC,rpsL、rrs、pncA、gyrA B等基因突变有关〔4, 5, 6, 7, 8〕。
多重 PCR可节省模板,提高效率。首先,在多重 PCR引物设计时确保反应中所有的引物有相近的熔解温度,引物之间不会发生相互作用。其次,根据以下原则对多重 PCR进行优化〔9〕:第一,确保所有的靶位点可以用相同的 PCR程序在单个的反应中得到有效的扩增 ;第二,在使用相同的 PCR程序和反应条件的前提下,对单个 PCR中每对引物的量进行优化以达到最大的扩增效率 ;第三,平衡多重 PCR中每对引物的量,使之对每个靶位点都能获得足够的扩增量。
本研究膜芯片检测 23株耐药株的耐药种类与药敏试验耐药种类完全一致率为 53. 5% ( 23 /43),比前期研究中试剂盒的 15. 0%〔1〕有明显提高,其中膜芯片对利福平耐药的检出率和准确率均达到 100%,这与利福平耐药基因的突变相对集中、探针的合理设计以及耐药机制主要为基因突变有关。
总之,本研究通过多重 PCR反应在同一反应条件下有效地扩增了结核杆菌 9个耐药基因,为膜片杂交检测提供了良好的前提。该方法从 PCR扩增到膜杂交结果判断仅需 1d时间,用生物素代替荧光作为标记,降低了检测成本,并可根据需要灵活调整、调换探针,具有简便经济、准确快速、易于保存等优点,对指导临床医生及早用药较有价值,具有广阔的应用前景。
| 〔1〕 | 韦世录,何晓,何敏,等.利用反向杂交膜片检测结核杆菌多耐药基因的研究[J].广西医科大学学报,2008,25(2):202-204. |
| 〔2〕 | 何敏,万逢洁,周凌云,等.反向杂交膜片检测结核菌耐利福平基因突变[J].中国公共卫生,2005,21(12):1420-1422. |
| 〔3〕 | Felmlee TA,Liu Q,et al.Genotypic detection of Mycobacterium tuberculosis rifampin resistance:comparison of single-strand conformation polymorphism and dideoxy fingerprinting[J].J Clin Microbiol,1995,33:1617-1623. |
| 〔4〕 | 崔振玲,景奉香,胡忠义,等.用DNA芯片快速检测结核杆菌对异烟肼的耐药性[J].中华检验医学杂志,2003,26(4):244. |
| 〔5〕 | Rudi R,Hamidou T,Hans D B,et al.Evaluation of the INNO-LIPA Rif TB assay,a reverse hybridization assay for the simultanceous detection of Mycobacterium tuberculosis omplex and its resistance to rifampin[J].Antimicrobial Agents And Chemotherapy,1997,41(10):2093-2098. |
| 〔6〕 | Zhang Y,Telenti A.Genetics of dray resistance in Myocbacterium tuberculosis[M]//Hatful GF,Jacobs Jr WR.Molecular Genetics of Myocbacteria,Washington DC:ASM Press,2000:235-251. |
| 〔7〕 | Sreevatsan S,Pan X,Stockbauer KE,et al.Restricted structural gene polymorphism in the Myocbacterium tuberculosis complex indicates evolutionary recent global dissemination[J].Proc Natl Acad Sci USA,1997,94:9869-9874. |
| 〔8〕 | 黄四邑,邱望龙,潘智灵,等.聚合酶链反映-单链构象多态性技术检测多药结核分支杆菌ropB、katG、rpsL突变的研究[J].中国防痨杂志,2001,23(6):341-343. |
| 〔9〕 | J.萨姆布鲁克,D.W.拉塞尔.分子克隆实验指南[M].3版,北京,科学出版社,2002:698-699. |
 2012, Vol. 28
2012, Vol. 28