目前,结核分枝杆菌 ( Mycobacterium tuberculosis,MTB)抵制抗结核药物的机制主要有 3种类型,即降低细胞膜的通透性和外排泵活性机制,产生降解或灭活酶类,药物靶位的改变。研究表明,结核分枝杆菌阻止药物通过细胞壁,引起细胞壁渗透性改变从而引起获得性耐药。近些年人们发现主动外排泵的表达,是另一种重要耐药机制 〔1, 2〕,并在获得性耐药中起主要作用。结核分枝杆菌的外排泵 RND超家族,为质子依赖型多药耐药外排泵,也称为 MMPL系统,首先在结核分枝杆菌 H37Rv中〔3〕发现,13个编码结核分枝杆菌的蛋白命名为 MmpL( mycobacterial membrane proteins),其中大部分功能尚不清楚。一些 MmpL蛋白共区域化,与多聚乙酰的生物合成有关 ( pks基因),并且这些基因与脂质代谢( papA,fadD )有关,其中 11个与膜通道蛋白及膜融合蛋白序列外排泵蛋白相关。序列分析发现,MmpL4不仅与细菌的增殖有关,而且与细菌毒力有关。为此,本研究构建了原核基因表达载体,研究其在大肠杆菌中的表达,为其进一步的功能研究提供依据。
1 材料与方法 1.1 细菌菌株及培养情况结核分枝杆菌标准菌株 H37Rv及无毒菌株 H37Ra由中国疾病预防控制中心万康林研究员惠赠,7H9培养基 (内含终浓度为 0. 05% Tween 80,终浓度为10%的 ADC营养物 )上培养,37 ℃培养 2~3周。大肠埃希菌在 L-B培养基生长 (内含卡那霉素 5 μg /mL)。
1.2 MMPL4跨膜结构分析利用TMHMM和 HMMTOP软件对 MMPL4蛋白跨膜结构域的数目、拓扑结构以及膜内外区域的分布进行预测。
1.3 引物设计根据 genebank中 Rv0450c基因序列设计引物,其中扩增全长 Rv0450c基因的上游引物为 5'-GCATGCTAGCAGTACTAAATTCGCGAACGACT-3',下游引物为 5'-GCATAAGCTTTCAGCCGAGGCGGTCG-3'。扩增 I161片段的引物为 5'-GCATGCTAGCTTTGTCCCGTCACTGGAAG3'和 5'-GCATAAGCTTTCACATGGTGATCCTGGCCAT-3';扩增 0371片段的引物为 5'-GCATGCTAGCCTCGCCCTGCCTGGATA-3'和 5'-GCATAAGCTTTCAAAGGTCCCATTGGGC-G-3',并在引物 5端分别设计引入 Nhe I和 Hind III酶切位点 (下划线部分 )。引物由英国 Invitation公司合成。 PCR扩增试剂盒购自美国 Takara公司。
1.4 质粒pET28b购自德国 Novagen公司,质粒提取试剂盒、大肠埃希菌 DH5α和 BL21( DE3) pLysS感受态菌株购自天根生化科技有限公司,DNA限制性核酸内切酶 Hind III、 Nhe I、核酸 markerDL 1000、蛋白分子质量 marker分别购自美国 Takara公司; DNA marker IV购自天根生化科技有限公司; DNA胶回收及 PCR产物纯化试剂盒购自美国 Takara公司。
1.5 DNA提取固体培养基上刮取菌落,悬浮于 500 μL TE( pH 8. 0),80 ℃水浴灭活至少 30 min。加入溶菌酶至终浓度 2 mg /mL,37 ℃孵育 2h。提取方法按照分子生物学实验手册 DNA抽取酚-氯仿提取方法〔4〕提取 DNA,-20 ℃保存。
1.6 PCR反应条件以结核分枝杆菌 H37Rv株的基因组为模板进行 PCR扩增目的基因。PCR扩增反应条件 : 94 ℃ 5 min; 94℃ 45s,59℃ 45s,72℃ 2min30 s,30个循环 ; 72℃ 10min。1. 2%琼脂糖凝胶电泳鉴定 PCR结果。
1.7 克隆PCR产物及重组转化子的鉴定扩增的 DNA片段经纯化后,用 Nhe I、Hind III 2种限制性内切酶在 37 ℃酶切 4h,将酶切产物经琼脂糖凝胶电泳,应用胶试剂盒回收纯化,将纯化产品与经同样酶切的 pET28b载体用 fermentase T4连接酶连接,转化大肠杆菌克隆感受态细胞 DH5α,于 LB固体培养基 37 ℃培养过夜。挑取培养好的单菌落,37 ℃恒温箱 250 rpm培养过夜。提取质粒,经 Nhe I和 Hind III双酶切鉴定,得到重组质粒 pET28b-Rv0450c。将重组质粒送往上海生工公司测序。
1.8 Rv0450c融合蛋白的诱导表达将上述正确构建的重组质粒转化 BL21( DE3) pLysS宿主菌,LB培养基 37 ℃培养过夜。挑取培养好的单菌落,37 ℃恒温箱 250 rpm培养过夜。将培养产物 1∶ 50稀释到接种于新鲜 LB液体培养基,加终浓度为 lmM的 IPTG诱导 3h后,5 000×g离心 10 min收集菌体,沉淀经 B-PER大肠杆菌裂解液 ( Invitrogen公司 )室温涡旋振荡处理 10 min后,离心,分别对上清和沉淀中的总蛋白进行 10% SDS-PAGE蛋白电泳分析,考马斯亮蓝 R250染色并脱色,分析融合蛋白的表达及重组蛋白的可溶性。
1.9 重组蛋白的纯化带6-His标签的重组蛋白的纯化按照 Invitrogen公司 B-PER 6 × His fusion protein purification kit试剂盒操作。约 150 mL含重组质粒的 BL21( DE3) pLysS宿主菌经诱导 3h后,离心收集菌体。菌体沉淀重悬在 5 mL B-PER裂解液中,并加入适量 complete miniEDTA-free prote-ase inhibitor cocktail蛋白酶抑制剂 ( Roche公司),室温涡旋振荡处理 10 min后,15 000 rpm离心 15 min,将离心上清加入到亲和层析柱中,待总蛋白完全通过后,分别用洗涤液 l和 2洗柱,最后用洗脱液收集重组蛋白,收集各步组分,进行 SDS-PAGE电泳分析。
2 结果 2.1 MTB H37Rv基因组Rv0450c基因编码蛋白质 MMPL4的特征 MMPL4总长为 966个氨基酸,理论分子量为 103 kDa,等电点预测为 9. 83。TMHMM和 HMMTOP软件预测该蛋白具有 11个跨膜螺旋结构,其中氨基酸 44~204和400~ 770分别为最大的膜内结构域和膜外结构域。
2.2 PCR扩增产物琼脂糖电泳结果(图 1)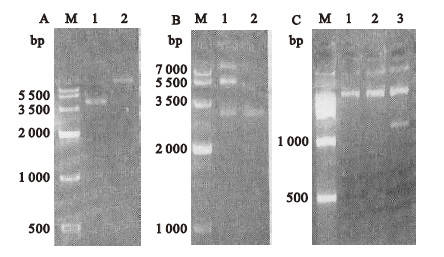 | 注: A为 H37Rv和 H37Ra基因组中 Rv0450c基因的扩增 ; M : DNA marker Ⅳ; 1: H37Rv基因组 DNA为模板 ; 2: H37Ra基因组 DNA为模板。B为 H37Rv基因组中 I161和 O371片段的扩增。M : DNA marker DL 1000; 1: O371编码基因片段 ; 2: I161编码基因片段。 图 1 Rv0450c基因和基因片段的 PCR扩增 |
以结核杆菌 H37Rv基因组 DNA为模板,以对应引物进行 PCR扩增,分别得到约 3 kb、1 kb以及 0.5 kb的特异性片段,与预期目的基因片段大小相符,且 H37Rv与 H37Ra基因组中 Rv0450c基因片段大小无明显差别。
2.3 重组质粒双酶切电泳检测结果 (图 2)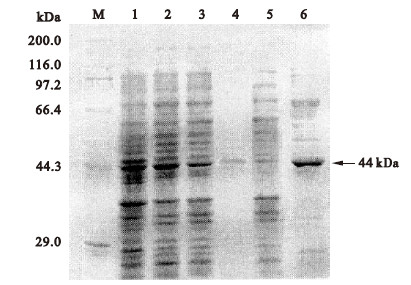 | 注: A为重组质粒 pET28b-Rv0450c与空白载体 pET28b电泳比较; l:空载体 ; 2:重组质粒 pET28b-Rv0450c。B为重组质粒 pET28b-Rv0450c双酶切检测 ; 1:不完全双酶切后的重组质粒; 2: MMPL4 PCR扩增产物。C为重组质粒 pET28b-I161和 pET28b-O371双酶切检测 ; 1:空质粒 pET28b; 2: pET28b-I161; 3: pET28b-O371。 图 2 重组质粒的鉴定 |
琼脂糖凝胶电泳对 H37Rv重组质粒 pET28b-Rv0450c与空载体 ( 5.4 kb)进行比较,重组质粒在胶上的移动速度明显慢于空载体 (图 2A)。进行 Hind III/Nhe I不完全酶切后产生 3条片段,其中重组质粒不完全酶切产生约 8.4 kb的线性载体片段,完全酶切产生约 5.4 kb的载体片段及与 PCR产物大小吻合的 3 kb插入片段 (图 2B)。重组质粒 pET28b-I16l和 pET28b-O371经 Nhe I/Hind III双酶切后,分别释放出大小约为 500和 1 000 bp的插入片段 (图 2C)。
2.4 重组质粒的测序鉴定重组质粒测序结果表明,克隆的目的基因核苷酸序列无碱基突变,与 Genebank上 Rv0450c编码序列完全一致,且插入片段读码框与表达载体读码框相吻合。
2.5 重组 MMPL4蛋白的诱导表达(图 3 )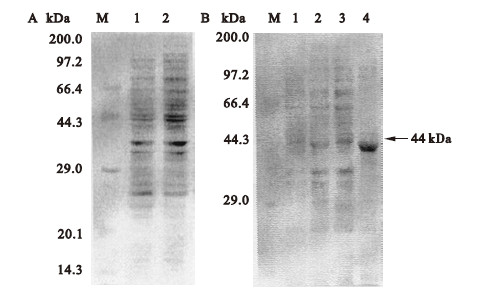 | 注: M :蛋白 marker; 1:诱导前 ; 2:诱导后 ; 3:诱导上清 ; 4:诱导沉淀; 5:亲和柱流出液 ; 6:纯化蛋白。 图 3 重组 MMPIA在大肠杆菌中的表达及纯化 |
重组质粒 PET28b-Rv0450c转化大肠杆菌表达菌株 BL21( DE3) pLysS,经 1mM IPTG诱导 3h后,进行 SDS-PAGE分析,如图 3所示,在理论分子量 100 kDa位置未见明显表达条带,但在 44 kDa附近有明显差异(比较图 3泳道 1和 2),该蛋白主要集中在上清中,在沉淀液中也见极少量表达。经 6 × His亲和层 析纯化后,该蛋白被特异性的分离出来 (图 3,泳道 6),表明重组 MMPL4蛋白在大肠杆菌表达过程中可能由于不正确折叠,缺乏糖基化保护等原因被降解。
2.6 重组 MMPL4蛋白膜内和膜外结构域的诱导表达(图 4)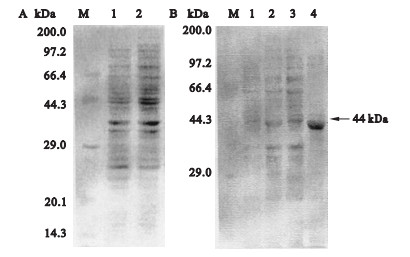 | 注: A: M :蛋白 marker; 1:诱导前 ; 2:诱导后。B: 1:诱导上清 ; 2:诱导沉淀 ; 3:亲和柱流出液 ; 4:纯化蛋白。 图 4 重组蛋白在大肠杆菌中的诱导表达 |
重组表达载体 pET28b-I161和 pET28b-O37l转化大肠杆 菌表达宿主 BL2l( DE3) pLysS,经 1 mM IPTG诱导 3h后,SDS-PAGE检测重组蛋白表达。膜内结构域 I161( 161个氨基酸,理论分子量 19 kDa)在诱导后未见清晰表达 (图 4A),而 O371( 371个氨基酸,理论分子量 44 kDa)表达量较高,在理论分子量附近出现清晰条带。进一步分析表明该蛋自主要为包涵体形式表达(图 4B)。
3 讨论外排泵蛋白由 Dano等〔5〕1972年在哺乳动物细胞中发现,与多耐药密切相关〔6〕,目前已发现数个与结核分枝杆菌和龟分支杆菌相关的外排 RND家族成员,与 10、36、98、154、 204和 205基因相关,运输不同的抗生素如利福平、氟喹诺同类、土霉素、氨基糖甙类等,还可能与异烟肼及乙胺丁醇的运输有关。但目前在临床中对菌株与耐药的研究尚不清楚。
Domeneeh等〔7〕研究结核分枝杆菌所有 MmpL蛋白,发现 MmpL4是鼠类结核模型复制有效生长的必需因素,缺少该蛋白可引起细菌毒力衰减。MmpL4抑制 IdeR相关的离子运输,MmpL4相关蛋白可能为结核分枝杆菌生长的调节基因。MmpL蛋白由 Rv0405c编码产生,本研究成功构建的结核分枝杆菌真核表达质粒 PET28b-Rv0450c,并在 BL21重组菌内表达,为进一步进行外排泵基因的相关研究提供了基础。但在表达中发现,该蛋白在理论分子量 100 kDa位置未见明显表达条带,在 44 kDa附近有明显差异,考虑该蛋白是一种膜蛋白,在转运过程中可能被降解或衰减,不以完全蛋白形式表达,从而使蛋白分子量变小。这一现象在构建的 MMPL4膜内结构域片段 I161的表达中也有体现。Lamichhane等〔8〕应用高通量 DNA探针检查小鼠肺内结核分枝杆菌生存基因,结果发现包括 MmpL4在内的 6个基因存在变异,并且 MmpL4衰减较明显,提示 MmpL4较其他膜蛋白更不稳定,容易降解,不易在重组菌中完全表达。由于 MmpL4衰减较快,干扰该蛋白的代谢,可以使结核分枝杆菌生长减慢或死亡,从而为新药研发提供理论依据。此外,本研究中 MMPL4蛋白膜外结构域 O371在大肠杆菌中的成功表达,为对 MMPL4的功能研究以及特异性抗体的制备提供了便利条件和实验基础。
| 〔1〕 | De Rossi E,Ainsa JA,Riccardi G.Role of mycobacterial efflux transporters in drug resistance:an unresolved question[J].FEMS Microbiol Rev,2006,30(1):36-52. |
| 〔2〕 | Colangeli R,Eelb D,Sridharan S,et al.The Mycobactefium tuberculosis iniA gene is essential for activity of an efflux pump that confers drug tolerance to both isoniazed and ethambutol[J].Molecular Microbiolog,2005,55(6):1829-1840. |
| 〔3〕 | Piddock LJV.Clinically relevant chromososmally encoded multidrug resistance efflux pumps in bacteria[J].American Society for Microbiology,2006,19(2):382-340. |
| 〔4〕 | 奥斯伯FM,布伦特 R,金斯顿RE,等.精编分子生物学实验指南[M].5版.北京:科学出版社,2008:47. |
| 〔5〕 | Dano K.Cross resistance between vinca alkaloids and anthracyclines in Ehrlichascites tumor in vivo[J].Cancer Chemother Rep,1972,56(6):701-708. |
| 〔6〕 | 吴健,张少平,穆瑞瑞,等.志贺菌外排泵基因emr基因克隆及耐药作用[J].中国公共卫生,2007,23(12):1494-1495. |
| 〔7〕 | Domenech P,Reed MB,Barry CE.Contribution of the Mycobacterium tuberculosis MmpL protein family to virulence and drug resistance[J].Infect Immun,2005,73(6):3492-3501. |
| 〔8〕 | Lamichhane G,Tyagi S,Bishai WR.Designer arrays for defined mutant analysis to detect genes essential for survival of Mycobacterium tuberculosis in mouse lungs[J].Infect Immun,2005,72(4):2533-2540. |
 2012, Vol. 28
2012, Vol. 28


