2. 河南科技大学医学院
随着抗生素的广泛应用,细菌耐药现象越来越普遍,给临床治疗带来巨大挑战。细菌耐药机制涉及多个方面,主动外排泵,尤其是耐药结节化细胞分化家族成员对革兰阴性菌的自身突变与获得性耐药的获得起重要作用〔1〕,目前研究较多的是大肠埃希菌AcrAB-TolC耐多药外排泵〔2, 3〕。研究表明,该泵在志贺菌属细菌中也存在〔4〕,调控基因marOR突变可能影响其介导的耐药性〔5〕。为探讨志贺菌属耐多药机制,为耐药性防治提供依据,本研究对志贺菌敏感株进行多抗生素诱导,建立耐多药模型,观察比较诱导耐药前后志贺菌敏感株marOR基因的差异及其诱导耐药后基因突变状况。结果报告如下。
1 材料与方法 1.1 材料 1.1.1 菌株(1)福氏痢疾杆菌标准株:菌株号51571-9(中国药品生物制品检定所)。(2)药敏实验标准控制菌:大肠埃希菌ATCC-25922(河南省临床检验中心)。(3)野生志贺菌敏感株Z23:来源于郑州大学第三附属医院临床分离株,由本实验室进行抗生素敏感性鉴定。采用改良K-B纸片法筛选1株对头孢噻吩(cephalothin,CF)、诺氟沙星(norfloxacin,NOR)、庆大霉素(gentamycin,GM)、磺胺甲基异恶唑(cotrimoxazole,SMZ)均敏感的福氏志贺菌作为敏感株。
1.1.2 试剂SS琼脂、EMB琼脂、营养琼脂、水解酪蛋白(Mueller-Hinten,MH)琼脂(上海市医学化验所);各种琼脂平板在本实验室按配方配制。头孢噻吩、诺氟沙星、庆大霉素、磺胺甲基异恶唑(中国药品检验中心)等抗生素均为标准品。聚合酶链反应(PCR)相关试剂(北京天根生化科技有限公司)。
1.1.3 引物marOR基因引物序列〔5〕A1: 5'-CACTCTTTAGCTAGCCTTG-3',A2: 5'-TGGACATCGTCATACCTCT-3',引物由北京赛百盛基因技术有限公司合成,扩增片段长度为604 bp。
1.2 方法 1.2.1 诱导志贺菌耐多药模型对野生志贺菌敏感株Z23进行生化、血清学及抗生素敏感性鉴定后,与标准株接种到固体培养基中,用肉汤稀释法测定最低抑菌浓度(minimalinhibitory concentration,MIC)。然后采用次抑菌浓度〔5〕,将标准株和敏感株分别在含1/2 MIC的CF、NOR、GM、SMZ的营养肉汤液体培养基中传代,建立诱导耐多药模型;12代后转无药物LB固体培养基,挑单个菌落测定MIC。判定标准:抗生素诱导后MIC/诱导前MIC≥4倍为耐药;设不含抗生素液体培养基中培养12代作为对照。
1.2.2 志贺菌marOR基因检测煮沸法提取模板DNA,采用聚合酶链反应扩增marOR基因,扩增体系为50 μL,其中三蒸水36.7 μL,10 × PCR反应缓冲液5 μL,dNTPs 1.5 μL,10μmol/L引物各1 μL,模板DNA 4 μL,5 U/μLTaq酶0.8 μL;反应条件为94 ℃预变性5 min,循环参数为: 94 ℃ 60 s,52 ℃45 s,72 ℃ 60 s共32个循环,最后72 ℃延伸10 min。取5 μLPCR产物进行1.5%琼脂糖凝胶电泳,用凝胶成像仪观察结果并照相。
1.2.3 核酸序列分析委托北京三博远志生物有限公司对敏感株和诱导耐药株marOR基因扩增产物核酸序列进行测序。
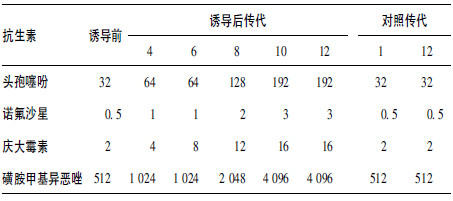
2 结果 2.1 菌株鉴定与耐多药模型临床分离志贺菌株为福氏志贺菌,对头孢噻吩、诺氟沙星、庆大霉素、磺胺甲基异恶唑4种抗生素均敏感,命名为Z23株。经4种抗生素1/2 MIC传代培养后,在无药物LB固体培养基上得到MIC≥4倍于诱导前的耐多药菌株,耐多药株MIC分别为初始菌株的6、6、8、8倍。表明成功建立志贺菌诱导耐多药株模型,并命名为YD株。
| 表 4 4种抗生素诱导志贺菌敏感株耐多药前后MIC(μg /mL)比较 |
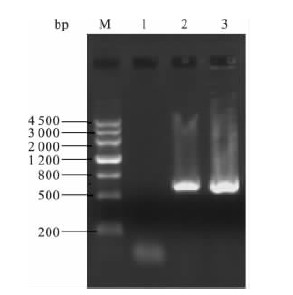 | 注: M: DNA Maker I; 1: 空白对照; 2: Z23; 3: YD。 图 1 marOR基因PCR扩增结果(604 bp) |
对志贺菌敏感株Z23和诱导耐药株YD的marOR基因进行PCR扩增,均扩增到约604 bp长度的目的片段,判定为marOR基因扩增产物。
2.3 核酸序列分析结果(图 2)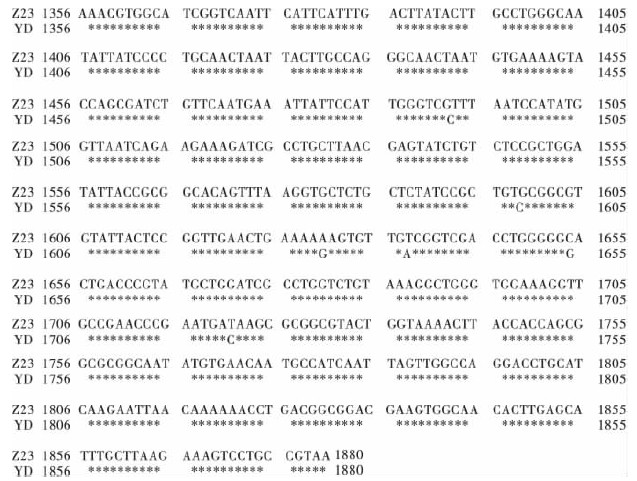 | 注: * YD株与Z23株碱基相同。 图 2 志贺菌Z23株与YD株marOR基因碱基位点比较 |
Z23株和YD株的marOR基因扩增产物的测序结果显示,发现诱导耐药株和与敏感株比较,YD株marOR有6个位点出现突变。其中有5个位点是同义突变,有1个位点为错义突变(1630位点A→G,赖氨酸→精氨酸)。
3 讨论本研究选择4类临床常用抗生素,体外诱导志贺菌耐多药模型,诱导过程与其在人体内产生耐药过程极为相似〔6〕。结果表明,通过诱导试验使细菌通过抗生素选择压力从垂直方向获得耐药性,最终得到MIC≥4倍于诱导前的耐多药志贺菌菌株。因为使用同一株志贺菌敏感株作初始菌株建立耐多药模型,避免了菌株不同而导致的差异,可比性较高。耐多药株诱导前后调控基因marOR位点变化比较结果显示,临床分离的志贺菌敏感株通过诱导耐多药后,marOR基因有6个位点出现突变,提示这些碱基尤其是1 630位点碱基突变可能引起acrAB-tolC泵基因的高表达,进而影响志贺菌耐多药性变化,但其具体作用需进一步研究。
| 〔1〕 | Poole K.Efflux-mediated multiresistance in Gram-negative bacteria[J].Clin Microbiol Infect,2004,10(1):12-26. |
| 〔2〕 | Perez A,Canle D,Latasa C,et al.Cloning,nucleotide sequencing,and analysis of the AcrAB-TolC efflux pump of Enterobacter cloacae and determination of its involvement in antibiotic resistance in a clinical isolate[J].Antimicrob Agents Chemother,2007,51(9):3247-3253. |
| 〔3〕 | de Cristobal RE,Vincent PA,Salomon RA.Multidrug resistance pump AcrAB-TolC is required for high-level,Tet(A)-mediated tetracycline resistance in Escherichia coli[J].Journal of Antimicrobial Chemotherapy,2006,58(5):31-36. |
| 〔4〕 | 杨海燕,段广才,郗园林,等.主动外排系统 acrAB在志贺菌中分布和表达[J].中国公共卫生,2005,21(6):685-687. |
| 〔5〕 | 吕锐利,段广才,宋春花,等.志贺菌临床分离株耐多药与调控基因突变关系[J].中国公共卫生,2008,24(5):568-570. |
| 〔6〕 | Adler-Mosca H,Luthy-Hottenstein J,Martinetti LG,et al.Development of resistance to quinolones in five patients with campylobacteriosis treated with norfloxacin or ciprofloxacin[J].Eur J Clin Microbiol Infect Dis,1991,10(11):953-957. |
 2012, Vol. 28
2012, Vol. 28