2. 江苏省南京市卫生监督所;
3. 南京医科大学公共卫生学院;
4. 南京军区军事医学研究所
丙型肝炎病毒(hepatitis C virus,HCV)属黄病毒属,病毒基因组是一单链正股RNA,其1~191位氨基酸编码可产生一种蛋白质,称之为核心蛋白(C蛋白),它能够影响宿主细胞多种分子,从而促进HCV感染慢性化和肝细胞癌进程〔1, 2〕。近年来研究显示,HCV RNA的C区通过移码读框表达另外一种低水平的新型C蛋白,被命名为选择性核蛋白体移码蛋白(alternative ribosomal frame shift protein,ARFP)或移码蛋白(frameshifting,F)〔3〕。研究表明,F蛋白可在HCV自然感染中产生〔4〕。血液透析患者是丙型肝炎病毒感染的高危人群,为探讨HCV-F蛋白在HCV致病中的作用,为F蛋白的功能研究提供线索,本研究选取血液透析患者,以HCV-F蛋白为捕获抗原,检测血液透析者血清F蛋白抗体,比较F蛋白抗体在特殊人群中的分布特点。
1 对象与方法 1.1 对象2008年6月-2009年1月选取江苏省2所三级甲等医院,1所二级甲等医院收治的血液透析患者500例,进行包括性别、年龄、血透时间等基本情况调查,并采集血清标本500份。选取其中HCV抗体阳性者128例,作为观察组,男性88例,女性40例,平均年龄(53.52 ± 11.20)岁。按就诊医院相同、年龄± 5岁,选取HBsAg和抗HCV均阴性的血液透析患者100例,作为对照组。
1.2 方法 1.2.1 试剂与仪器96孔板酶联反应板(上海晶美公司);辣根过氧化物酶(HRP)标记的羊抗人IgG抗体(南京阿恩地公司);抗原包被液为碳酸盐缓冲液(pH值9.6);封闭液、样本稀释液与酶标抗体稀释液均由本实验室配制;山羊血清(北京军区兽医防治中心),小牛血清(美国Hyclone公司);洗液为磷酸盐T缓冲液(含0.05% Tween-20)。辣根过氧化物酶(HRP)底物采用三甲氧基苯甲醛显色系统,底物及终止液(南京华欣药业生物工程有限公司,南京军区军事医学研究所制备);Model 550酶联免疫测定仪(美国Bio-Rad公司)。HCV-F/谷胱甘肽-S-转移酶(GST)蛋白(HCV-F/GST蛋白)制备见文献〔5〕。HCV抗体检测试剂(上海科华生物有限公司)。
1.2.2 HCV-F抗体检测每孔100 μL包被液(50 mmol/L碳酸盐缓冲液,pH值9.6)含0.1μg HCV-F/GST蛋白加入96孔板,44℃过夜。次日用磷酸盐T缓冲液(下文简称洗液)洗涤后,加入封闭液(含30%山羊血清和10%小牛血清的磷酸盐缓冲液,每孔100 μL),4℃封闭4 h。吸去封闭液后,洗液洗涤3次拍干。将待测血清用样品稀释液(含20%山羊血清,10%小牛血清和0.2% Tween-20磷酸盐缓冲液)做1:100稀释后加入包被封闭好的酶联反应板内,每孔100 μL,37℃反应30 min,同时设立空白对照。洗液洗板5次后,加入稀释好的辣根过氧化物酶标记的抗人IgG抗体(每孔100 μL),37℃反应30 min。洗板5次后,每孔加入三甲氧基苯甲醛底物A、B液各1滴,37℃避光显色15 min,再分别加入2 mol/L硫酸50 μL终止反应。用空白孔调零,酶标仪测定吸光度(A490)值。临界值=对照组平均值(A)+2s,观察组A值>临界值,定义为F抗体阳性,随机选择10%样本进行盲法重复检测。
1.2.3 乙型与丙型肝炎感染检测HBsAg,HBcAb,抗HCV检测采用酶联免疫吸附试验,试验步骤和结果判断均参照试剂盒说明书。HCV RNA检测方法参照文献〔6〕。
1.3 统计分析采用SPSS 13.0软件进行统计分析。两组均数比较采用t检验,率比较采用χ2检验,多因素分析采用Logistic回归方法,检验水准α为0.05。
2 结果 2.1 观察组血清标本HCV-F抗体阳性率对照组100例血清标本HCV-F抗体A490值为0.0450+0.0056,临界值为0.056 2。128例HCV感染者中,血清HCV-F抗体阳性(A490 > 0.056 2)58例,阳性率为45.3%。重复检测13例,均与第1次结果一致。
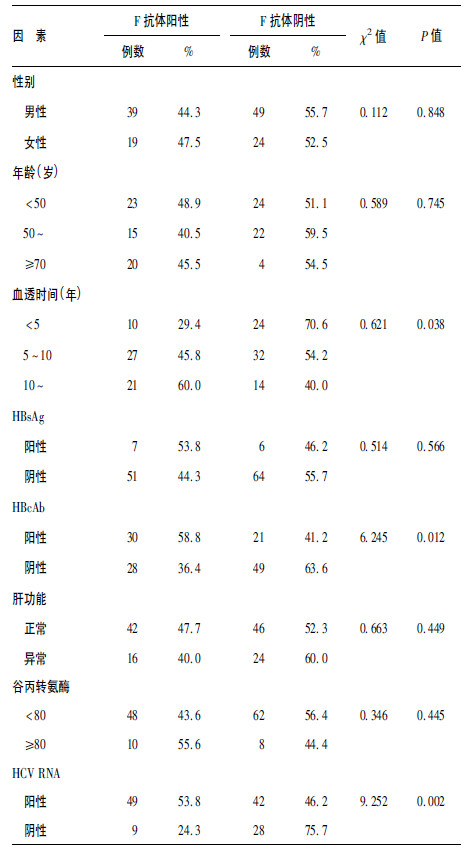
2.2 HCV-F抗体单因素比较(表 1)| 表 1 血液透析丙型肝炎感染者F抗体单因素分析 |
血透时间、HBcAb、HCV RNA的阴阳性与HCV-F抗体有统计学关联。
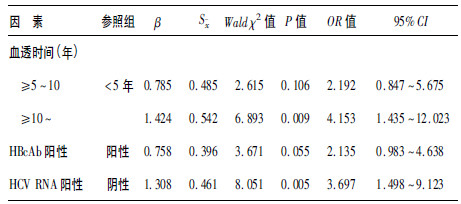
2.3 F抗体阳性率多因素分析将单因素分析有意义的3个因素变量纳入logistic回归模型,进行多因素分析,结果显示,血透时间、HCV RNA是F抗体阳性率的影响因素,血透时间≥10年和HCV RNA阳性会增加F抗体阳性的可能性。
| 表 2 血液透析丙型肝炎感染者F抗体阳性率多因素分析 |
国内外相关研究表明,在HCV慢性患者和HCV所致肝细胞癌患者体内可检出F抗体〔7〕,HCV所致肝癌患者肿瘤组织内可检出F蛋白准种〔8〕。本研究结果显示,肾透析患者HCV感染者中,F抗体阳性率为45.3%,提示F蛋白可在HCV感染者体内表达并诱导特异性体液免疫反应。
单因素分析结果显示,血透时间> 10年的HCV感染者的F抗体阳性率明显高于< 5年组,一方面可能由于血透时间越长机体抵抗力越差,从而使F蛋白在不同免疫水平机体中存在表达差异;另一方面可能与HCV感染时间长短有关。但由于HCV感染的真实时间较难获得,故本文未能做该方面分析。结果还显示,F抗体与血清HCV RNA间存在关联,差异具有统计学意义,提示F蛋白可能与病毒复制有关。
HCV、HBV具有相似的传播途径,常常引起双重感染。有研究表明,HCV/HBV之间的双重感染可以显著影响肝纤维化、肝硬变、肝癌的发生发展〔9〕。本研究结果表明,HCV/HBV联合感染与HCV单独感染比较,F抗体阳性率存在差异,提示F蛋白可能参与肝炎慢性化和肝细胞癌发生发展。
目前,HCV的致病机制尚不明确,阻碍了HCV疫苗和丙型肝炎治疗性药物的研制。研究HCV-F蛋白功能对了解HCV的致病机制有着重要的作用,本研究提示,F蛋白与HCV的感染时间和复制情况有关,可能在HCV的致病过程中起到重要的作用。
| 〔1〕 | Moriya K,Fujie H,Shintani Y,et al.The core protein of hepatitis C virus induces hepatocellular carcinoma in transgenic mice[J].Nat Med,1998,4(9):1065-1067. |
| 〔2〕 | 王旭东,贲昆仑,陈溥言.丙型肝炎病毒基因和结构蛋白研究[J].中国公共卫生,2004,20(8):998-1000. |
| 〔3〕 | Xu Z,Choi J,Yen TS,et al.Synthesis of a novel hepatitis C virus protein by ribosomal frameshift[J].EMBO J,2001,20(14):3840-3848. |
| 〔4〕 | Cohen M,Bachmatov L,Ben-Ari Z,et al.Development of specific antibodies to an ARF protein in treated patients with chronic HCV infection[J].Dig Dis Sci,2007,52(9):2427-2432. |
| 〔5〕 | 蒋春梅,刁振宇,崔国兴,等.丙型肝炎F蛋白的原核表达及初步应用[J].细胞与分子免疫学杂志,2007,23(2):134-137. |
| 〔6〕 | 许可,邓小昭,丁伟良,等.江苏省宜兴地区丙型肝炎病毒基因分型研究[J].中华流行病学杂志,2005,26(11):901-903. |
| 〔7〕 | Ogata S,Nagano-Fujii M,Ku Y,et al.Comparative sequence analysis of the core protein and its frameshift products,the F protein,of hepatitis C virus subtype 1b strains obtained from patients with and without hepaocellular carcinoma[J].J Clin Microbiol,2002,40(10):3625-3630. |
| 〔8〕 | Branch AD,Stump DD,Gutierrez JA,et al.The hepatitis C virus al-ternate reading frame(ARF) and its family of novel products:the alternate reading frame protein/F-protein,the double-frameshift protein,and other[J].Semin Liver Dis,2005,25(1):105-117. |
| 〔9〕 | Shi J,Zhu L,Liu S,et al.A meta-analysis of case-control studies on the combined effect of hepatitis B and C virus infections in causing hepatocellular carcinoma in China[J].Br J Cancer,2005,92(3):607-612. |
 2012, Vol. 28
2012, Vol. 28