大气污染可使呼吸道防御功能受到破坏。经呼吸道吸收的毒物大多可直接作用于呼吸系统,大气污染物因含有害气体、化学物质及金属等,对机体的影响可因含有的物质不同而不同,其中颗粒物(particulate matter,PM2.5)对人体的损害较大〔1, 2, 3, 4〕。为探讨大气污染对呼吸道微环境的影响机制,于 2008年12月-2009年3月,选择辽宁省沈阳市交通繁华地段为采样点,模拟大气污染现状,用Wistar大鼠制作大气污染动物模型,从病理学角度分析其对机体的致病机制和影响机制,为大气污染防治及其对人体的损害提供理论依据。
1 材料与方法 1.1 大气污染物的制备 1.1.1 总悬浮颗粒物(total suspended particulates,TSP)用 Mini Vol PM2.5便携式采样器和称重的47mm玻璃纤维滤膜采样(美国Air Metrics公司),分别在工业区和交通要道每天采样24 h,连续采集4个月,采样流量为6~8L/min。将采样后滤纸剪成1 cm × 1 cm大小,浸泡于蒸馏水中超声震荡20 min,用多层纱布过滤后将滤液离心,1 000 r/min,4℃,收集底层颗粒物,真空冷冻干燥,-80℃保存。
1.1.2 混合气体由大连特种气体产业公司提供标准混合气体,高、中、低浓度分别含SO2、NO2为192、120,96、60,48、30 mg/m3。染毒时分别稀释6倍。
1.2 实验动物SPF级Wistar大鼠80只,雌雄各半,体重 190~210 g〔北京维通利华实验动物技术有限公司,动物许可证编号:SCXX (京)2007-0001〕,在本实验室饲养1周,以观察其活动及进食是否正常。分别称体重后随机分为对照组及低、中、高剂量组4组,每组20只。
1.2.1 染尘采用气管注入法。用生理盐水配制TSP混悬液。高、中、低剂量组分别注入TSP 30、15、7.15 mg,灌注量为1 mL,对照组注入同体积的生理盐水。
1.2.2 染毒于染尘后的第2 d,各组动物分别进行静式吸入染毒。采用体积为60 L的有机玻璃染毒柜,每柜放入2只大鼠。对照组吸入一般空气,其他3组分别吸入稀释6倍的标准混合气体。高、中、低剂量组SO2浓度为32、16、8 mg/m3,NO2浓度为20、10、5 mg/m3。每天染毒2 h,分别连续染毒1、7 和30 d。用快速检气管测定染毒柜内SO2、NO2浓度。
1.3 动物处理方法于染尘染毒后第2 d,第8 d和第31 d处死。
1.4 病理学观察在各组动物中分别随机抽取2只大鼠,取其气管及支气管用3%戊二醛(pH 7.6,0.1 mol/L二甲砷酸钠缓冲液)固定,采用冷冻割断技术制备样品,在H-500型日立透射电子显微镜和KYKY1000B型扫描电子显微镜下观察。
2 结 果 2.1 大鼠气管扫描电镜观察(图 1、2) | 注: A: 对照组: B: 染毒1 d 组; C: 染毒7 d 组: D: 染毒30 d 组。图 1 PM2.5中剂量染毒大鼠扫描电镜下气管超微结构( 2 000 × ) |
 | 图 2 PM2.5中剂量染毒大鼠扫描电镜下肺超微结构改变( 2 000 × ) |
由图 1可见,对照组气管柱状上皮纤毛密集而规整。随着染尘染毒剂量的增高,气管上皮纤毛粘连、紊乱;中剂量组出现粘连、倒伏。PM2.5 对气管柱状上皮的影响只是导致上皮纤毛粘连、紊乱、倒伏和缺失,而不出现鳞状化生和新生的纤毛柱状上皮细胞。从图 2 可见,PM2.5对大鼠肺组织的损害比对气管上皮的损害严重得多,中剂量PM2.5染尘染毒30 d,可使肺纤维增生,肺泡腔变小。 而中剂量PM10染尘染毒30 d,仅见尘细胞聚集、包裹,形成颗粒。高剂量PM2.5染尘染毒30 d,可使肺泡上皮细胞脱落溶解。
2.2 大鼠气管和肺组织透射电镜观察(图 3、4)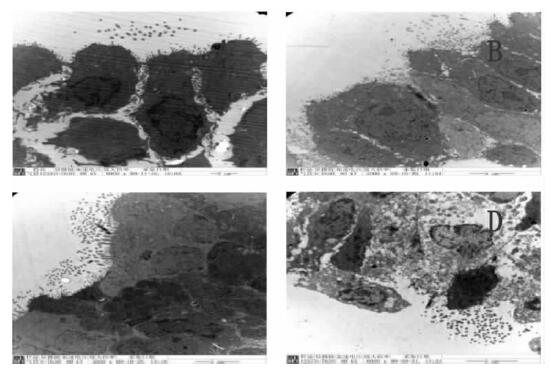 | 注: A: 对照组: B: 染毒1 d 组; C: 染毒7 d 组: D: 染毒30 d 组。图 3 PM2.5中剂量染毒大鼠透射电镜下气管超微结构( 5 000 ~ 8 000 × ) |
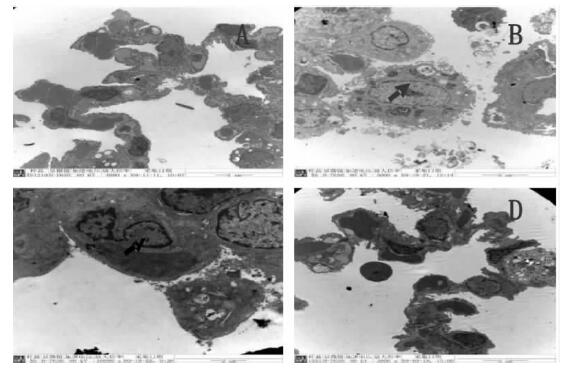 | 注: A: 对照组: B: 染毒1 d 组; C: 染毒7 d 组: D: 染毒30 d 组。图 4 PM2.5中剂量染毒大鼠透射电镜下肺超微结构( 4 000 ~ 10 000 × ) |
由图 3可见,正常气管上皮纤毛密集,中剂量染尘染毒后1 d使肺泡上皮排列不规则;7 d肺泡上皮紧密连接消失;30 d肺泡上皮细胞溶解脱落。气管上皮细胞空泡变性,纤毛变少;进行高剂量染尘染毒后气管上皮纤毛短稀,且出现大量吞噬泡,泡内可见吞入的微尘颗粒,气管软骨细胞出现蜕变坏死,核呈肿胀、均质化,胞浆结构不清,严重的水肿变性。随着染尘染毒后时间的延长,在第8 d时,低、中剂量组气管病变多己恢复正常,高剂量组气管上皮也大多恢复,新生上皮纤毛排列较紊乱,偶见有上皮小溃疡。由图 4可见,染毒:1 d出现肺泡上皮细胞核固缩;7 d出现肺泡上皮细胞核碎裂;30 d肺泡上皮细胞核溶解、核膜断裂。
3 讨 论呼吸系统是大气污染直接作用的靶器官。流行病学研究表明,空气中的细颗粒物(PM2.5)、SO2等与慢性阻塞性肺部疾病、肺心病及肺癌的死亡率明显相关;肺功能明显著降低与暴露于酸性气体、NO2和PM2.5有关;城市大气污染与炎症、氧化应激、血凝及心率紊乱均有关,而且这些效应主要是由交通污染中的硫酸盐和臭氧引起,可见大气污染所致的负健康效应是多种污染物共同作用的结果〔5, 6〕。本研究通过透射电镜观察结果表明,长期吸入含有PM2.5有害气体,可使大鼠气管上皮细胞损伤,但与前期研究报道〔7〕的PM10对大鼠气管柱状上皮纤毛影响不同,即随着染尘染毒剂量的增高局部出现鳞状化生,并且可见新生的纤毛柱状上皮细胞。PM2.5对大鼠呼吸系统的损伤主要在肺组织,大量吸入含有PM2.5有害气体,可使肺泡上皮排列不规则;肺泡上皮紧密连接消失;肺泡上皮细胞溶解脱落。气管上皮细胞空泡变性,纤毛变少、出现大量吞噬泡,泡内可见吞入的微尘颗粒,气管软骨细胞出现蜕变坏死,核呈肿胀、均质化,胞浆结构不清,严重的水肿变性。同时出现肺泡上皮细胞核固缩、核碎裂、溶解、核膜断裂等肺泡上皮变性坏死现象。扫描电镜观察结果表明,长期吸入含有 PM2.5有害气体,可以导致大鼠气管上皮纤毛粘连、紊乱、倒伏和缺失,更为严重的是可以导致可使肺纤维增生,肺泡腔变小。而肺纤维增生,肺泡腔变小是肺硬化和肺功能丧失的表现。停止染毒后电镜观察表明,动物气道上皮有缓慢修复的明显变化,因此再次证明改善环境的重要性。
| 〔1〕 | Laumbach RJ.Outdoor air pollutants and patient health[J].Am Fam Physician,2010,81:175-180. |
| 〔2〕 | Eilstein D.Prolonged exposure to atmospheric air pollution and mortality from respiratory causes[J].Rev Mal Respir,2009,26:1046-158. |
| 〔3〕 | Joad JP.Smoking and pediatric respiratory health[J].Clin Chest Med,2002,2(1):37-40. |
| 〔4〕 | 刘春涛,王曾礼,冯玉麟,等.哮喘气道炎症中嗜酸性粒细胞凋亡与IL-5、IL-10关系的研究[J].华西医科大学学报,2001,32(10):55-58. |
| 〔5〕 | Harrod KS,Jaramillo RJ,Berger JA.Inhaled diesel engine emissions reduce bacterial clearance and exacerbate lung disease to Pseudo-monas aeruginosa infection in vivo[J].Toxicol Sci,2005,83 (1):155-165. |
| 〔6〕 | Maitre A,Bonneterre V,Huillard L,et al.Impact of urban atmos-pheric pollution on coronary disease[J].Eur Heart J,2006,27(19):2275-2284. |
| 〔7〕 | 肖纯凌,王任群,赵肃,等.模拟大气污染所致大鼠气管的病理学改变[J].中国公共卫生,2005,21(9):1147-1148. |
 2011, Vol. 27
2011, Vol. 27
