氟骨症的病理表现复杂多样,主要是骨形成和骨吸收平衡破坏,骨转换加速〔1〕。成骨细胞功能活跃,在氟骨症病变中是一个发生较早、并起主导作用的环节。OSX是最近由Nakashima等〔2〕发现的成骨细胞特异性转录因子,只在发育的骨组织中特异性表达,是成骨细胞分化和骨形成过程中所必需的转录因子〔3〕。它在氟骨症的发生发展中的作用尚不清楚。本研究通过实时荧光定量PCR和免疫组织化学方法对饮水型慢性氟中毒大鼠骨组织中的OSX基因及蛋白表达进行检测,探讨OSX在氟骨症发病机制中的作用,为地方性氟中毒的防治提供参考。
1 材料与方法 1.1 主要试剂及仪器OSX兔抗大鼠多克隆抗体(北京博奥森生物技术有限公司)、SP9000免疫组化试剂盒、二氨基联苯胺显色(DAB)试剂盒(北京中杉金桥生物技术有限公司);Biomias2000彩色图像分析仪系统(四川大学图像图形研究所)。
1.2 动物分组与处理清洁级SD大鼠[四川大学动物实验中心,动物许可证号SCXK(川)-2006-10]36只,雌雄各半,体重100~120g,适应性饲养1周后,按性别和体重随机分为3组,每组12只,组内雌雄各半,对照组,自由饮用自来水(氟含量<1mg/L);低氟组,自由饮用含氟5mg/L自来水;高氟组,自由饮用含氟50mg/L自来水。各组大鼠喂饲全营养颗粒大鼠饲料。6个月后,收集大鼠24h尿样,股动脉放血处死大鼠,进行有关检测。
1.3 检测指标及方法 1.3.1 尿氟、骨氟含量检测骨标本先碳化、灰化后再采用氟电极法测定。
1.3.2 骨组织形态计量检查石蜡切片,苏木素伊红染色(hematoxylin-eosinstain,HEstain),应用彩色图像分析仪测量股骨下段骺板下1mm处的骨皮质厚度、骨小梁宽度、骨髓腔宽度、骨小梁百分比,每组每项指标随机选择5个视野,测定5个数值,取平均值,并进行统计学处理。
1.3.3 骨组织中OSX蛋白表达免疫组织化学(SP)法测定大鼠股骨下段骨中OSX蛋白表达,同时用磷酸盐缓冲液作为阴性对照,细胞浆或细胞核中出现棕黄色颗粒为阳性表达。计数每张切片5个视野的成骨细胞阳性细胞数,然后算出每张切片的成骨细胞平均阳性细胞数。
1.3.4 骨组织中OSXmRNA表达大鼠经股动脉放血处死,取一侧股骨迅速置于液氮中保存。Trizol法提取大鼠股骨下段总RNA,在DU60核酸蛋白分析仪上测量RNA样品的含量,选取A260/A280比值为1.9~2.1的样品进行反转录。引物设计和合成:通过Oligo6.0引物设计软件,设计引物序列。OSXmRNA引物上游:5'-CTATGCCAATGACTACCCACCC-3',下游:5'-CTGCCCACCACCTAACCAA-3'。参照物β-actin上游:5'-CCGTGAAAAGATGACCCAGAT-3',下游:5'-GGAAGAGGATGCGGCAGTG-3'。实时荧光定量PCR,按照QuantSYBRGreenPCRkit说明,real-timePCR反应体系为:cDNA模板2μL,2.5×RealMasterMix/20×SYBRsolution10μL,ddH2O6.4μL,引物上、下游(10mmol/L)各0.8μL,总体积为20μL。反应条件为:50℃120s,95℃600s,95℃15s,60℃60s,共40个循环。同时做65~95℃溶解曲线。
1.4 统计分析采用SPSS 16.0统计软件进行方差分析,每组所得结果用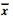 ±s表示,P<0.05差异有统计学意义。
±s表示,P<0.05差异有统计学意义。
表 1 各组大鼠尿氟、骨氟含量比较(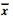 ±s,n = 12) ±s,n = 12) |
染氟组大鼠尿氟含量较对照组明显升高,各组间尿氟含量差异均有统计学意义(P<0.05,F=100.25);与对照组比较,各染氟组大鼠的骨氟含量明显升高,差异均有统计学意义(P<0.05,F=111.81)。
2.2 大鼠骨组织形态计量检查(表 2)
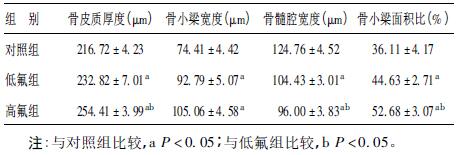
表 2 各组大鼠股骨形态计量学检查结果(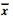 ±s,n = 12) ±s,n = 12) |
低倍镜下可见,对照组大鼠股骨远端骺板静止层和增生层的软骨细胞排列整齐,骨小梁粗细均匀、数目适中。染氟组大鼠股骨远端骺板增生活跃,骨小梁数目增多,排列紧密,骨髓腔变窄,表现为骨质硬化。
2.3 大鼠骨组织中OSX蛋白表达(图 1)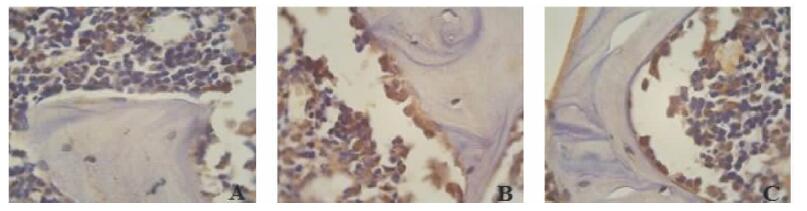 | 注:A 为对照组,B 为低氟组,C 为高氟组。图 1 慢性氟中毒大鼠股骨远端OSX 表达(SP 法,× 400) |
对照组免疫组化反应阳性产物染色较淡,成骨细胞稀少;染氟组阳性产物呈棕褐色,染色较深,成骨细胞数量显著增多。高氟组OSX阳性成骨细胞数增多[(51.47±3.37)个],明显高于低氟组[(36.80±2.83)个]和对照组[(27.00±2.92)个],差异有统计学意义(P<0.05,F=199.52);高氟组OSX阳性成骨细胞数与对照组相比有所增多,但差异无统计学意义。
2.4 各组大鼠OSXmRNA表达变化染氟组OSXmRNA表达量增加,低氟组为对照组的(2.10±0.09)倍,高氟组为对照组的(2.82±0.13)倍,与对照组比较,差异具有统计学意义(P<0.05,F=175.96)。
3 讨 论有研究证明,P物质(substanceP)可通过OSX表达促进成骨细胞分化及骨形成〔4〕。骨形态发生蛋白(BMP)2通过Smad途径、Dlx5上调OSX表达〔5, 6〕。OSX表达也受丝裂原活化蛋白激酶信号系统(MAPK)途径和蛋白激酶D途径的调控〔7〕。张亚楼等〔8〕的最新研究证实,氟可影响体外培养的成骨细胞OSXmRNA表达,呈现低剂量促进表达,高剂量下调表达的双向趋势。但OSX是否参与活体的氟骨症发病尚不清楚。
本实验中,随染氟剂量的增加,各染氟组OSX表达水平明显升高,提示氟可能是通过上调OSX的表达来促进骨髓间质干细胞向成骨细胞分化。本实验结果与前人的研究结果一致。因此,本实验结果证明,5mg/L的染氟剂量足以促进OB分化成熟,而50mg/L的染氟剂量对OB的促分化能力更加明显,这种现象证明长期小计量氟可促进骨形成;OSX蛋白参与过量氟对成骨细胞的促增殖和分化作用,是氟中毒时氟骨症发生的机制之一。那么,过量氟是通过哪些信号通路对OSX进行调控,成为研究关注的问题。
| 〔1〕 | Chambers TJ,Hall TJ.Cellular and molecular mechanisms in the regulation and function of osteoclasts[J].Vitam Horm,1991,46:41-86. |
| 〔2〕 | Nakashima K,Xin Z,Kunkel G,et al.The novel zinc finger-containing transcription factor osterix is required for osteoblast differentiation and bone formation[J].Cell,2002,108(1):17-29. |
| 〔3〕 | Ohyama Y,Nifuji A,Maeda Y,et al.Spaciotemporal association and bone morphogenetic protein regulation of sclerostin and osterix expression during embryonic osteogenesis[J].Endocrinolgy,2004,145(10):4685-4692. |
| 〔4〕 | 郭海锋,孙海飚,刘强.P物质在成骨细胞分化过程中对转录因子Osterix表达的影响[J].第四军医大学学报,2009,30(5):431-434. |
| 〔5〕 | 潘秋辉,李益广,杨松海,等.骨形态发生蛋白2通过Smad途径上调osterix的表达[J].中国生物化学与分子生物学报,2008,24(1):40-45. |
| 〔6〕 | Uisamer A,Ortuno MJ,Ruiz S,et al.BMP-2 induces osterix expression through up-regulation of Dlx5 and its phosphorylation by p38[J].J Biol Chem,2008,283(7):3816-3826. |
| 〔7〕 | Celil AB,Camphbell PG.BPM-2 and insulin-like growth factorⅠ-mediate osterix(Osx)expression in human mesenchymal stem cell via the MAPK and protein kinase D signaling pathways[J].J Biol Chem,2005,280(36):31353-31359. |
| 〔8〕 | 张亚楼,刘开泰,刘继文,等.氟对成骨细胞Runx2和Osterix及COLⅠA2表达的影响[J].中国地方病学杂志,2011,30(1):23-26. |
 2011, Vol. 27
2011, Vol. 27