2. 南昌大学医学院
真菌是引起变态反应疾病重要的变应原之一。研究显示,中国居民支气管哮喘和过敏性鼻炎的患病率约为8%,对以上患者皮试发现真菌变应原产生阳性反应达40% ~60% [1]。曲霉菌是过敏性哮喘、过敏性鼻炎的常见诱因; 杂色曲霉菌为曲霉菌属的一种,是湿热的沿海地区和内陆常见的室内外致敏真菌[2]。本研究对其变应原进行分离、鉴定和纯化,分离出特异性变应原组分,拟为真菌变态反应疾病的诊断和治疗提供科学依据。现将结果报告如下。
1 对象与方法 1.1 对象于2009年1~ 12月在广东省深圳市人民医院第一门诊部收集患者及健康者血清。由临床医生参照文献[3]确诊曲霉菌过敏患者并采集血清8份,其中男性4例,女性4例,年龄范围为12~ 57岁,平均年龄32 岁,血清中曲霉菌特异性IgE抗体(sIgE) 检测结果为≥ 2级(血清sIgE 的检测及等级评定方法参照多种变应原检测体系说明书); 非曲霉菌过敏健康者血清2份(血清中sIgE检测结果为阴性),男女性各1例,其中男性23岁,女性51岁,平均为37岁。
1.2 主要仪器与试剂垂直电泳槽、1000 /500 转膜电泳槽、常压层析控制系统(美国BIO-RAD公司) ; 凝胶成像及分析系统(法国VILBER LOURMAT 公司); 层析柱及快速蛋白液相层析系统(瑞典Pharmacia 公司)。生物素标记的IgE二抗、辣根过氧化物酶标记的亲和素(美国Kirkegaard& Perry Laboratories公司); 硝酸纤维膜(NC 膜) (美国Gelman Laboratory公司); DEAE-Cellulose DE-52离子交换柱填料、Hiprep 16 /60 Sephacry l S-200 High resolution高分辨率凝胶(瑞典Amersham Pharmacia公司)。其余试剂均为国产分析纯。
1.3 真菌变应原提取杂色曲霉菌(深圳大学生命科学院)接种活化后,挑取杂色曲霉菌孢子,接种于葡萄糖- 蛋白胨液体培养基,在25℃ ,相对湿度为75%的培养箱培养1周。将真菌生长物取出,蒸馏水冲洗1次。将真菌培养物破碎细胞(用剪刀剪碎)后,常规脱脂,自然干燥后,称重,用不同提取液制备变应原粗浸液: (1)碳酸氢盐- 盐水提取液(Coca' s液)提取: 取样品5 g 加入Coca' s液25 mL(w /v),4℃ 下提取72 h,期间每天磁力搅拌2次,每次1 h。将粗浸液15000 r/m in高速冷冻离心15 m in,取上清,4℃ 下对蒸馏水透析72 h后,冷冻干燥。- 80℃ 待用。(2)蒸馏水提取: 除提取液不同外,其余步骤同(1) 。
1.4 真菌变应原分离采用不连续十二烷基硫酸钠- 聚丙烯酰胺凝胶电泳(SDS- PAGE)体系分离粗提液中蛋白质组分并测定分子量。用12%分离胶、5% 浓缩胶进行电泳,脱色后用凝胶成像及分析系统拍照并分析分子量。
1.5 真菌变应原免疫学特性鉴定参照文献[4]采用免疫印迹(western-blot)对曲霉菌过敏性病人血清进行免疫学特性鉴定。
1.6 真菌变应原纯化(1)离子交换层析: 离心杂色曲霉菌粗提液,取上清对0.02 mol/L tris-HCl(pH 7.2)缓冲液透析2d。参照文献[4]进行离子交换层析(ion exchange chromatography,IEC)。(2)高分辨凝胶过滤层析: 将离子交换层析后收集的活性部分对凝胶过滤层析平衡缓冲液透析1 d,冷冻干燥,重悬后参照文献[5]进行高分辨率凝胶过滤层析(gelchrom atography,GL)。将以上2种层析收集的组分进行SDS-PAGE 和western-blot分析。
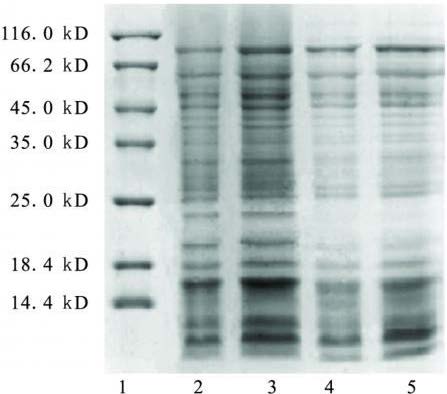
2 结 果 2.1 SDS-PAGE电泳(图 1)Coca' s液提取法提取的杂色曲霉菌蛋白条带有23 条,分子量分别为106、87、62、55、52、47、44、39、37、35、31、29、27、25、23、21、20、18、17、15、13、12、10kD。水提取法提取的条带有19 条,分子量分别为109、87、62、52、47、44、40、37、35、31、30、28、26、20、18、17、13、12、11kD。用Coca' s提取法所得的蛋白质条带无论数量和清晰度均明显优于水提取法。
|
注: 1: 标准蛋白分子量; 2~ 3: Coca' s粗浸液,蛋白质上样量分 别为5和10 μg; 4~ 5: 水粗侵液,蛋白质上样量分别为5和10 μg。 图 1 杂色曲霉菌粗浸液SDS-PAGE 结果 |
收集8例曲霉菌过敏患者血清对杂色曲霉菌粗浸液中的变应原进行免疫印迹,结果显示,分子量为62(6例)、20(5例) 、17 kD(5 例)的变应原可与> 50%的曲霉菌过敏病人血清中特异性IgE 结合,鉴定为主要变应原。而分子量为76(1例)、35(1例) 和22 kD(2例) 的变应原可与< 50% 的曲霉菌过敏病人血清中特异性IgE 结合,为次要变应原。
2.3 杂色曲霉菌变应原纯化 2.3.1 杂色曲霉变应原的离子交换层析用对DE - 52 离子交换层析缓冲液充分透析的杂色曲霉菌粗浸液上柱,结果显示,有6个蛋白峰,经SDS-PAGE 和免疫印迹检测分析表明,主要变应原组分在Ⅱ 峰(IEC-Ⅱ 峰)。
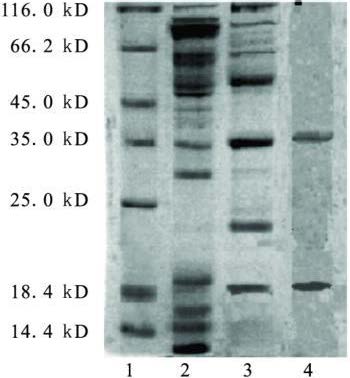
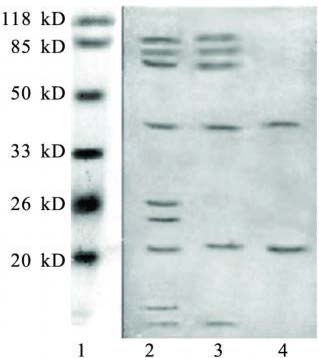
2.3.2 杂色曲霉菌变应原的凝胶过滤层析(图 2,3)将离子交换层析Ⅱ 峰对水透析后上凝胶过滤层析柱,结果显示,有2个蛋白峰,经SDS-PAGE和免疫印迹检测分析表明,主要变应原组分在Ⅱ 峰(GL-Ⅱ 峰)。
|
注: 1: 标准蛋白分子量; 2: 杂色曲霉菌提取液; 3. IEC-Ⅱ峰; 4: GL-Ⅱ峰。 图 2 杂色曲霉菌变应原凝胶层析峰电泳结果 |
|
注: 1: 预染蛋白分子量; 2: 杂色曲霉菌提取液; 3. IEC-Ⅱ峰; 4: GL-Ⅱ 峰。 图 3 杂色曲霉菌变应原凝胶层析峰蛋白印迹图 |
在引起变态反应性疾病的众多变应原中,大气致敏真菌是最重要因素之一[6]。过敏性哮喘病人约有30%对真菌过敏[7]。杂色曲霉菌是湿热沿海及内地常见的气传真菌,与过敏性呼吸道疾病的关系密切[8, 9]。真菌变应原/抗原受很多因素影响,如不同培养基、培养时间和周围的生长环境。本研究在参考文献[10]基础上优筛了杂色曲霉菌的最优培养方法和条件,选用第7 d对数生长物进行变应原制备。另外,通过不同提取方法初步分离出了20~ 30种蛋白质成分,分子量在14~ 120 kD,而用Coca' s提取法得到的蛋白质条带的数量和清晰度均高于水提取法。本研究结果表明,分子量为62、20、17 kD的蛋白为杂色曲霉菌主要变应原,分子量为76、35、22kD的蛋白为次要变应原。本研究通过离子交换和凝胶层析等方法初步纯化出分子量为20 kD主要变应原和35 kD的次要变应原组分,为进一步得到纯度更高的变应原组分和研究其理化性质提供了科学依据。
| [1] | 叶世泰.变态反应学[M].北京:科学出版社,1998:230-258. |
| [2] | Gibson PG.Allergic bronchopulmonary aspergillosis[J].Semin Respir Crit Care Med,2006,27(2):185-191. |
| [3] | 李明华,殷凯生,朱栓立.哮喘病学[M].北京:人民卫生出版社,1998:536-540. |
| [4] | 杨慧,刘志刚,韩庆国,等.艾蒿花粉主要变应原的分离、纯化与鉴定[J].中华微生物学和免疫学杂志,2005,25(1):73-77. |
| [5] | 喻海琼,刘志刚,张帆,等.刀额新对虾变应原的分离、鉴定与纯化[J].中国公共卫生,2006,22(10):1199-1201. |
| [6] | Baxi SN,Phipatanakul W.The role of al.ergen exposure and avoidance in asthm a[J].Adolesc Med State Art Rev,2010,21(1):57-71. |
| [7] | Ibez M D,Navarro A,Snchez M C,et al. Rhinitis and its association with asthma in patients under 14 years of age treated in alergy. departments in Spain[J].J Investig Allergol Clin Immunol, 2010,20(5):402-406. |
| [8] | Korpi A,Kasanen JP,Raunio P,et al. Acute effects of Aspergillus versicolor aerosols on murine airways[J].Indoor Air,2003,13(3):260-266. |
| [9] | Bellanger A P,Rebousx G,Roussel S,et al. Indoor fungal contamination of moisture damaged and alergic. patien thousing analysed using real time PCR[J].Letters in Applied Microbiology,2009,49(2):260-266. |
| [10] | Ishibashi K I,Kurone Y,Motoi M,et al. The in fluence of glucan on the growth and cell walarch. itecture of A spergillus spp[J].Microbiology and Immunology,2010,54(11):666-672. |
 2011, Vol. 27
2011, Vol. 27


