2. 沈阳军区药品检验所;
3. 辽宁大学生命科学院动物资源与疫病防治重点实验室
目前,人类中枢神经系统的淀粉样纤维疾病与7种蛋白质或它们的酶解产物有关[1, 2]。其中淀粉样血管病(cy statin Camyloid angiopathy,CAA) 是一种直接与cystatin C 蛋白基因突变引起68位氨基酸突变的显性遗传病,其特点是在血管内形成淀粉样组织沉淀,从而导致中风、脑出血等严重后果[3, 4]。由于人cy statin C 和鸡半胱氨酸蛋白酶抑制剂(ch icken cy ste tine,cC)在结构上有许多相似性,具有更高的热力学稳定性,而且在蛋白质结晶中能够分离出单体形式,因此,本研究利用前期构建的毕赤酶母X-33菌株实现具有天然N-末端的重组cC 的可溶性分泌表达,并对重组cC 类淀粉样特性的研究[5],为淀粉样血管病的发病机制研究提供理论基础。
1 材料与方法 1.1 材料酵母菌株菌株cystatin-pPICZαA-X-33(辽宁大学动物资源与疫病防治重点实验室构建),Aβ、硫磺素T (美国Sigma公司) ,木瓜蛋白酶(USPP 6000 Pmg) (国药集团化学试剂有限公司),酪蛋白(北京奥博星生物技术责任有限公司),其他化学试剂为进口或国产分析纯产品。
1.2 方法 1.2.1 重组cC的诱导表达取甘油保种菌株cystatin-pPICZαA-X-33接种于5 mL 酵母浸出粉胨葡萄糖琼脂(yeastextract peptone dextrose,YPD) 液体培养基,30℃ ,180 r /min振荡过夜培养。取50 μL分别涂布于YPD 固体平板,30℃ ,倒置培养48 h。将0.5 mL菌体转接至50 mL YPD液体培养基中进行次级培养24 h。将菌液分装离心管中,1 500 g离心5 min,弃上清。无菌水稀释沉淀,3 000 g离心5 min,弃上清。用酵母膏胨脂(yeast extract peptonem edium,YPM) 培养基培养基稀释沉淀菌液,到A600值约为1时,30℃ ,180 r /min 振荡过夜培养,并于诱导表达起始后,每隔24 h 补加100% 的甲醇溶液至终浓度为0.5%。连续诱导表达72 h,4℃ 下3 000 g离心10 min,去菌体回收上清液。硫酸铵分段盐析,十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(soddodecy l su lfate-po lyacry lamide gel electrophores is,SDS-PAGE)检测。
1.2.2 刚果红(Congored,CR)染色参照Gu ijarro[6]的方法,将1 m g /mL 的蛋白样品(2 mL) 溶于反应缓冲液(66mmol/L甘氨酸-HCl,pH 2.0) 中,终体积达到10 mL,混合均匀后于57℃ 培养30 d。每6 d取出1.5 mL加入相同体积新鲜配制的刚果红溶液(30 μmo l/L,在使用前用0.2 μm 滤器过滤) ,混合均匀后于室温静置30 min后,分别在480 nm 和540nm 处测定吸光度A 值,根据公式计算: 刚果红结合量(Congored binding,CRB) (μmol/L) = (A540 /25295) - (A480 /46306)。
1.2.3 硫磺素T(thioflavine-T,Th-T)荧光分析聚积方法Th-T荧光分析检测cC 的荧光强度随聚积量增强,淀粉样纤维的浓度在0~ 2.0 mg /mL范围内,荧光强度的大小和淀粉样纤维的浓度成正比,从而间接地判断cC是否聚集以及聚集的程度[5, 7, 8]。取1 μg /μL的蛋白样品溶液各2 mL置于细胞培养板中,37℃ ,5% CO2培养箱中分别孵育0、1、10、20和30d。以0 d 空白对照,以牛血清蛋白(bov ine serum a lbumin,BSA) 为阴性对照组,将1 μg /μL Aβ (am ylo id prote in β,Aβ)溶液为阳性对照组[5, 7, 8]。取各时间组孵育液20 μL 和新鲜配制的3.0 μmol/L硫磺素T溶液80 μL充分混合,Th-T 在Ex= 440 nm,Em = 510 nm 处下荧光分光光度计检测,进行固定时间扫描,记录5 min 末的荧光强度,以3次独立实验的平均值作为该组的荧光强度(fluo rescence intensity,FI) 。
2 结 果 2.1 重组cC表达结果酵母培养上清液经SDS-PAGE 及考马斯亮蓝染色后,可见重组蛋白条带,质量约为14 kD。
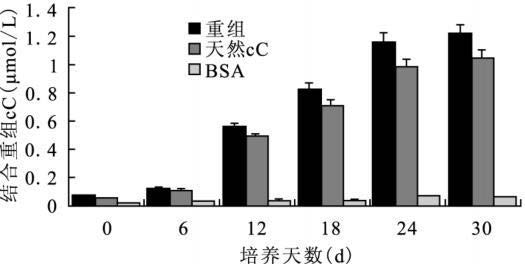
2.2 重组cC紫外分光光度检测类淀粉样沉淀(图 1)在pH 2甘氨酸-盐酸缓冲溶液中,刚果红为蓝色,λmax = 540 nm;当淀粉样沉淀重组cC特异性地与刚果红结合形成红色复合物结合时,吸收峰发生紫移,λmax = 480 nm。在57℃ 、pH 2的极端条件下培养30 d的重组cC,与刚果红的结合量随时间的延长而增大,第30 d达到了约1.21 μmo l/L,天然的cC培养30 d后与重组cC 相比沉淀略少(1.05 μmo l/L),而作为对照的牛血清蛋白在同样条件下培养30 d 后仅有0.07 μmo l/L,与0 d相比变化不大。
|
图 1 与刚果红结合的重组cC 的量 |
各组重组cC孵育如表 1所示,无盐酸胍组孵育1d和荧光物质Th 2T溶液的荧光强度接近表明孵育1 d的重组cC 未发生类淀粉样蛋白的聚集或未发生明显聚集; 孵育10、20 和30 d后,重组cC荧光强度逐渐升高,说明随着孵育时间延长,重组cC聚集程度逐渐增高,尤其孵育30 d组荧光强度大幅度提高。而盐酸胍组基本未变,说明盐酸胍能破坏重组cC 类淀粉样蛋白的聚集。
|
|
表 1 孵育时间与荧光强度关系 |
利用本实验的方法表达出来的重组cC,经非变形聚丙烯酰胺凝胶电泳native-PAGE 电泳表明具有分子内二硫键,显微镜观察和荧光分光光度计分析结果也显示重组cC 形成类淀粉样沉淀的倾向,同时,随着培养时间的增加,沉淀更明显。重组cystatin C突变体I66 Q 的类淀粉样沉淀形成的明显效果[5],这种结论在实验室的前期的分子动力学的模拟也得到了验证[9]。研究还表明,同是类淀粉样蛋白的疯牛病病原体朊病毒也可通过该方式形成三聚体,从而进一部形成纤维[10]。因此,有关cystatin C 致病机制的研究将为解决疯牛病、帕金森氏症、阿尔茨海默症等相关淀粉样病变疾病提供理论指导。
| [1] | Arjan Q,Ivo DH.Amyloidion channels:a common structural link for proteinmis folding disease[J].PNAS,2005,102(30):10427-10432. |
| [2] | McCarron MO,Nicoll JA.Cerebral amyloid angiopathy and throm bolysis related intracerebral haem orrhage[J].Lancet Neurol, 2004,3(8):484-492. |
| [3] | Sanders A,Jeremy Craven C,Higgins LD,et al. Cystat in forms a tetramer through structural. rearrangement of domain swapped dmiers prior to amyloidogenesis[J].J Mol Biol, 2004,336(1):165-178. |
| [4] | He JW,Song Y T,Nobuhiro U,et al. Prevention of amyloid fibril for mation of amyloidogenic chicken cystatin by site specific glycosylation in yeast[J].Protein Sci, 2006,15(2):213-222. |
| [5] | 张慧丽,杨松,何金萍,等.天然氮末端重组cC可溶性分泌表达[J].中国公共卫生,2008,24(4):485-487. |
| [6] | Guijarro J,ISundeM,Jones JA,et al. Am yloid fibril formation by an SH 3 domain[J].PNAS1998,95,4224-4228. |
| [7] | 罗焕敏,谷峰,李晓光.牛膝醇提物对A42聚集的抑制作用[J].中药材,2003,26(6):412-415. |
| [8] | He WJ,Sakamoto T,Song Y T,et al. Effect of Eps1 gene deletion in Saccharomyces cerevisiae on the secretion of foreign proteins which have disulfide bridges[J].FEBS Letters,2005,579(11):2277-2283. |
| [9] | 张慧丽,刘元,于媛媛,等.用分子动力学方法对Cystatin蛋白的研究[J].辽宁工程技术大学学报,2008,27(3):472-475. |
| [10] | Sichun Y,Herbert L,Jos NO,et al. Structure of infectious prions:stabilization by domain swapping[J].The FA SEB Journ al. 2005,19(13):1778-1782. |
 2011, Vol. 27
2011, Vol. 27


