2. 温州医学院药学院
目前常见的蛋白质染色方法有考马斯亮蓝染色法和银染法以及荧光染色[1]。在实际应用过程中,考马斯亮蓝染色灵敏度低,银染重现性差,荧光染色染料贵,且需要特殊仪器等。离子对染色体系根据离子对作用理论,在染料染色过程中,使用2种带相反电荷的染料,使染色溶液处于离子配对临界点,减少染色时间,增加蛋白质检测灵敏度; 所使用的染料分子同时是银离子敏化剂,可以促进银离子还原,增加银染的重现性和灵敏度。该染色系统把染料染色与银染过程结合,特别适于染料染色后再行银染。本研究将该体系应用于细菌蛋白染色并与其他染色试剂盒进行效果对比,结果报告如下。
1 材料与方法 1.1 主要试剂与仪器副溶血弧菌(本实验室分离保存);离子对染色体系(温州安德森公司)。适用于还原剂和去垢剂的蛋白质定量试剂盒、蛋白Marker、对比染料试剂盒、银染试剂盒(美国Bio-Rad公司); B-PER细菌蛋白质提取试剂(美国Thermo Fisher Scientific 公司); 丙烯酰胺、亚甲双丙烯酰胺、过硫酸铵、N,N,N',N' -四甲基二乙胺(TEM ED)、三羟甲基氨基甲烷(Tris)、溴酚蓝、二硫苏糖醇(DTT)、甘氨酸、十二烷基磺酸钠(SDS)、甘油(美国Amresco 公司)。Mini-PROTE-AN TetraM P 4电泳仪(美国Bio-Rad公司),UMAX Powe rLook2100 x l扫描仪。
1.2 细菌纯化扩增菌种复苏,接种于3 mL营养肉汤培养基,37℃ 振荡培养过夜,接种于150 mL营养肉汤振荡培养18 h。收集菌液,4 500 g离心10 min,去上清,生理盐水洗2次重悬,分装1.5 mL离心管,5 000 g离心2 min,收集菌体。每管约收获0.4 g 菌体(湿重) ,- 80℃ 冻存备用。
1.3 细菌裂解蛋白提取和定量将每管约0.4 g 细菌样品加入150 uL细菌蛋白提取液,超声破碎菌体,15 000 g 离心5min,留取上清,定量后稀释至1 μg /uL。
1.4 SDS-聚丙烯酰胺电泳灌制1 mm 厚聚丙烯酰胺凝胶(12%的分离胶+ 5%的浓缩胶,8 × 10 cm) [2]。上样量依次为10,2.5,5 /8,5 /32,5 /128,5 /512,5 /2048,5 /8192,5 /32768μg(依次进行4倍系列稀释上样)。每块胶第10孔加预染蛋白m arker。电泳条件: 20 V,20 min后升压至60 V 至溴酚蓝移到玻璃板最底部为止。
1.5 染色 1.5.1 染料染色离子对染料染色: 每块凝胶用固定液50%乙醇+ 10%乙酸100 mL,室温振摇固定30 min; 使用离子对染料染色液100 mL(将凝胶完全浸泡) 振摇染色过夜; 在固定液里脱色45 s,再用去离子水洗5~ 10 min至背景清亮条带清晰。国外进口染料染色按试剂盒说明书进行。
1.5.2 银染对比离子对体系银染程序: 凝胶用固定液50%乙醇+ 10%乙酸100 mL,振摇固定10min × 2次; 增敏2min(染料染色后银染无需增敏),水洗2 min × 2次; 银染5min,水洗2 min × 2次; 显影约8 min,至凝胶背景显黄色,加入终止液10 min至过夜。最后水洗至凝胶平展即可扫描成像。进口试剂盒银染按说明书进行(为比较最低显色样品量,显色至第一泳道发黑,连片为止)。
1.5.3 染料染色后复银染在染料染色的基础上进行银染复染时,离子对染色体系可略过固定和增敏步骤。
1.6 图像扫描分析(扫描仪投射扫描)染色后凝胶置扫描仪上平展,采用600 dp i投射扫描获取图像。
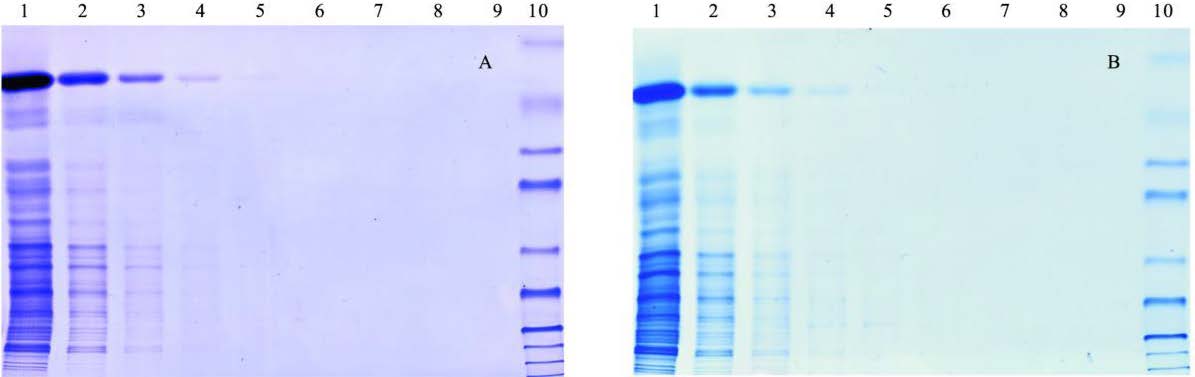
2 结 果 2.1 染料染色灵敏度(图 1)离子对染料染色对副溶血弧菌蛋白最低检出水平约为0.16 μg,与进口试剂盒染料染色相似,但染出的条带更清晰。
|
注: A: 离子对染色体系染色; B: 进口染色试剂盒染色; 1 ~ 9: 泳道: 副溶血弧菌蛋白, 第1泳道上样10 μg,以后依次稀释4倍上样; 第10泳道: 蛋白质分子量标志。 图 1 2种染色体系对副溶血弧菌蛋白染料染色效果比较 |
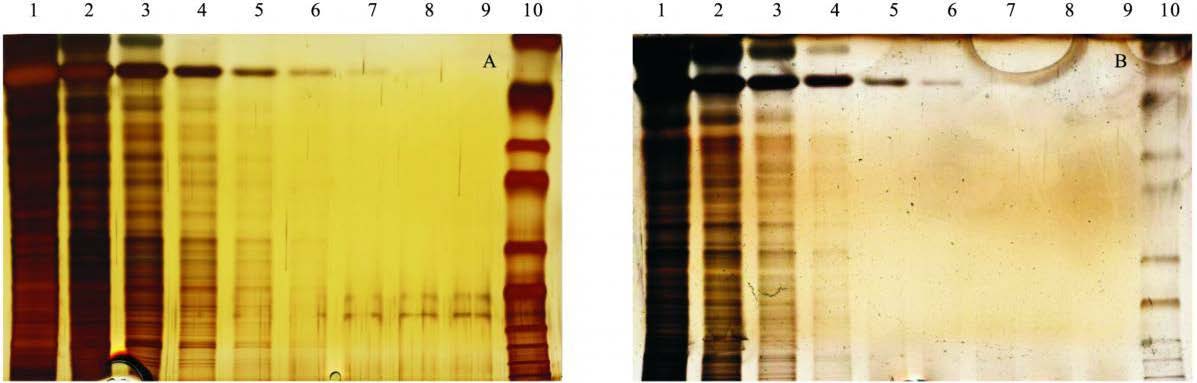
离子对银染染色可以看到上样5 /512μg(约0.01 μg)副溶血弧菌蛋白显现条带,其中一条小分子量条带甚至上样5 /8 192 μg (约0.000 6 μg)仍然可见,与染料染色相比灵敏度提高近百倍。特别是离子对银染复染时多出一条更小分子量条带,与直接银染相似(图 2A),进口染料试剂盒染色后再银染未出现该条带。
2.3 染料染色与银染的兼容性(图 2)使用离子对染色体系银染与直接银染效果几乎相同(图 2A) 。进口染料试剂盒染色后再银染,条带残缺模糊,染色过程中出现较多的黑色颗粒沉淀,染色背景不洁净。
|
注: A: 离子对银染体系染色; B: 进口银染试剂盒染色; 1~ 9: 泳道: 副溶血弧菌蛋白,第1泳道上样10 μg,以后依次稀释4 倍上样;第10 泳道: 蛋白质分子量标志; 离子对染色体系(A)菌体蛋白显现条带最低量为10 /1 024 μg(6泳道)。 图 2 2种染色体系对副溶血弧菌蛋白银染色效果比较 |
离子对染色体系银染试剂对容器无特殊要求,染料染色后的容器水冲洗干净即可进行银染复染。蛋白条带着色迅速而清晰,且可耐受较长时间显色。进口银染试剂盒对容器有要求,不能使用塑料染色盒,玻璃染色盒需要经过强酸浸泡。染色过程中必须轻缓震荡,否则很容易出现颗粒沉淀,使胶面出现花纹、斑点(图 2B)。显影控制较难,必须精准控制终点,时间稍长就会出现很厚背景。
3 讨 论实验中使用离子对染色体系的最大优点在于染料染色与银染的兼容性[3, 4],在银染过程中染料分子可以作为高效的银离子敏化剂,改善银离子的还原[4, 5],降低背景着色,从而增加银染的重现性和灵敏度。且该染色方案染料染色和银染技术巧妙结合,无需使用甲醛或戊二醛,而灵敏度较商品化试剂盒提高10倍以上,操作更加简化,凝胶着色均匀,条带清晰,重复性较好,更适合蛋白分离染色检测需要。
离子对染色体系染料染色灵敏度与国外同类进口试剂盒相近,染色进程可在70 min 内完成[6],离子对染料染色最低可使0.16 μg 细菌蛋白显出条带。与美国商品化染色试剂盒对比,最低显带菌体蛋白需要量接近,但背景干净,操作简便,而且显现的条带更清晰,优于国外进口产品。离子对染色法由于先行固定,蛋白扩散少,当进行银染复染时可显示更多的条带。与此体系对比的进口试剂盒为了降低染色被景,在染色前先行水洗凝胶去除SDS,导致部分小分子量蛋白扩散甚至丢失,低分子量条带边缘较模糊。且再行银染时由于小分子量带丢失,与直接银染(先行固定)有明显区别,而离子对体系复银染与直接银染效果几乎没有区别。
| [1] | Congw T,Hwang SY,Jin LT,et al. Sensitive fluorescent staining for proteomic analysis of proteins in 1-D and 2-D SDS-PAGE and its comparison with SYPRO Ruby by PMF[J].Electrophoresis,2008,29(21):4304-4315. |
| [2] | 夏其昌.蛋白质电泳技术指南[M].北京:化学工业出版社,2007:23-27. |
| [3] | Jin LT,Li XK,Cong wT,et al. Previsibles ilver staining of protein in electrophores is gels with mass spectrometry compatibility[J].Anal Biochem,2008,383(2):137-143. |
| [4] | Jin LT,Hwang SY,Yoo G S,et al. Amass spectrometry compatible silver staining method for protein incorporatinga new silver sensitizer in sodium dodecyl sulfate polyacrylamide electrophores is gels[J].Proteomics,2006,6(8):2334-2337. |
| [5] | Jin LT,Choi JK.Usefulness of visible dyes for the staining of protein or DNA in electrophoresis[J].Electrophoresis,2004,25(15):2429-2438. |
| [6] | Choi JK,Chae H Z,Hwang SY,et al. Fastvisible dyestaining of proteins in one and two dmiensional sodium dodecyl sulfate polyacryl amidegels compatible with matrix assisted laser desorption/ionization mass spectrometry[J].Electrophoresis,2004,25(7-8):1136-1141. |
| [7] | Jin LT,Hwang SY,Yoo G S,et al. Sensitive silver staining of protein in sodium dodecyl sulfate polyacrylamide gels using anazodyecal,concarboxylic acid,as as ilverionsensitizer[J].Electrophoresis,2004,25(15):2494-2500. |
 2011, Vol. 27
2011, Vol. 27
