2. 大连雅立峰生物制药有限公司;
3. 江苏延申生物科技股份有限公司;
4. 河南省长葛市疾病预防控制中心
自2009年4月25日WHO正式确认新型甲型H 1N 1流感暴发以来,该病在世界范围内迅速蔓延〔1〕。截至2010年1月10日,全球至少208个国家和地区报告有实验室确诊病例,其中包括至少13 554例死亡病例〔2〕。流感疫苗是应对甲型H 1N 1流感疫情最有效的"武器"〔3〕。为了解国产甲型H1N1流感病毒裂解疫苗的免疫原性与安全性,以指导人们安全有效地接种疫苗,本研究于2009年7-9月在河南省长葛市对2种国产甲型H 1N1流感病毒裂解疫苗进行了观察与评价。结果报告如下。
1 对象与方法 1.1 对象依照知情同意、自愿参加的原则,在长葛市选择年龄.3岁健康者748人,随机分为2组,每组按年龄分为3岁~、7岁~、12岁~、18岁~和60~75岁5个亚组。入选条件:身体健康,无先天性、遗传性和免疫缺陷性疾病史,无发热和接种禁忌症,本次接种前3个月内未接受过血液制品或季节性流感疫苗、1个月内未接受过其他研究药物或减毒活疫苗。
1.2 方法 1.2.1.疫苗分别选取江苏延申生物科技股份有限公司和大连雅立峰生物制药有限公司生产的新型甲型H 1N1流感裂解疫苗,2种疫苗均以WHO推荐的NYMCX.179A甲型H 1N1流感毒株制备而成,15μg剂型,规格为0.5 mL/支。疫苗成品经中国药品生物制品检定所注册检定,其质量符合甲型H 1N1流感病毒裂解疫苗的质量标准。甲、乙2种疫苗的批号分别为200907L01和H 1N120090701。
1.2.2 疫苗接种2组人群按随机、双盲原则分别接种2种疫苗,所有接种者接种前均签署知情同意书。疫苗使用前充分摇匀,在接种者上臂外侧三角肌附着处皮肤经75%酒精消毒,待皮肤微干后,应用2 mL无菌注射器肌肉注射试验疫苗;免疫程序均为第1针接种后,第21 d再接种1针;接种剂量均为15μg血凝素/剂。
1.2.3 免疫原性观察分别于第1针接种前(当日)、第1针接种后第21 d (21 d)、第2针接种后第21 d (42 d),采集静脉血5.0 mL于非抗凝管中,分离血清,每管血清量≥0.5 mL,于-20 ℃以下保存。采用微量血凝抑制(H I)试验检测病毒分型H I抗体滴度。抗体阳转率、保护率及疫苗免疫前后血清H I抗体几何平均滴度(geometric meantiter,GMT)增长倍数的判定参照欧盟标准〔4〕:18~60岁H I抗体阳转率≥40%,且保护率≥70%,GMT≥2.5;> 60岁H I抗体阳转率≥30%,且保护率≥60%,GMT≥2; 3~17岁比照18~60岁标准。
1.2.4 安全性观察每次疫苗接种后留观30 m in,记录局部和全身反应情况。接种后6、24、48、72 h,由被接种者依据自我症状和体征,填写《甲型H 1N1流感病毒裂解疫苗接种日记卡》;局部皮疹、红肿和硬结经医生测量后填写;不良反应强度分为轻、中、重度及危及生命4级,判定标准:1级:轻度,能感觉到症状或体征的存在,但很容易耐受,无需医疗;2级:中度,不适程度足以影响日常活动,不需或只需少量的医疗干预;3级:重度,明显限制日常活动,需要日常生活照顾,需要医疗,可能需要住院;4级:危及生命,极度限制日常活动,非常需要日常生活照顾,需要医疗和住院。
1.3 统计分析采用STATA 8.0进行随机化分组,采用Epi.Data 3.02双份录入数据,由2人分别独立完成,采用SAS 9.13软件进行统计分析,分析比较使用χ2检验及两独立样本秩和检验,检验水准α=0.05。
2 结果 2.1 基本情况第1针接种748人,平均年龄(30.91±23.93)岁,男性386人,女性362人,性别比为1.07:1;其中接种甲疫苗360人,接种乙疫苗388人,甲乙2组性别与年龄构成差异均无统计学意义(分别χ2=0.07,P=0.79;χ2=7.53,P=0.11)。第2针接种734人,平均年龄(30.99±23.99)岁,男性380人,女性354人,性别比为1.07:1;其中接种甲疫苗353人,接种乙疫苗381人,甲乙2组性别与年龄构成差异亦无统计学意义(分别χ2=0.07,P=0.80;χ2=7.13,P=0.13)。
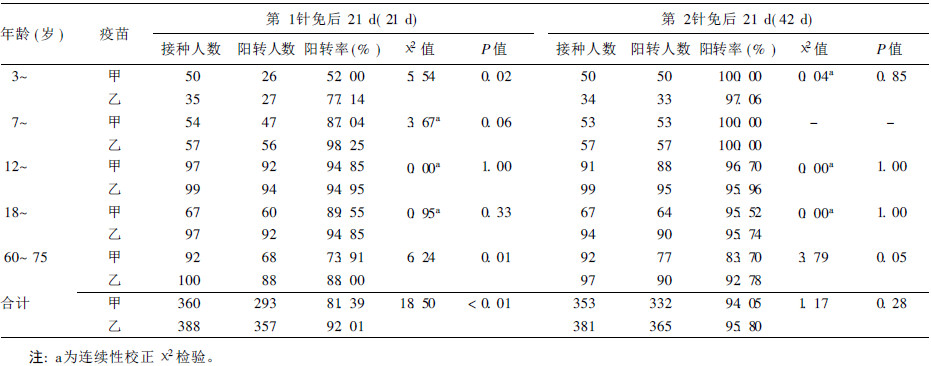
2.2 2种疫苗免疫原性比较 2.2.1 抗体阳转率比较(表 1)表 1可见,第1针接种后42 d时,各组抗体阳转率均高于21 d时的抗体阳转率。第1针接种后21 d时,3岁~和60~75岁组的乙疫苗抗体阳转率均明显高于甲疫苗抗体阳转率(P < 0.05);42 d时各组2种疫苗的抗体阳转率差异均无统计学意义(P > 0.05)。
| 表 1 不同年龄组2种疫苗抗体阳转率比较 |
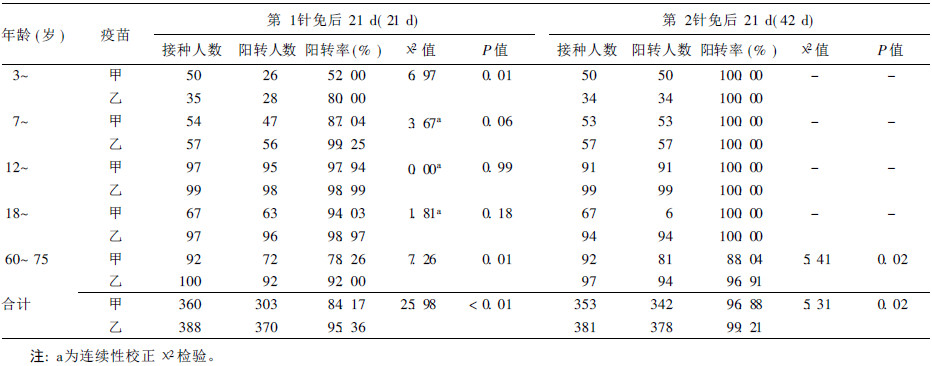
表 2可见,第1针接种后42 d,各组抗体保护率均高于21 d的抗体保护率;第1针接种后21 d和42 d,乙疫苗抗体保护率均高于甲疫苗(P < 0.05);第1针接种后21 d,3岁~和60~75岁组的乙疫苗抗体保护率均明显高于甲疫苗(P < 0.05);第1针接种后42 d,60~75岁组乙疫苗抗体保护率明显高于甲疫苗(P < 0.05),其余各年龄组差异无统计学意义(P > 0.05)。
| 表 2 不同年龄组2种疫苗抗体保护率比较 |
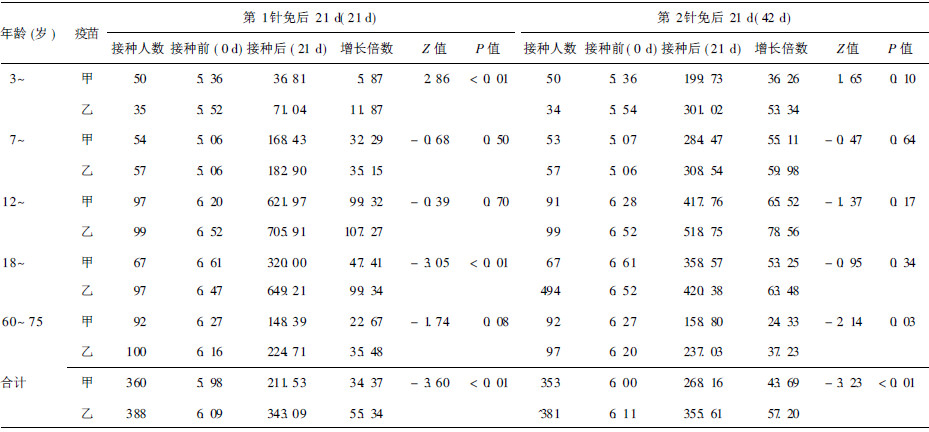
无论是免后21 d还是免后42 d,乙疫苗GMT均高于甲疫苗,且GMT增长倍数均明显高于甲疫苗。免后21 d各组观察对象GMT介于1:36.81~1:705.91,42 d各组观察对象GMT介于1:158.80~1:518.75。42 d GMT与21 d比较,3岁~、7岁~和60~75岁组对象普遍上升,12岁~组普遍下降,在18岁~组甲疫苗上升、乙疫苗下降。
| 表 3 抗体平均几何滴度(GMT, 1: )比较 |
第1针接种748人,仅1人于6 h出现轻度头痛,未经医学处理,症状于24 h内消失;疫苗接种后30 m in内,腋温增高91人,占12.17%,未经医学处理均自然恢复;其中1级发热反应(≤37.5 .)占94.51%,2级发热反应(≤38.5.)占5.49%;乙疫苗发热发生率(14.69%)明显高于甲疫苗(9.44%),差异有统计学意义(χ2=4.81,P=0.03)。第2针接种734人,疫苗接种后30 m in内,腋温增高25人,占3.41%,其中1级发热反应占96%,2级发热反应占4%;甲、乙2种疫苗发热发生率分别为4.53%和2.36%,差异无统计学意义(χ2=2.62,P=0.11)。所有被接种者均未发生其他局部或全身反应。
3 讨论疫苗是在流感大流行中保护人类最有效的方法之一。然而新型甲型H 1N1流感病毒包含有禽流感、猪流感和人流感3种流感病毒的核糖核酸基因片段〔5〕,从迄今尚不完整的可靠科学证据来看,季节性流感疫苗对防范甲型H1N1流感没有多大作用或毫无作用〔6〕。本研究所用疫苗由国际A(H 1N1)流感NYMC X-179A毒株制备而成,疫苗株与北美、欧洲和大洋洲分离的新型甲型H 1N1流感病毒在遗传和抗原性方面高度相似,可以产生特异性抗体,为人们提供有效防护。
本研究中,疫苗接种前各组受试对象性别、年龄均衡可比,排除了某些非处理因素对试验结果的影响。仅接种1针15μg血凝素/剂的甲疫苗并不能对3~6岁人群提供有效保护,但是接种第2针后抗体保护率达到100%。其余各指标也远远超过了欧盟标准〔4〕的要求,高于文献报道的A1、A3和B型等某些季节性流感疫苗〔7〕。接种2针的抗体阳转率、疫苗保护率均高于接种1针者。儿童(3~7岁组)和老年人群(60~75岁组)在接种第2针后可引起较强的免疫反应,而在青少年组(12~17岁组)和成年人群(18~64岁)则不引起免疫反应增强,这与季节性流感疫苗在健康儿童人群引起的免疫反应相一致〔8〕。无论是接种第1针还是第2针,甲疫苗的抗体阳转率、疫苗保护率及疫苗免疫前后血清H I抗体几何平均滴度(GMT)的增长倍数均低于乙疫苗,提示乙疫苗的免疫效果优于甲疫苗。甲乙2种疫苗在接种后未发生局部及全身严重不良反应,也未发生任何不良事件。虽然有一部分接种者接种后出现短暂性腋温升高现象,发生率同Feng-cai Zhu等报道〔9〕的新型甲型H 1N1流感疫苗不良反应发生率(12.0%)相接近,但属于正常免疫反应,均未经医学处理,多在6 h左右自然恢复,转归较好,提示甲乙2种疫苗应用于3岁以上健康人群后具有良好的安全性。
综上所述,甲、乙2种疫苗均是安全有效的,但乙疫苗的免疫效果优于甲疫苗。由于是新研制疫苗,故上述2种疫苗的免疫持久性及实际保护效果有待在人群中推广应用后进一步研究。
| 〔1〕 | 林磊, 童贻刚, 祝庆余.新甲型H1N1流感病毒及疫情分析[J].军事医学科学院院刊, 2009, 33(3):201-204. |
| 〔2〕 | World Health Organization.Global A lert and Response(GAR)Pandemic(H1N1)2009 update 83[EB/OL].[2010-01-15].http://www.who.int/csr/don/2010-01-15/en/index.html. |
| 〔3〕 | 曾光, 申涛.我国应对甲型H1N1流感的策略与展望[J]. 中国急救医学, 2009, 29(6):481-482. |
| 〔4〕 | Commission of the European Communities.Hamronization of require ments for influenza vaccine[S].Brussels:EEC document Ⅲ/3188/91-EN, 1991. |
| 〔5〕 | 李秀兰, 毛羽, 陈凤欣, 等.甲型H1N1流感的临床和流行病学特点分析及对防控工作的启示[J].中华医院管理杂志, 2009, 25(8):510-511. |
| 〔6〕 | World Health Organization.Vaccines for pandemic(H1N1)2009[EB/OL].[2010-01-15] http://www.who.int/csr/disease/swineflu/frequently_asked_questions/vaccine_preparedness/en/index.html. |
| 〔7〕 | 朱向军, 刘志田, 高志刚, 等.儿童型流感疫苗(防感灵)的安全性及免疫原性研究[J].中国公共卫生, 2002, 18(2):211-212. |
| 〔8〕 | Neuzil KM, Jack son LA, Nelson J, et al.Immunogenicity and reacto genicity of 1 versus 2 doses of trivalen tinact ivated influenza vaccine in vaccine-naive 5-8-year-old children[J].J Infect Dis, 2006, 194(8):1027-1029. |
| 〔9〕 | Zhu FC, Wang H, Fang HH, et al.A novel influenza A(H1N1)vaccine in various age groups[J].N Engl J Med, 2009, 361(25):2414-2423. |
 2011, Vol. 27
2011, Vol. 27