缺氧、缺血或某些药物等外源性刺激可诱导脑内c-jun,c-fos表达,而c-jun、c-fos被认为与细胞凋亡有关〔1, 2, 3〕。目前对缺氧的研究多采用短暂缺血以及缺氧-复氧模型,而较长时间暴露在低氧环境中对机体尤其是神经系统影响的相关研究报道较少。为探讨持续低氧对神经元细胞的影响及机制,于2009年11月采用Hoechst33258荧光染色、蛋白印迹等方法对体外培养大鼠海马神经元细胞缺氧后凋亡及c-jun和c-fos蛋白表达情况进行了观察。结果报告如下。
1 材料与方法 1.1 材料与试剂SD乳大鼠(第三军医大学实验动物中心);Dulbecco'smodifiedeaglemedia:nutrientmixtureF-12(DMEM/F12)、Neurobasal培养基,B27神经细胞生长添加剂,胎牛血清,胰蛋白酶(美国GIBCO公司);c-jun,c-fos一抗(美国SANTA公司);神经元特异性烯醇化酶(NSE)单克隆抗体(北京中杉金桥技术有限公司);Hoechst33258凋亡检测试剂盒(上海碧云天生物技术有限公司)。
1.2 海马神经元细胞原代培养主要方法及操作步骤参照文献〔4〕。种植培养基为DMEM/F12,含10%胎牛血清,0.5mmol/L谷氨酰胺,2%B27,100U/mL双抗。接种12h后,更换为含0.5mmol/L谷氨酰胺,2%B27,100U/mL双抗的Neurobasal培养基继续培养。
1.3 形态学观察及鉴定用倒置相差显微镜观察神经元形态变化及存活情况(3%台盼蓝浸染3min)。取培养第10d的6孔板中细胞进行神经元特异的NSE免疫组织化学染色,方法参考文献〔5〕,棕黄色为阳性,随机观察6个视野(200×)并计数。
1.4 缺氧模型建立海马神经元细胞培养10d后,分别设立对照组和缺氧组,对照组继续在37℃、5%CO2、95%空气的培养箱中培育,低氧组置于90%N2、5%O2、5%CO2混合气体的培养箱中培养2,6,12,24h进行指标测定。
1.5 Hoechst 33258凋亡检测按试剂盒说明书操作步骤进行。荧光倒置相差显微镜观察并拍照,计数随机视野中凋亡细胞所占比例。实验重复3次。
1.6 蛋白印迹检测将细胞裂解,十二烷基磺酸钠(SDS)聚丙烯酰胺凝胶电泳。取下凝胶,在转移缓冲液平衡10min,半干转移20min。转移结束后,取出聚偏二氟乙烯(PVDF)膜,依次置于5%脱脂奶粉、磷酸盐缓冲液、一抗、二抗和二氨基联苯胺(DAB)显色液中孵育,用计算机生物图像分析系统对干燥后的PVDF膜进行扫描,并用qualityone软件进行灰度值分析。
1.7 统计分析采用SPSS 13.0统计软件进行单因素方差分析。
2 结果 2.1 海马神经元细胞观察及鉴定光镜下观察第10d的神经细胞,胞浆和突起被染成棕黄色为NSE抗体表达阳性细胞,以6个视野中阳性神经元的数目占总细胞的比例为神经元纯度,经鉴定神经元的纯度为90%。
2.2 持续低氧对细胞凋亡影响( 图 1)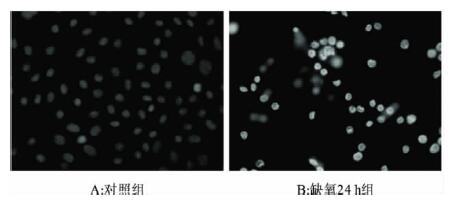 | 图 1 Hoechst 33258 染色原代培养海马神经元细胞 |
正常海马神经元细胞的细胞核呈蓝色,胞核较大,核荧光分布较匀(图 1A),而缺氧24h后的细胞核浓缩成致密的颗粒状,有分叶,呈现出凋亡核固缩形态(图 1B)。缺氧2,6,12和24h凋亡细胞所占比例分别为(23.79±3.43)%,(40.51±4.73)%,(56.24±4.30)%,(74.36±5.58)%,递增趋势明显(P<0.01)。
2.3 持续低氧对c-fos、c-jun 蛋白表达影响( 图 2) | 图 2 持续低氧对海马细胞c-fos、c-jun 蛋白表达影响 |
与对照组(低氧0h)比较,低氧2h蛋白含量开始升高,低氧6h达高峰,低氧12、24h水平降低,但仍略高于对照组(P<0.05)。
3 讨论研究发现,持续低氧可引起神经元细胞凋亡以及c-jun、c-fos蛋白表达上调。目前认为c-jun、c-fos表达增高与细胞凋亡相关〔6〕,推测有以下2种机制:(1)c-jun,c-fos蛋白通过亮氨酸拉链构成激活物蛋白1(AP-1),后者是一种核转录因子,与目标基因启动子特定序列结合调控相关基因转录,影响细胞的生长、增殖、分化、凋亡等〔7〕。(2)c-jun蛋白作为c-jun氨基末端激酶(JNK)信号通路的组成元件,其本身的增高可能引起JNK通路介导的相关蛋白活化,已证实神经细胞缺血再灌注损伤可导致细胞外信号调节激酶(ERK)及JNK通路激活,而后者与细胞凋亡有密切关系〔8〕。此外,c-jun、c-fos作为即早蛋白,其表达并非一过性改变,而是先增高后缓慢下降,24h时仍略高于正常对照。随着缺氧时间延长,凋亡、坏死细胞逐渐增多,剩余存活细胞表达c-jun、c-fos相对增加,提示可能具有一定的神经保护作用,与NessJM等〔9〕的研究结论相似。持续缺氧是个较长过程,c-jun、c-fos可能既介导细胞凋亡又对细胞进行保护。这2种相反的作用,可能与细胞对缺氧耐受的差异有关,但具体通过何种途径以及如何发挥作用,仍需进一步研究。
| 〔1〕 | Macaya A.Cell death in neonatal hypoxia-ischemia[J].Rev Neurol,2000,31(8):784-789. |
| 〔2〕 | 周珂,李庚山,余绍祖.脑缺血再灌注损伤时c-fos、c-jun的表达和细胞凋亡[J].卒中与神经疾病,2003(01):3-6. |
| 〔3〕 | Yuan Z,Gong S,Luo J,et al.Opposing roles for ATF2 and c-Fos in c-Jun-mediated neuronal apoptosis[J].Mol Cell Biol,2009,29 (9):2431-2442. |
| 〔4〕 | 王英,车宇,苗建亭,等.新生大鼠海马神经元原代培养方法的研究[J].细胞与分子免疫学杂志,2003,19(2):197-199. |
| 〔5〕 | 魏丽,彭瑞云,高亚兵,等.微波辐射对大鼠海马神经元损伤作用[J].中国公共卫生,2008,24(9):1103-1104. |
| 〔6〕 | Kumari SR,Alvarez-Gonzalez R.Expression of c-jun and c-fos in apoptotic cells after DNA damage[J].Cancer Invest,2000,18(8): 715-721. |
| 〔7〕 | Vesely PW,Staber PB,Hoefler G,et al.Translational regulation mechanisms of AP-1 proteins[J].Mutat Res,2009,682(1):7-12. |
| 〔8〕 | 郝慧琴,王蕴红.JNK转导通路在细胞凋亡中的作用[J].首都体育学院学报,2007,19(04):18-41. |
| 〔9〕 | Ness JM,Harvey CR,Washington JD,et al.Differential activation of c-fos and Caspase-3 in hippocampal neuron subpopulations following neonatal hypoxia-ischemia[J].J Neurosci Res,2008,86(5):1115-1124. |
 2010, Vol. 26
2010, Vol. 26

