2. 贵阳医学院
红色蚋(Simuliumrufibasis)是世界上较早发现的蚋科昆虫中的常见种,具有吸血特性,可叮食人血,能导致蚋病(simuliosis)和蚋热病〔1〕。红色蚋在中国分布广泛,在流行病学上具有重要意义。细胞色素氧化酶(cytochromeoxidase,CO)又称细胞色素氧化酶,是真核生物线粒体内膜和需氧菌细胞膜呼吸链上重要的终端氧化酶,由COI、COII、COIII等3个亚基组成,其基因是分子分类研究中应用较多的基因,目前对其他物种细胞色素氧化酶的研究较为深入〔2, 3〕,其中COI基因是稳定、可靠和应用范围广的非形态学昆虫分类特征基因〔4〕,为了观察红色蚋COI基因序列特征和蛋白质结构特点,为红色蚋的系统发育关系和DNA分类提供分子依据和基础性资料,本研究在前期研究〔5〕基础上,克隆其COI基因,测定其序列,结果报告如下。
1 材料与方法 1.1 材料 1.1.1 红色蚋与菌株红色蚋S.rufibasis,雄性成虫1只,2004年8月在湖北省利川市星斗山自然保护区采集其蛹,经隔离孵化培养育出成虫,随即用100%酒精固定。解剖茧和蛹皮,再将成虫尾端部分分离出来并用1%NaOH消化,4h后分离解剖成虫尾器;茧、蛹皮和成虫尾器制成玻片标本保存,成虫除尾器外保存于70%酒精中以备提取DNA;大肠埃希菌菌株DH5a(贵州省分子生物学重点实验室保存)。
1.1.2 主要试剂与仪器载体pMT18-T、TaqDNAPolymerase、T4DNALigase、dNTPs、5-溴-4氯-3吲哚-半乳糖苷(X-gal)、异丙基硫代半乳糖苷(IPTG)、蛋白酶K等(宝生物工程(大连)有限公司);限制性内切酶XbaI和SalI(华美生物工程有限公司);低熔点琼脂糖(美国Promega公司分装);UNIQ-10柱式PCR胶回收试剂盒(生工生物工程(上海)有限公司);DNAMarker200bpLadder〔天根生化科技(北京)有限公司〕;其他试剂均为国产分析纯。冷冻离心机(美国Beckman公司),PCR扩增仪(德国Eppendorf公司),成像及分析系统(美国UVP公司),多用途水浴恒温振荡器(江苏太仓市实验设备厂),蛋白核酸分析仪(美国Beckman公司)。
1.2 方法 1.2.1 基因组DNA 提取单只蚋置于1.5mL塑料离心管中,用无菌蒸馏水洗涤3次。按Marrelli等〔6〕方法略加改进提取单蚋基因组DNA,溶于100μL无菌蒸馏水中,4℃保存待用,用琼脂糖凝胶电泳检测其纯度及质量。
1.2.2 引物设计采用前期研究〔5〕设计的引物,上游引物W1在tRNA-酪氨酸(Tyr)基因3'端,下游引物W2在tRNA-亮氨酸(Leu)基因5'端,此对引物可扩增tRNA-Tyr基因和tRNA-Leu基因部分序列以及COI基因全长序列。W1:5'-CCCATAAATAGATTTACAATCT-3',W2:5'-TCATTGCACTAATCTGCCATAT-3'。
1.2.3 DH5α 感受态细胞制备参照文献 〔7〕进行,制备完后,添加终浓度7%的二甲基亚砜(DMSO),立即放入-70℃冰箱中冷冻贮存,临用时取出并在冰上解冻后即用。
1.2.4 PCR 扩增反应总体积30μL,其中,1×PCR缓冲液,2.5mmol/LMgCl2,0.2mmol/LdNTPs,引物W1和W2各0.2μmol/L,TaqDNA合成酶2.5U,模板DNA量为单蚋基因组DNA总量的1/50。反应条件:94℃预变性5min后,热循环94℃45s,55℃45s,72℃90s,共35个循环,最后72℃延伸10min。取5μLPCR产物与1/5体积的6×加样缓冲液混匀,用1%琼脂糖凝胶电泳检测扩增结果。
1.2.5 PCR 产物重组与转化PCR扩增产物经1%低熔点琼脂糖凝胶电泳分离后,于紫外灯下切割,用凝胶回收试剂盒回收纯化,以近6∶1摩尔比将PCR酶切产物和pMT-18T载体于16℃下连接过夜;连接产物经常规CaCl2方法转化大肠埃希菌DH5α感受态细胞,将转化菌液均匀涂布于含氨苄青霉素(10-4g/mL)的SOB/IPTG/X-gal琼脂糖平板上,倒置于37℃恒温培养箱中过夜培养,筛选转化子。
1.2.6 阳性克隆的筛选、验证与测序经蓝白斑筛选挑取转化平板上的单个白色菌落,接种于含氨苄青霉素的SOB液体培养基中,37℃于恒温摇床上振荡培养,小量抽提质粒DNA,同时进行XbaI和SalI双酶切和菌落PCR,PCR反应体系及扩增程序同前,将含阳性重组质粒的菌液送至Introvigen上海生物技术有限公司,以通用引物RV-M和M13-47进行序列测定,得到完整插入序列。
1.2.7 序列分析应用BLASTN同源比对工具将测序结果与GenBank中的核酸数据库进行同源性比对,筛选同源性最高的蚋科昆虫基因序列并利用美国国立生物技术信息中心(NCBI)上的ORFfinder软件分析该基因的完整读码框,再利用EMBL-EBI的UniProtKnowledgebase数据库和NCBIBLASTP程序对克隆基因序列编码的氨基酸序列在Ex-PASyProteomicsServer数据库上进行氨基酸残基数目、蛋白质相对分子质量(Mr)、理论等电点(pI)等参数进行分析,并搜索相应的蛋白质同源性和保守结构域。
2 结果 2.1 红色蚋总DNA 的提取与鉴定紫外分光光度计检测结果显示,260nm/280nm比值(纯度)为1.91,浓度为480μg/mL,可用作PCR模板。
2.2 PCR扩增(图 1)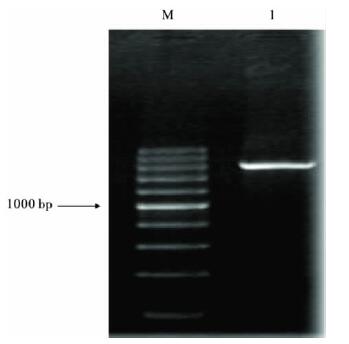 | 注: M: 200 bp DNA Ladder plus; 1: S. rufibasis。图 1 红色蚋COI 基因PCR 产物电泳图 |
扩增产物经1.0%琼脂糖凝胶电泳检测显示,在1600~1800bp处有一明显特异性扩增条带,大小约为1600bp,表明PCR扩增成功。
2.3 重组质粒酶切与菌落鉴定( 图 2,3)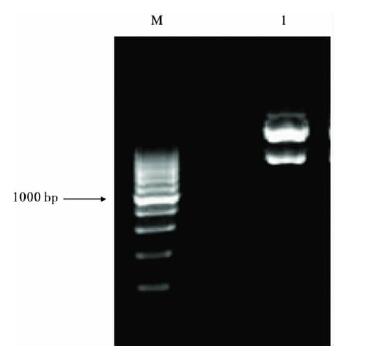 | 注: M: 200 bp DNA Ladder plus; 1: S. rufibasis。图 2 红色蚋COI 基因重组质粒Xba I 和Sal I 酶切电泳图像 |
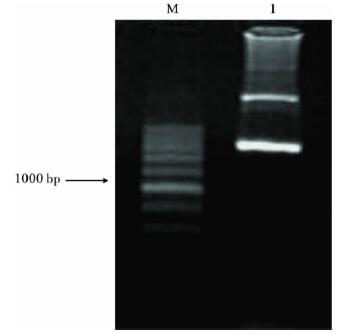 | 注: M: 200 bp DNA Ladder plus; 1: S. rufibasis。图 3 红色蚋COI 基因克隆PCR 验证结果电泳图 |
将双酶切质粒和菌落PCR产物经1.0%的琼脂糖凝胶电泳检测显示,酶切产物为2条特异性条带,1条大小在3.0kb左右,为空载体质粒DNA,另1条大小约1600~1800bp之间,与PCR产物大小相同,表明重组质粒含有目的基因片段;菌落PCR结果也显示,在1600bp与1800bp有一特异性DNA条带,大小与预期相符,可以确定阳性克隆子筛选成功。
2.4 基因片段测序与分析对阳性克隆插入片段进行核苷酸序列测定,结果显示,克隆得到的基因片段长1615bp,其中1~46bp为tRNA-Tyr基因部分序列,1595~1615bp为tRNA-Leu基因部分序列,53~1594bp为红色蚋COI基因序列,编码513个氨基酸残基,与预期结果一致。在NCBI上Blast比对分析表明,测序所得第53~1594bp之间DNA序列为红色蚋线粒体细胞色素氧化酶亚基I(COI)基因的基因序列,其完整序列包含有一个单独的开放阅读框(ORF),碱基组成A、T、C、G含量分别为28.60%、36.90%、17.76%、16.74%;G+C含量为34.5%,A+T为65.5%。该基因与GenBank中蚋科昆虫中蚋亚属中五条蚋和双齿蚋基因(登录号为:DQ534949和DQ534946)一致性达87%和89%。全长1615bp,COI基因编码区为53~1589bp,编码513个氨基酸。理论分子质量和等电点分别为56KDa和5.84。
2.6 基因序列分析将测序得到的DNA序列在NCBI数据库中利用BLASTN软件进行同源性检索,发现其与GenBank中登录号为DQ534946、DQ534949、AF425841、EZ419991等基因的同源性较高,均为86%以上。并且表明,本研究克隆的红色蚋COI基因长度在已知蚋科昆虫COI基因中为最长的序列之一,其它最长的序列也为本研究所得。比对范围均在84%以上;最大相似度均在85%以上。
蛋白质保守结构域分析表明,COI基因编码的氨基酸序列含有一个高度保守的细胞色素C氧化酶亚基I结构域,同时其编码蛋白与NCBI数据库中已发表的蚋科昆虫3个种类(双齿蚋S.bidentatum;五条蚋S.quinquestriatum;S.nigrimanum)的COI也具有较高的序列相似性。
3 讨论国外有研究〔8, 9, 10, 11〕将COI基因序列应用于蚋类研究,观察蚋亚属下的种间系统发育分析和种内系统地理学特征分析,而目前国内尚未见相关研究报道。上述研究均是应用COI基因部分序列,尚未见较长序列的相关报道,究其原因可能在于,克隆蚋类COI全基因序列的引物设计具有一定困难。本研究利用引物设计原理再进行改进,成功设计出了红色蚋COI基因克隆引物〔5〕。在此基础上,本次研究选取红色蚋湖北株,成功克隆其mtDNACOI基因,并成功对原核克隆载体质粒DNA进行了双酶切鉴定和克隆载体PCR鉴定。同源性比对显示,其与蚋科昆虫COI均有较高的同源性(>86%),其原因可能与线粒体基因组的高度保守性有关,也可能是它们有共同的进化起源,同时还可能为种类的遗传差异性导致。该基因在蚋科种内的差异较小,反映了种内的遗传稳定性,表明蚋科昆虫的COI基因序列保持了较高同源性,但又有少量稳定的科内差异性,是较为保守的序列,可将其作为该物种的基源。同时由其序列推导出的氨基酸序列相似性比较结果也显示,该基因的编码蛋白与其它蚋科昆虫COI家族蛋白具有较高同源性,这也为利用COI蛋白一级结构进行蚋科昆虫的分子系统学研究提供了基础性资料。
蚋科是双翅目中比较原始的一个类群,在形态学上具有明显的相似性,基础分类相对较难,迄今尚未建立一个既稳定又公认的分类系统。因此,从分子水平上寻找证据,为建立能够反映生物系谱的分类系统提供资料,应是一个有益的尝试。鉴于COI基因序列在分类学上的独特价值,对其进行深入研究,可为蚋科的系统发育重建提供重要资料。
| 〔1〕 | 陈汉彬,安继尧.中国黑蝇(双翅目,蚋科)[M].北京:科学出版社,2003:345-347. |
| 〔2〕 | 郭晓华,孙娜,张媛,等.基于细胞色素氧化酶I亚基基因的动物分子系统学概述[J].生物学教学,2009,34(10):8-10. |
| 〔3〕 | 张敏,曹天文,张睿,等.基于线粒体COⅠ基因的闪蛱蝶亚科系统发育关系研究[J].遗传学报,2007,34(9):812-823. |
| 〔4〕 | Hebert PD,Stoeckle MY,Zemlak TS,et a1.Identification of birds through DNA barcodes[J].Public Library of Science Biology,2004, 2(10):1657-1663. |
| 〔5〕 | 罗洪斌,杨明,陈汉彬.克隆医学昆虫蚋COI基因的引物设计方法探讨[J].湖北民族学院学报:医学版,2008,25(3):12-14. |
| 〔6〕 | Marrelli MT,Malafronte RS,Flores-Mendoza C,et al.Sequence analysis of the second internal transcribed spacer of ribosomal of ribosomal DNA in Anopheles oswaldoi(Diptera:Culicidae)[J].J Med Entomol,1999,36(6):679-684. |
| 〔7〕 | 萨姆布鲁克J,弗里奇E F,曼尼阿蒂斯T,等.分子克隆实验指南[M].3版.北京:科学出版社,2002:96-98. |
| 〔8〕 | St-Onge M,LaRue B,Charpentier G,et al.A molecular revision of the taxonomic status of mermithid parasites of black flies from Quebec(Canada)[J].J Invertebr Pathol,2008,98(3):299-306. |
| 〔9〕 | Joy D,Conn J.Molecular and morphological phylogenetic analysis of an insular radiation in pacific black flies(Simulium)[J].Syst Biol, 2001,50(1):18-38. |
| 〔10〕 | Pramual P,Kuvangkadilok C,Baimai V,et al.Phylogeography of the black fly Simulium tani(Diptera:Simuliidae)from Thailand as inferred from mtDNA sequences[J].Mol Ecol,2005,14(13):3989-4001. |
| 〔11〕 | Phayuhasena S,Colgan DJ,Kuvangkadilok C,et al.Phylogenetic relationships among the black fly species(Diptera:Simuliidae)of Thailand based on multiple gene sequences[J].Genetica,2010,138 (6):633-648. |
 2010, Vol. 26
2010, Vol. 26

 , 陈汉彬2
, 陈汉彬2