帕金森病(Park inson’s disease,PD)是一种常见的神经退行性疾病,其主要病理特征为黑质多巴胺能神经元损失和脑内出现特征性Lewy’s小体。研究发现,小胶质细胞介导的脑内炎症反应可能是导致PD发生的病因之一〔1, 2〕。脂多糖 (lipopoly saccharide,LPS)是革兰阴性细菌内毒素的有效成分,可导致小胶质细胞激活,释放炎性因子,从而导致多巴胺能神经元变性〔3, 4〕。多不饱和脂肪酸(polyun saturated fattyacids,PUFAs)是重要的膳食成分,研究发现摄入高剂量鱼油(n-3 PUFAs)与降低PD的风险有关〔5〕。本实验以SD大鼠为动物模型,观察n-3 PUFAs在LPS诱导的多巴胺能神经元损伤中的作用。
1 材料与方法 1.1 试剂与仪器LPS、阿扑吗啡(APO)(美国Sigma公司),n-3 PUFAs中二十碳五烯酸与二十二碳六烯酸占 60%,TH抗体(#2792)(美国Cell Signaling公司)。
1.2 实验动物健康雄性SD大鼠(第四军医大学实验动物中心)40只,体重180~220g,行为测试无异常,实验开始前常规饲料适应喂养7d。
1.3 分组与处理按体重随机分为对照组,LPS组,LPS+ 30%、60%鱼油组,每组10只。鱼油组喂食含鱼油基础饲料,分别含30%和60%鱼油,另外2组喂食基础饲料。喂食7d后,采用立体定向技术选择黑质致密部用微量注射器向右侧注射5μg/只LPS,给药速度1μL/min,注射完毕后留针5 min;缓慢退针缝合皮肤。对照组注射5μL生理盐水,注射后 14 d,进行行为学观察及酪氨酸羟化酶检测。
1.4 行为学观察经腹腔按体重0.5 mg/kg注射APO,记录大鼠30 min内旋转圈数及旋转方向。
1.5 酪氨酸羟化酶(TH)检测2%戊巴比妥钠麻醉大鼠,经左心室插管,4℃4%多聚甲醛400 mL灌注固定,断头,取脑,梯度脱水,冰冻切片(20μm)。免疫荧光法检测黑质TH表达,黑质多巴胺神经元计数,每只大鼠阅3张切片,荧光显微镜下认定结构,由第三者盲法于10%视野下计数TH阳性细胞数。
1.6 统计分析采用SPSS 12.0统计软件进行方差分析,以 P < 0.05为差异有统计学意义。
2 结 果 2.1 行为学观察对照组注射生理盐水后未出现明显行为学变化。LPS组大鼠在注射APO 5~10 min后开始出现转圈行为,伴有前肢抬举性震颤动作,大鼠身体向右侧(注射侧)曲成环状,头尾衔接,以右侧后肢为支点向右侧旋转。30min内,LPS组旋转(114±36)圈;30%,60%鱼油组平均旋转圈数分别为(42±22),(18±13)圈,明显低于LPS组(P < 0.05)。
2.2 中脑黑质TH变化(图 1-4)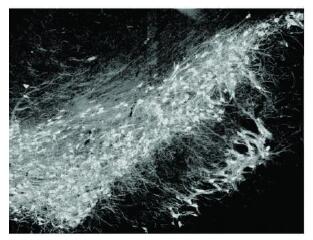 | 图 1 对照组可见大量TH+神经(10×) |
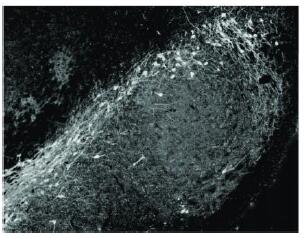 | 图 2 LPS组可见TH + 神经元明显减少(10×) |
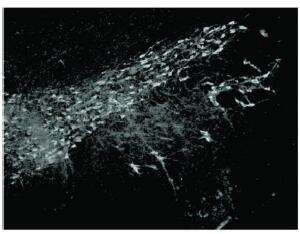 | 图 3 LPS+ 30%鱼油组(10×) |
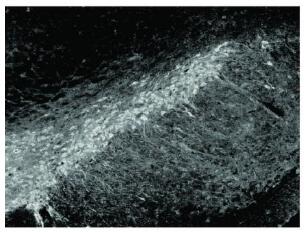 | 图 4 LPS+ 60%鱼油组(10×) |
LPS组TH阳性细胞数为(71.66±7.08)个,与对照组(174.33±16.95)比较明显减少,仅为对照组的41%;而30%,60%鱼油组TH阳性细胞数是对照组的89%和90%,分别为(156.5±7.86)和(157±17.81)个。
3 讨 论PD是一种神经系统退行性疾病,黑质多巴胺能神经元缺失、多巴胺减少是PD发生的主要原因。本研究结果表明,APO诱导后,对照组大鼠未出现明显的行为变化,LPS组大鼠出现旋转行为,并伴有明显前肢抬举性震颤,表明LPS定位注射导致了多巴胺能神经元的损伤,而鱼油组大鼠旋转圈数明显少于LPS组(P < 0.05),表明鱼油对于LPS所致大鼠多巴能神经元损伤具有一定保护作用。
研究表明,n-3 PUFAs对中枢神经系统疾病有防护作用,在灵长类帕金森动物模型中,二十二碳六烯酸(DHA)对多巴胺有关的运动功能有直接作用〔6〕。在神经毒性诱导的 PD动物模型中,膳食补充n-3 PUFAs能够抑制黑质TH阳性神经元的减少,产生神经保护作用〔7〕。这可能与n-3 PUFAs能够通过多种方式影响炎症反应,从而抑制炎症及免疫的作用有关。
| 〔1〕 | Herrera A J,Tomas M,Venero JL,et al. Inflammatory process as a determinant factor for the degeneration of substantia nigra dopaminergic neurons[J].J Neurol Transm,2005,112(1):111-119. |
| 〔2〕 | McGeer PL,Yasojmia K,McGeer EG.Inflammation in Park in sons disease[J].Adv Neurol, 2001,86:83-89. |
| 〔3〕 | Liu B,Du L,Hong JS.Naloxone protectsrat dopaminergic neurons againstin flammatory damage through inhibition of microglia activation and superoxide generation[J].J Pharmacol Exp Ther,2000,293(2):607-617. |
| 〔4〕 | Gao HM,Hong JS,Zhang WQ,et al. Microglia activation mediated delayed and progressive degeneration of rat nigral dopam inergic neurons:relevance to Parkinsons disease[J].J Neurochem,2002,81(6):1285-1297. |
| 〔5〕 | DeLau LM,Bornebroek M,Witteman JC,et al. Dietary fatty acids and the risk of Parkinson disease:the Rotterdam study[J].Neurology,2005,64:2040-2045. |
| 〔6〕 | Samadi P,Gregoire L,Rouillard C.Docosahexaenoic acid reduces levodopa induced dyskinesias in 1 methyl 4 phenyl 1,2,3,6 tetrahydropyridine monkeys[J].Ann Neurol, 2006,59:282-288. |
| 〔7〕 | Bousquet M,Saint Pierre M,Julien C.Beneficial effects of dietaryomega 3 polyun saturated fatty acid on toxininduced neuronal degeneration in an animal model of Parkinsons disease[J].The Federation of American Societies for Expermiental Biology Journal, 2008,22(4):1213-1225. |
 2010, Vol. 26
2010, Vol. 26

