隐孢子虫感染引起的隐孢子虫病(cryp to sporidiosis)是一种全球性以腹泻为主要症状的人畜共患寄生虫病〔1, 2〕。疫苗是防治该病的主要手段之一。研究表明,微小隐孢子虫表面抗原CP23、CP15/60、CP15等以其较强的免疫原性,是免疫诊断、免疫预防及免疫治疗的靶抗原,其中C P23基因编码的蛋白是宿主免疫识别的主要蛋白,能够刺激机体产生强烈的免疫反应,并且能够在原核和真核中表达〔3, 4, 5〕。本课题前期研究中成功构建了微小隐孢子虫CP23基因的真核表达载体 pcDNA3.0和pcDNA 3.0-23重组质粒〔6〕,为了进一步评价 pcDNA 3.0-23重组质粒作为微小隐孢子虫核酸疫苗的免疫效果,我们通过肌肉注射和滴鼻2种途径对BALB/c小鼠进行pcDNA 3.0-23重组质粒免疫,观察比较机体的免疫反应及不同免疫途径的影响。结果报告如下。
1 材料与方法 1.1 材料(1)实验动物:BALB/c小鼠80只(山东大学医学院实验动物中心),雌雄各半,SPF级,6~8周龄,体重18~ 22 g。(2)虫种、质粒与菌株:微小隐孢子虫卵囊及真核质粒 pcDNA3.0(山东省寄生虫病防治研究所惠赠);大肠埃希菌 DH5α(本实验室保存)。(3)主要试剂及仪器:异硫氰酸荧光素(FITC)标记与藻红蛋白(PE)标记的小鼠IgG2a及其同型对照(美国BD公司);1640培养液(上海克隆生物高技术公司产品);小牛血清(上海复旦天呈公司);碱性磷酸酶(AP)标记的羊抗鼠IgG结合物及兔抗大鼠IgG结合物,碱性磷酸酶(AP)标记的大鼠抗小鼠γ干扰素(IFN-γ)单抗(美国Sigma公司);MK3型酶标仪(芬兰Labsystem s公司);FC500型流式细胞仪(美国Beckm an Cou lter公司)。
1.2 方法 1.2.1 pcDNA3.0-23重组质粒扩增按照文献〔6〕构建 pcDNA3.0-23重组质粒,经验证构建正确后,大量扩增,提取足够量,调节浓度为100 g/L,备动物免疫用。
1.2.2 免疫接种BALB/c小鼠80只,随机分为4组,每组20只。(1)对照组:肌注磷酸缓冲液(PBS)100 L/只;(2) pcDNA3.0-23肌肉注射组(肌注组):大腿肌肉注射重组质粒100 L/只;(3) pcDNA3.0-23滴鼻组(滴鼻组):鼻腔滴注重组质粒100 L/只;(4) pcDNA3.0肌注组(空质粒组):大腿肌肉注射pcDNA3.0 100μL/只。每隔2周免疫1次,共免疫3次,末次接种量均加倍。每只小鼠在每次接种前24 h均用0.25%的布比卡因100μL预处理。每次免疫前剪尾取血,最后1次免疫2周后,75%的酒精消毒,摘眼球取血,收集细胞悬液,用于检测抗体及细胞因子。
1.2.3 特异性抗CP23抗体检测采用间接ELISA法检测免疫小鼠血清中特异性抗体,包被抗原为大肠埃希菌表达的重组CP23蛋白。用1%小牛血清(BSA)封闭,不同稀释度各组免疫鼠血清、正常鼠血清为一抗,羊抗鼠IgG-AP结合物为二抗,对硝基苯基磷酸钠(pNPP)底物显色,酶标仪测吸光度(A405值);检测孔A405≥2.1阴性对照(正常鼠血清)孔A405者判为阳性,计算血清IgG抗体滴度,动态检测免疫小鼠特异性抗CP23抗体。
1.2.4 脾脏T细胞CD4+、CD8+亚群检测末次免疫后2周,随机取各组BALB/c小鼠各4只,无菌取脾,制备脾细胞悬液,调整细胞数至5×106/mL,分别加入FITC-CD3/PE- CD4和FITC-CD3/PE-CD8单抗,混匀后室温放置30 min,用流式细胞仪检测并计算T细胞亚群CD4+、CD8+和CD4+/ CD8+的百分率。
1.2.5 细胞因子IFN-γ的检测将细胞悬液浓度调至6.4×107/mL,分别滴入96孔无菌细胞培养板中,每孔0.2 mL,培养3 d后,收集上清。取培养液上清包被96孔反应板,常规ELISA法检测IFN-γ。
1.2.6 攻击感染第3次免疫2周后,将各组剩余BALB/c小鼠计60只(各组15只),分别灌胃接种1×106个卵囊,于接种第3 d开始收集小鼠粪便并称重,用简化的不连续蔗糖密度梯度离心法提取、纯化粪便中的卵囊,检测卵囊排出情况,计算平均每克粪便中卵囊数(EPG)。
1.3 统计分析采用SPSS 13.0软件进行统计分析,采用单因素方差分析。
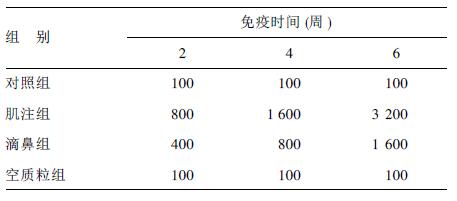
2 结 果 2.1 IgG抗体滴度比较(表 1)| 表 1 3次免疫后小鼠血清中IgG抗体平均几何滴度(GMRT) |
肌注组与滴鼻组小鼠血清 IgG抗体平均几何滴度均随免疫次数增多而明显增高,高于对照组及空质粒组(P < 0.05);肌注组IgG抗体滴度升高幅度大于滴鼻组,与对照组比较,差异有统计学意义(P < 0.05)。
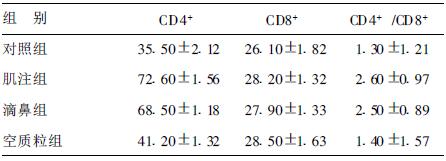
2.2 T淋巴细胞百分率比较(表 2)| 表 2 pcDNA3.0- 23免疫小鼠脾脏淋巴细胞 含量比较(x±s,%) |
第3次免疫后2周,肌注组与滴鼻组小鼠脾细胞CD4+、CD4+/CD8+比值明显高于对照组及空质粒组(P < 0.05),但肌注组与滴鼻组差异,以及各组间CD8+T细胞差异均无统计学意义(P > 0.05)。
2.3 细胞因子滴度比较单因素方差分析结果表明,肌注组和滴鼻组的IFN-γ平均几何滴度明显高于对照组及空质粒组,差异有统计学意义(P < 0.05),肌注组IFN-γ平均几何滴度为52,滴鼻组为48,2组间差异无统计学意义(P > 0.05)。
2.4 攻击感染后粪便卵囊比较(图 1)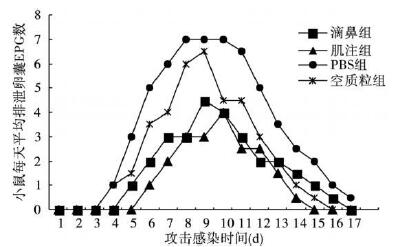 | 图 1 隐孢子虫攻击感染后各组小鼠卵囊排泄数及其排泄时间比较 |
用微小隐孢子虫卵囊攻击感染后17 d中,肌注组及滴鼻组小鼠平均每克粪便中卵囊数(EPG)始终低于对照组和空质粒组,并且初始排卵囊时间延长至感染后第4~6 d,卵囊持续排出时间仅持续9~ 14 d。与对照组及空质粒组比较,卵囊排泄数量减少了 40%~60%,初始排卵囊时间延迟2 d;卵囊持续排出时间缩短5 d,差异均有统计学意义(F=3.6,P < 0.05)。肌注组和滴鼻组间差异无统计学意义(P > 0.05)。
3 讨 论DNA疫苗是近几年应用分子生物学等新技术研制的一种新型疫苗,它的出现为防治人类寄生虫感染带来了新希望。已经有很多研究者对各种病原生物的DNA疫苗进行了研究〔7, 8〕,编码子孢子表面抗原的基因被公认为疫苗的候选基因,已发现抗CP23蛋白的单克隆抗体可抑制微小隐孢子虫感染,重组的CP23蛋白也可诱导产生保护性抗体,是诱导保护性免疫力的主要成分。
检验基因疫苗免疫效果的关键是其能否有效刺激机体产生免疫反应。本研究用构建的真核表达质粒免疫小鼠,结果表明,pcDNA3.0-23重组质粒作为基因疫苗,可产生较好的细胞及体液免疫反应。该疫苗以引起CD4+细胞升高为主,而CD8+T细胞无明显增殖,提示CD4+T细胞在抗隐孢子虫感染中有重要作用。有研究表明,将感染了隐孢子虫小鼠的 CD4+T细胞移植到IFN-γ和白介素-12(IL-12)缺陷的小鼠体内,可使小鼠排出卵囊明显减少〔9〕。本实验结果也证明,2种不同免疫途径的小鼠产生的IFN-γ滴度较2个对照组明显增高,抗CP23特异性抗体滴度随免疫次数增加而升高。攻击感染实验结果表明,2个免疫组小鼠排出卵囊的量均明显减少,且排出时间缩短。不同免疫途径观察结果表明,肌肉注射pcDNA3.0-23重组质粒,可产生较好的细胞和体液免疫反应;鼻粘膜免疫产生的细胞免疫和肌肉注射免疫相近,但特异性抗体滴度水平略弱于肌肉注射,这可能是免疫部位不同、质粒吸收量不同以及抗原提呈细胞不同等原因引起。采取多途径联合免疫途径是否可提高免疫效果,有待进一步研究。
| 〔1〕 | 黄民主,关岚,谢梅芝,等.长沙市某戒毒所男性吸毒人员中隐孢子虫感染状况的研究[J].中国公共卫生,2003,19(3):301-303. |
| 〔2〕 | Getaneh A,Medhin G,Shmielis T.Cryp tosporidium and Strongy loides stercora lisinfections among people with and without HIV in fection and efficiency of diagnostic methods for Strongy loides in Yirgalem Hospital, southern Ethiopia[J].BMC Res Notes,2010,3(1):90. |
| 〔3〕 | 何宏轩,张西臣,欧阳红生,等.微小隐孢子虫CP23基因真核表达载体的构建及表达[J].寄生虫与医学昆虫学报,2003,10(1):16-20. |
| 〔4〕 | 宰德富,张佃波,魏庆宽,等.微小隐孢子虫表面抗原CP23基因的克隆及表达[J].中国病原生物学杂志,2006,1(3):193-196. |
| 〔5〕 | 何宏轩,张西臣,欧阳红生,等.微小隐孢子虫子孢子表面抗原CP23融合蛋白在大肠杆菌的表达[J].中国人兽共患病杂志,2003,19(3):52-54. |
| 〔6〕 | 张玉梅,李波清,柏雪莲,等.微小隐孢子虫CP23基因真核表达载体pcDNA3.0-23的构建及鉴定[J].中国病原生物学杂志,2009,4(5):347-349. |
| 〔7〕 | Fu YH,He JS,Zheng XX,et al. Intranasal vaccination with a helper dependent adenoviral vector enhances transgene specific immunere sponses in BALB/c mice[J].Biochemical and Biophysical Research Communications,2010,391(1):857-861. |
| 〔8〕 | Watts AM,Kennedy RC.DNA vaccination strategies against infectious diseases[J].Vaccine,1999,29(8):1149-1163. |
| 〔9〕 | Tessema TS,Dauber E,Petry F.Adoptive transfer of protective mimunity from Cryptosporidium parvum infected in terferon gamm a and in terleuk in 12 deficient mice to naive recipients[J].Vaccine,2009,27(47):6575-6581. |
 2010, Vol. 26
2010, Vol. 26