8-羟基喹啉(8-hydro xyquinoline)作为一种重要工业原料,广泛存在于工业废水等水体中,对水生生物的生存具有潜在危害〔1〕。因此,检测水体中的8-羟基喹啉指标具有重要意义。已知鱼类的胚胎期和仔鱼期是整个生活史中对各种药物最为敏感时期。因此,可以利用其胚胎期和仔鱼期的敏感性来评价多种化合物及各种环境的毒性影响〔2, 3〕。本研究以大鳞副泥鳅为试验对象,探讨8-羟基喹啉对其胚胎及仔鱼毒性影响,为制定8-羟基喹啉水卫生标准及渔业用水水质标准提供科学依据。
1 材料与方法 1.1 材料大鳞副泥鳅(P.dabryanus)(河南省新乡市某农贸市场),体重26~30g,体长13~16cm,健康,性成熟个体。实验用水为自来水(阳光下曝晒3 d,同时用增氧机增氧)。8 -羟基喹啉(C9H7NO)(北京化工厂),分析纯。
1.2 受精卵制备参照文献〔4〕制备大鳞副泥鳅受精卵。
1.3 实验分组及处理实验共分6组,分别为对照组,8-羟基喹啉1.00×10-4(约1/4 LC50 24 h),5.00×10-5,2.50× 10-5,1.25×10-5,6.25×10-6 mol/L组,每组设3个平行样。(1)胚胎实验:取发育正常卵100枚,放入直径12 cm的培养皿,分别于胚胎发育的胚盘隆起期、原肠胚中期、神经胚期、尾芽期(大鳞副泥鳅胚胎发育分期),参照文献〔4, 5〕,加入含有不同浓度的8-羟基喹啉溶液100 mL,直至孵化出仔鱼,每日更换溶液,及时剔除死亡个体,利用解剖镜连续观察其发育状况。(2)仔鱼实验:取体长相近、健康状况良好的仔鱼,每皿 20尾;于仔鱼孵出期,至孵化出仔鱼后96h给予8-羟基喹啉,每日更换溶液,清除死亡个体。观察指标包括胚胎孵化率及畸形率(如死亡个体同时存在畸形,则计入死亡)、仔鱼的死亡率、体长、外部形态特征及行为反应〔6, 7〕等,并计算出仔鱼的半数致死浓度(LC50)、安全浓度〔8, 9, 10〕。
1.4 统计分析采用SPSS 16.0软件进行单因素方差分析,用最小显著差数法进行多重比较。
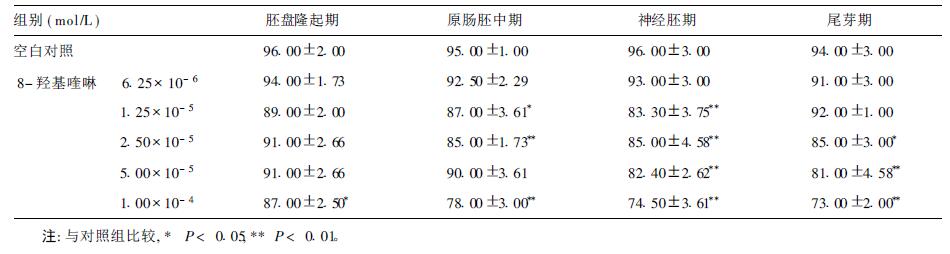
2 结 果 2.1 大鳞副泥鳅胚胎孵化率(表 1)| 表 1 8- 羟基喹啉对大鳞副泥鳅胚胎孵化率影响(%,x±s) |
在胚盘隆起期给予8-羟基喹啉,1.00×10-4 mol/L组胚胎孵化率明显低于对照组 (P < 0.05)。在神经胚期给予8-羟基喹啉,除6.25×10-6 mol/L组外,其余各组胚胎孵化率均明显低于对照组。
2.2 8-羟基喹啉对大鳞副泥鳅胚胎畸形率影响(表 2)| 表 2 8- 羟基喹啉对大鳞副泥鳅胚胎畸形率的影响(%,x±s) |
与对照组比较,随着8-羟基喹啉的浓度增加,4个不同时期处理组中胚胎畸形率均有明显增加。4个不同处理时期的致畸半数有效浓度,分别为5.47×10-5,3.20×10-5,2.55×10-5,4.17×10-5 mol/L。原肠胚中期、神经胚期时给予8-羟基喹啉,致畸作用更明显。
2.3 8-羟基喹啉对大鳞副泥鳅仔鱼影响仔鱼孵出后96 h内,与对照组比较,各处理组仔鱼死亡率明显升高(P <0.05)。随着8-羟基喹啉浓度增加,仔鱼死亡率逐渐升高,呈剂量-效应关系。8-羟基喹啉对大鳞副泥鳅仔鱼24,48,96 h LC50分别为3.96×10-5,1.66×10-5,1.10×10-5 mol/L。当8-羟基喹啉浓度增加至5.00×10-5mol/L时,大鳞副泥鳅仔鱼体长受到明显抑制。8-羟基喹啉安全浓度为8.72×10-7 mol/L。
3 讨 论在8-羟基喹啉处理大鳞副泥鳅胚胎过程中,如以孵化率为指标,只有在胚盘隆起期处理时,对胚胎毒性影响最差,其余各时期影响较明显。分析原因可能与卵膜的保护作用有关,胚胎周围卵膜有选择透过性及对毒物的天然屏蔽作用。以畸形率为指标,发现各时期给予8-羟基喹啉均对胚胎有致畸作用,尤其在原肠胚中期、神经胚期,1.00×10-4 mol/L组致畸率高达75%和72%。原因可能是这2个时期恰处在胚胎高度分化期,当高度分化胚胎的某部分发生异常变化后,会导致将来发育的个体某些组织或器官异常,形成畸形个体。此外,比较大鳞副泥鳅胚胎及仔鱼的毒性试验结果发现,仔鱼在处理96h时,5.00×10-5 mol/L组死亡率就已达到100%。表明大鳞副泥鳅仔鱼对8-羟基喹啉的敏感性比胚胎时期稍高,可能与卵膜的保护作用有关。
目前,鱼类毒性实验〔11, 12, 13〕是监测水环境污染物毒性影响的一种简便易行方法,且胚胎是反映环境中有害因素影响的敏感生物标志物之一。但是,有毒物质对胚胎毒性的作用机制错综复杂。8-羟基喹啉对大鳞副泥鳅胚胎、仔鱼的毒性机制以及体内代谢变化等有待进一步的探讨。
| 〔1〕 | 江敏,李咏梅,顾国维.含氮杂环化合物对水生生物的毒性作用研究[J].环境科学学报,2005,25(9):1253-1258. |
| 〔2〕 | Duan ZH,Zhu L,Gong ZY.Bioaccum ulation and toxicity test of diethylstilbestrol to zebrafish(Daniorerio)embryo[J].Environ-mental Science,2009,37(2):522-526. |
| 〔3〕 | Chen Z,Zhu L,Yao K,et al.Interaction between calcium and lead affects the toxicity to embryo of zebrafish(Daniorerio)[J].Environmental Science,2009,30(4):1205-1209. |
| 〔4〕 | 杜启艳,南平,燕帅国,等.豫北地区大鳞副泥鳅胚胎发育的观察[J].河南师范大学学报:自然科学版,2007,35(2):146–149. |
| 〔5〕 | 张恒远.大鳞副泥鳅胚胎发育观察[J].淡水渔业,2001,31(5):20-21. |
| 〔6〕 | Wang JJ,Xu C,Tu Y J,et al. Expermiental research and application of zebrafish and embryos in toxicology[J].Asian Journal of Ecotoxicology,2007,2(2):124-135. |
| 〔7〕 | Braunbeck T,Lammer E.Fishembryo toxicity assays[S].D essau:Gemran Federal Environment Agency,2006,14-48. |
| 〔8〕 | 高红霞,闫红,高铁利,等.污灌土壤中有机污染物遗传毒性检测[J],中国公共卫生,2008,24(10):1250-1251. |
| 〔9〕 | 付保荣,曹向宇,惠秀娟,等.杀菌剂粉唑醇遗传毒性试验研究[J],中国公共卫生,2008,24(9):1140-1141. |
| 〔10〕 | 李梓民,何爱桃,吴成秋,等.苯致小鼠胚胎肢芽发育毒作用[J],中国公共卫生,2008,24(4):458-459. |
| 〔11〕 | Kammann U,Vobach M,Wosniok W.Toxic effects of brominated indoles and phenols on zebrafish embryos[J].Arch Environ Contam Toxicol, 2006,51:97-102. |
| 〔12〕 | Lin JQ,Wang XH,Zhong JX,et al. Evaluation of using fish embryototest the toxicity of sewage treatments[J].Journal of O ceanography in Taiwan Strait,2008,27(3):329-333. |
| 〔13〕 | Li Y,Wang M.Toxicity and teratogenic effects of bu sulfan in early developing embryo and larva of zebrafish(D aniorerio)[J].Ecological Science,2008,27(5):368-375. |
 2010, Vol. 26
2010, Vol. 26