微波是高频电磁波,广泛应用于科研、医疗、工农业生产等领域。微波作用于生物体的生物效应备受关注。神经系统是微波辐射最为敏感的靶部位之一。突触是神经元间信息传递通路,神经递质是突触传导化学信息的媒介分子。突触结构和功能变化可以引起神经信息加工能力的改变,最终影响机体综合能力正常发挥。突触体保持突触前囊(轴突末梢)、突触间隙和突触后膜的完整结构。本实验通过探讨微波辐射对大鼠大脑皮质突触体特性以及神经递质释放的影响,为揭示微波辐射致脑结构和功能损伤机制提供科学依据。
1 材料与方法 1.1 仪器和试剂Philip-CM 120透射电镜(日本飞利浦公司);ESP 300电子自旋共振仪(德国Bruker公司);高效液相色谱仪(美国Hp公司)。Fluo-3-AM、谷氨酸(Glu)、甘氨酸(Gly)、天冬氨酸(Asp)、γ-氨基丁酸(GABA)和毒扁豆碱 (美国Sigma公司);马来酰亚胺(美国Aldrich公司)。
1.2 实验动物二级雄性Wistar大鼠20只(军事医学科学院实验动物中心),体重(180 ± 20) g。统一饲养,室内温度 21~23℃,相对湿度60%。
1.3 突触体制备采用蔗糖梯度离心法制备突触体〔1〕:取正常大鼠脑组织,分离大脑皮质,按1:100(W:V)加入0.32 mol/L蔗糖匀浆,1 500 r/min离心10 min,将上清液覆加于 1.5 mL 1.2 mol/L蔗糖表面;25 000 r/min离心25 min,收集中间带,用0.32 mol/L蔗糖稀释3~3.5倍后,覆加于1.5 mL 0.8 mol/L蔗糖表面,25 000 r/min离心15 min,将离心管底部突触体,悬浮于生理盐水缓冲液中,4℃保存。用前37℃孵育2 h。
1.4 实验分组与处理制备好突触体随机分为对照组、30,50 mW/cm2微波辐射组。每组5个样本。采用军事医学科学院自建的微波模拟源进行辐射。将突触体接种于直径 35mm培养皿中,放于辐射台上辐射。平均功率密度为30和 50 mW/cm2,辐射时间为5 min。对照组置于辐射台上5 min,不给予辐射。
1.5 突触体内Ca2+浓度检测〔2〕辐射后即刻10 000 r/min离心10 min,弃上清;20 mmol/L 4-羟乙基哌嗪乙磺酸 (HEPES)缓冲液洗涤2~3次,10 000 r/min离心10 min;用 Fluo-3-AM (终浓度为5 μmol/mL)于37℃避光孵育 0.5~1 h;采用流式细胞仪进行检测。
1.6 突触体膜蛋白流动性检测微波辐射后取突触体悬液,加入适量膜蛋白自旋标记物马来酰亚胺,0.2 mol/L,37℃孵育4 h;0.1 mol/L磷酸盐缓冲液洗涤,直到洗涤缓冲液中无自旋标记物信号为止;离心,沉淀置于样品腔中,进行电子自旋共振测试。参照文献〔3〕计算膜蛋白强弱固定化比值 (S/W)及旋转相关时间(τc ):S/W=hs/hw ,τc=2.756 × 10-10 ×△H0 × ﹛〔h (0)/h (-1)〕1/2-〔h (0)/h (1)〕1/2 ﹜。
1.7 突触体氨基酸递质释放检测突触体辐射后,37℃孵育 0.5 h,10 000 r/min离心5 min,取上清,样品处理参照文献〔4〕进行。用高效液相色谱法检测神经递质,100 μL衍生试剂内加入20 μL样品,振荡2 min,加样20 μL。测得氨基酸所占峰面积(A样)。根据标准品峰面积(A标)和浓度(C标)比,计算出被测氨基酸浓度(C样):C样(mg/ml)=C标× A样/A标,突触体氨基酸递质释放量=上清液容积(mL)× C样(mg/mL)= 1 × C标× A样/A标。
1.8 突触体乙酰胆碱(Ach)检测〔5〕突触体辐射后,37℃孵育0.5 h,10 000 r/min离心5 min,取上清0.8 mL,加蒸馏水1.4 mL混匀,加1.54 mmol/L毒扁豆碱0.2 mL,缓慢滴加 1.84 mol/L三氯乙酸0.8 mL,充分混匀,3 000 r/min离心15 min,取上清液采用碱性羟胺比色法测定,计算方法:Ach (μg/g)=(测定管A-对照管A)/(标准管A-空白管A)× (3.2/0.24)× 50。
1.9 统计分析采用SAS软件进行单因素方差分析。
2 结 果 2.1 大脑皮质突触体膜蛋白流动性变化30 mW/cm2微波辐射后突触体膜蛋白强弱固定化比为(0.278 ± 0.022),明显高于对照组(0.237 ± 0.010)(P < 0.05),表明微波辐射后突触体膜蛋白运动加快,流动性升高。
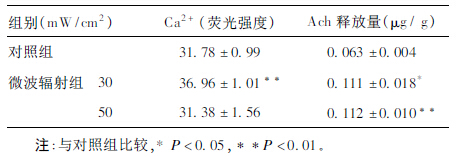
2.2 突触体内Ca2+浓度和Ach释放量变化(表 1)| 表 1 不同组别大鼠突触体内Ca2+ 浓度及Ach 释放量( x± s,n = 5) |
30 mW/cm2微波辐射后突触体内Ca2+浓度为(36.96 ± 1.01),与对照组比较明显升高(P < 0.01),表明突触体Ca2+发生内流;而50 mW/cm2微波辐射后Ca2+浓度与对照组比较差异无统计学意义(P > 0.05)。30和50 mW/cm2微波辐射后大脑皮质突触体乙酰胆碱释放均明显增加(P < 0.01),显示微波辐射后乙酰胆碱代谢活跃。
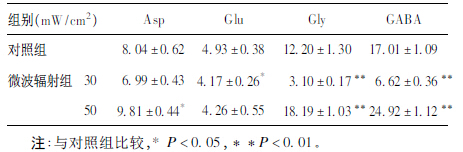
2.3 氨基酸递质释放量变化(表 2)| 表 2 不同组别大鼠突触体氨基酸递质释放量比较( x± s,n = 5) |
30 mW/cm2微波辐射后大脑皮质突触体Glu、Gly和GABA释放均明显减少(P < 0.05或P < 0.01);50 mW/cm2微波辐射后大脑皮质突触体 Asp、Gly和GABA释放均明显增加(P < 0.05或P < 0.01)。表明微波辐射后30 mW/cm2组以递质释放减少为主,50 mW/cm2组以递质释放增加为主。
3 讨 论研究发现,微波辐射可引起突触小体膜钙跨膜外排率增加,Ca2+-Mg2+-ATPase活性增加〔6〕。本研究发现,大脑皮质在30 mW/cm2微波辐射后突触体内Ca2+浓度升高。微波辐射后突触体内Ca2+浓度升高可能是递质释放障碍早期的一种代偿性反应。另一方面,由于细胞内Ca2+浓度升高,会造成钙超载,加重细胞损伤〔7〕。辐射后膜蛋白强弱固定化比增加,表明微波辐射可引起膜蛋白肽链断裂、蛋白质降解或交联膜蛋白流动性增加。突触体膜流动性升高可能是造成突触体内钙超载的原因之一,或由于高浓度Ca2+直接影响突触体膜的通透性,导致细胞能量代谢紊乱,细胞信号转导异常,二者可能均参与了突触结构损伤。
研究表明,微波辐射可引起神经递质代谢紊乱〔8, 9, 10〕。本实验发现,30 mW/cm2微波辐射后大脑皮质突触体氨基酸递质GABA释放减少;而50 mW/cm2微波辐射后大脑皮质突触体氨基酸递质释放增加。由于Ca2+是神经递质释放时所必需的,GABA释放减少后可能促使细胞内Ca2+浓度代偿性升高。由于释放于突触间隙的乙酰胆碱通过作用于突触后膜上的受体而发挥作用,并主要通过胆碱酯酶对其进行清除。因此,辐射后乙酰胆碱释放增加可能是微波辐射所引起的一种代偿性反应。
| 〔1〕 | Dunkley PR,Jarvie PE,Robinson PJ.A rapid percoll gradient procedure for preparation of synaptosomes[J].Nat Protoc,2008,3 (11):1718-1728. |
| 〔2〕 | 蒋青松,徐蜀远,杨俊卿,等.缺氧和/或缺糖对大鼠突触体游离钙浓度和氨基酸释放的影响[J].儿科药学杂志,2003,9(4):8-10. |
| 〔3〕 | 赵梅兰,王德文,曹晓哲.电磁脉冲辐照对海马神经元膜流动性的影响[J].中国医学物理学杂志,2001,18(3):171-175. |
| 〔4〕 | Wang SJ.Caffeine facilitation of glutamate release from rat cerebral cortex nerve terminals(synaptosomes)through activation protein kinase C pathway:an interaction with presynaptic adenosine A1 receptors[J].Synapse,2007,61(6):401-411. |
| 〔5〕 | 张慧灵,顾振纶,曹奕.夏天无总生物碱对痴呆大鼠学习记忆障碍及中枢胆碱能神经系统功能的影响[J].中国药理学通报, 2004,20(10):1158-1160. |
| 〔6〕 | 徐洋,赵宗群,张孙曦.微波对大鼠脑突触小体膜的钙外排率影响[J].卫生毒理学杂志,1999,13(2):109-112. |
| 〔7〕 | Orrenius S,Zhivotovsky B,Nicotera P.Regulation of cell death: the calcium-apoptosis link[J].Nat Rev Mol Cell Biol,2003,4 (7):552-565. |
| 〔8〕 | Testylier G,Tonduli L,Malabiau R,et al.Effect of exposure to low level radio frequency fields on acetylcholine release in hippocampus of freely moving mouse[J].Bioelectromagnetics,2002, 23(4):249-255. |
| 〔9〕 | 王丽峰,彭瑞云,胡向军,等.HPM对大鼠大脑结构及其神经递质的影响[J].中国公共卫生,2005,21(9):1059-1060. |
| 〔10〕 | 刘朝晖,王小娟,陈景藻,等.毫米波辐射对大鼠下丘脑及海马化合物含量的影响[J]. 中华物理医学与康复杂志,2002,24 (6):363-364. |
 2010, Vol. 26
2010, Vol. 26

 , 彭瑞云
, 彭瑞云